近日,来自重庆新桥医院、重庆西南医院及美国MD Anderson癌症研究中心等多家国内外机构的研究人员,通过外显子测序、RNA测序、转录组分析和T细胞库分析,对15例非小细胞肺癌(NSCLC)患者的肿瘤微环境进行了研究,发现肿瘤免疫微环境具有高度空间异质性并受突变驱动。此外,尽管局部总突变负荷(TMB)与局部的T细胞扩增有关,但是局部的抗肿瘤细胞毒性与肿瘤新生抗原没有直接关系。这些发现表明,在同一肿瘤微环境中,肿瘤免疫活性会发生显著变化,这为肿瘤免疫治疗精准分型提供了新的思路。相关研究于2018年12月18日发表在Nature Communication杂志,论文题为“Local mutational diversity drives intratumoral immune heterogeneity in non-small cell lung cancer”。

针对NSCLC的多种靶向药物已经研发成功并获批。其中,号称抗癌“神药”的PD-1抑制剂Nivolumab(纳武单抗)在针对NSCLC的一期临床和二期临床试验中取得了巨大成功,并可使患者获得持久性的治疗反应。遗憾的是,该药仅适用于一小部分人群。随着研究的深入,科学家发现TMB与抗肿瘤应答之间有着重要联系。
在该最新研究中,除了新抗原丰度和TMB外,研究人员还采用多种系统方法对免疫原性进行了评估。由于免疫空间异质性可能会削弱某些肿瘤预测标志物的反应,因此,研究人员开发了一种集成278个变量的机器学习算法来描述局部抗肿瘤反应。与仅仅关注TMB或者新抗原负荷相比,通过更全面的测量局部肿瘤的属性能够帮助改善对免疫疗法候选物的准确定义。这也该领域目前最为迫切的工作之一。
该研究团队表示,对于一些NSCLC患者,PD-1抑制剂Nivolumab目前已取得了显著的治疗效果。在此基础上,研究人员一直致力于探索与免疫治疗效果相关的肿瘤微环境特征。
1. TMB与局部T细胞扩增有关,与细胞溶解活性无关
为了评估免疫肿瘤抗原丰度与TMB之间的免疫原性,研究人员采取了一些互补性的方法。研究人员收集了15例NSCLC患者活体样本,并对于每一个样本进行了全外显子测序(WES)、转录组测序(RNA-seq)以及T细胞库测序[1],如图1。
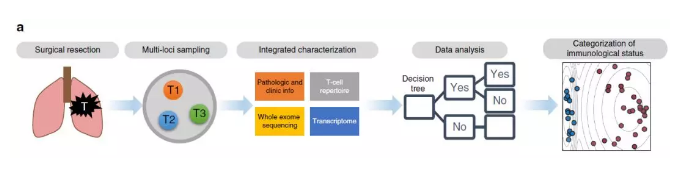
图1.对手术切除肿瘤进行多个组织位点高通量测序,包括非同义突变、HLA分型、肿瘤抗原的预测、转录组分析、T细胞测序,最后进行肿瘤微环境异质性分析
研究发现,高水平的TMB与肿瘤新生抗原特异的T细胞浸润以及T细胞集落形成有关,如图2。同时,研究人员还检测了T细胞颗粒酶A(GZMA)、INK-γ[2];并检测了一些能代表T细胞浸润性的标记物(CD8A、CXCL9、CXCL10、IFNG等),值得关注的是,研究人员最终并未发现以上参数与TMB有关[3],如图3。
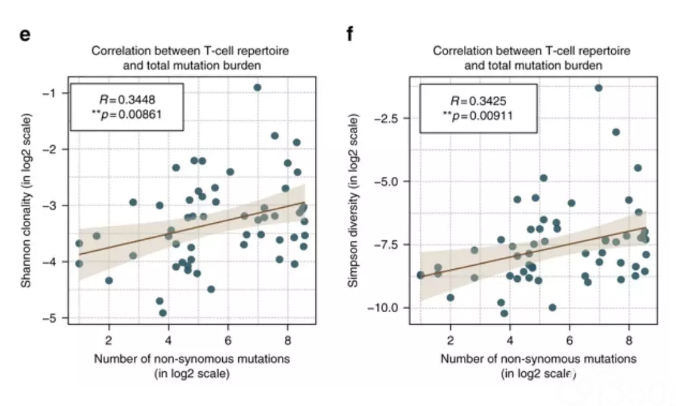
图2. e、f为表明肿瘤突变负荷与T细胞扩增之间关系的散点图。e为T细胞的集落形成能力,f为辛普森系数,用于预测T细胞库的组成
2. 突变异质性与免疫异质性有关
局部肿瘤抗原性和细胞毒性的不耦合表明[4],T细胞活性受到额外的免疫抑制调节。在肿瘤微环境中,存在两种可能的机制调节免疫抑制性:(1) 反馈诱导的检查点分子表达可抑制肿瘤浸润T细胞和免疫调节细胞的富集;(2) 不同的突变在修饰免疫反应应答中发挥不同的作用。
为了研究抑制性免疫细胞群的调控,研究人员构建了一个热点图来显示28个浸润性免疫细胞群的相对丰度。同时,他们观察到了两个主要特征:(1)免疫细胞浸润也具有空间性、孤立性,这导致了单个肿瘤内不同位点间的免疫细胞组成不均匀。(2)免疫热肿瘤区域整体具有较高的免疫细胞浸润度,包括具有抗肿瘤活性的细胞。具体来说,对于瘤内免疫异质性患者,6个突变中有5个(83%,患者024除外)表现为突变二分法,将冷区与热区分离为不同的进化方向。除了每个位点的同源(祖)突变外,热区与冷区肿瘤区域没有任何共同突变,如图3。
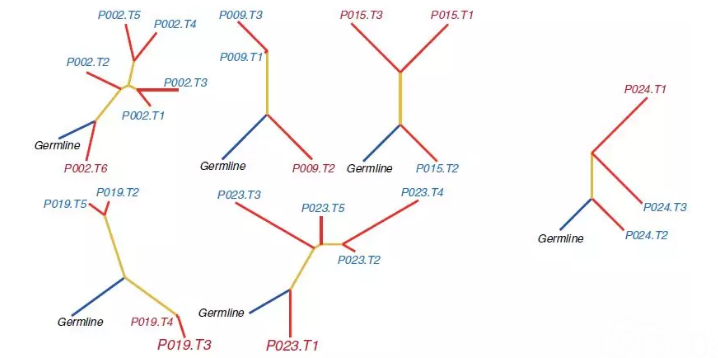
图3.对于异质性免疫状态的患者,检测到的突变分布的系统树状图
针对免疫治疗,研究人员认为,应谨慎使用过于简单的免疫监测策略,多元化参数以及多位点分析或将有助于评估肿瘤细胞内免疫环境的异质性,这将对发展更精确和更个体化的癌症免疫疗法具有深远的意义与影响。
3. 小结与展望
肿瘤的发生和发展不仅依赖于基因突变,还与肿瘤微环境的异质性密切相关。肿瘤异质性是恶性肿瘤的主要特征之一,免疫疗法的发展开启了消灭肿瘤的希望之门,但肿瘤异质性一直是攻克肿瘤的一大障碍。随着多区域活检、液体活检、单细胞测序等检测技术的不断发展,肿瘤异质性的更多奥秘逐步被揭示。想要实现真正的精准治疗,提高诊治水平、改善预后,肿瘤的异质性以及肿瘤免疫微环境的异质性都将是不可小觑的研究领域。
参考文献:
1. Morrissy, A. S. et al. Spatial heterogeneity in medulloblastoma. Nat. Genet. 49, 780–788 (2017).
2. Lavin, Y. et al. Innate immune landscape in early lung adenocarcinoma by paired single-cell analyses. Cell 169, 750–765 e717 (2017).
3. Spranger, S. et al. Density of immunogenic antigens does not explain the presence or absence of the T-cell-inflamed tumor microenvironment in melanoma. Proc. Natl. Acad. Sci. USA 113, E7759–E7768 (2016).
4. Rooney, M. S., Shukla, S. A., Wu, C. J., Getz, G. & Hacohen, N. Molecular and genetic properties of tumors associated with local immune cytolytic activity. Cell 160, 48–61 (2015).


