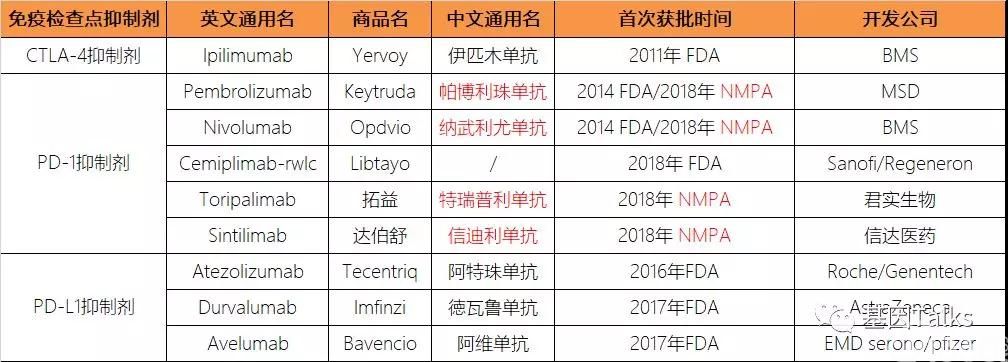
▲ 免疫检查点抑制剂主要包括CTLA-4抑制剂与PD-(L)1抑制剂,目前FDA及NMPA一共批准9款ICIs上市
Nature Reviews Cancer 发表了一篇综述,描述了预测免疫检查点抑制剂(ICIs )疗效的生物标志物最新进展,讨论了肿瘤与宿主基因组、肿瘤微环境和免疫功能相互作用产生的机制基础。

▲ 检查点抑制剂免疫治疗生物标志物的发展前景
免疫检查点抑制剂原理T细胞活化需要两个信号:信号1是MHC呈递的免疫原性肽抗原能与TCR结合;信号2又称为共刺激,通过将T细胞共刺激表面受体CD28连接到专业抗原呈递细胞(APCs)表面的配体CD80(B7-1)和CD86(B7-2)转导。(CTLA-4与CD28竞争结合CD80和CD86,CTLA-4可抑制T细胞活化,CD28可激活T细胞活化)。
T细胞杀伤识别杀伤肿瘤细胞的过程中,PD-1与其配体PD-L1的结合会抑制TCR下游的信号传递,从而阻断了信号1。PD-L1经常在肿瘤或肿瘤微环境中表达。因此,PD-1靶向或PD-L1靶向抗体疗法可以在肿瘤部位重新激活“疲惫”的T细胞。
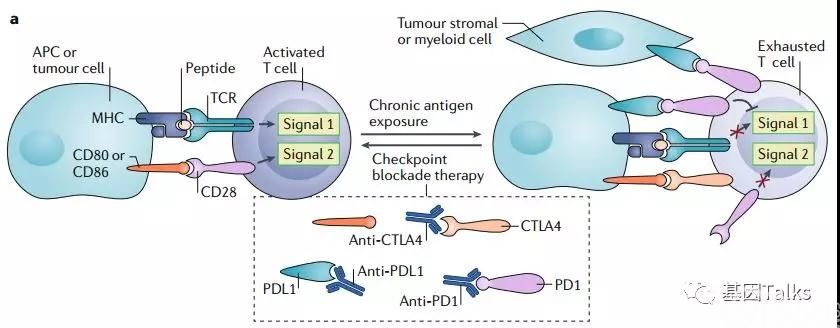
▲ 免疫检查点抑制剂的原理
免疫检查点就好像是一个关卡,告诉免疫系统是该继续杀,还是“下班休息”。肿瘤细胞正是利用了免疫检查点的指挥功能,让机体的免疫系统一直处于“下班休息”的状态,不能正常工作。免疫检查点抑制剂正是通过抑制肿瘤细胞发出的“下班休息”的信号,恢复免疫系统的正常工作,进而对肿瘤细胞发动进攻。免疫检查点抑制剂主要包括CTLA-4抑制剂与PD-(L)1抑制剂,主要针对免疫T细胞激活过程中的两个关键免疫检查点通路:CTLA-4/B7-1/2和PD-1/PD-L1。
免疫检查点抑制剂是通过激活T细胞发挥抗肿瘤作用,影响其疗效的因素可以大致分为两类:一类是与激活T细胞相关的肿瘤基因组特征,包括激活T细胞的新生抗原、产生新生抗原的体细胞突变、决定抗原提呈的HLA、识别新生抗原的TCR等;另一类是与肿瘤相互作用的免疫微环境,包括肿瘤中PD-L1表达、T细胞浸润以及其它免疫细胞等。
免疫检查点抑制剂40种生物标志物
在免疫检查点抑制剂的所有的生物标志物中,TMB、PD-L1表达和dMMR/MSI是经过三期临床试验验证的,在临床上使用比较普遍:
1,TMB可以预测 ICIs 疗效,并且可以作为泛癌种免疫治疗的标志物(正相关)。检测样本类型为:血液或肿瘤组织;检测方法为:WES或 NGS 大panel测序。
2,PD-L1表达可以预测 ICIs 疗效,并且可以作为泛癌种免疫治疗的标志物(正相关)。检测样本类型为:肿瘤组织;检测方法为:免疫组化。
3,dMMR/MSI 可以预测 ICIs 疗效,并且可以作为泛癌种免疫治疗的标志物(正相关)。检测样本类型为:血液或肿瘤组织;检测方法为:promega-MSI,qPCR,NGS或dMMR免疫组化。
其他生物标志物,都处于临床待定状态(TBD, To Be Determined),比如:
4,体细胞CNV变化:可以预测或/和预后 ICIs 反应,并且可以作为泛癌种免疫治疗的标志物(负相关)。检测样本类型为:肿瘤组织;检测方法为:WES或 NGS 大panel测序。
5,HLA-I类多样性:可以预测 ICIs 反应,并且可以作为黑色素瘤和非小细胞肺癌免疫治疗的标志物(正相关)。检测样本类型为:血液;检测方法为:WES或 PCR方法。
6,HLA I类等位基因的杂合性缺失(LOH):可以预测 ICIs 反应,并且可以作为黑色素瘤免疫治疗的标志物(负相关)。检测样本类型为:肿瘤组织;检测方法为:待定。
7,T细胞库克隆性改变:可以预测 ICIs 反应,并且可以作为黑色素瘤免疫治疗的标志物(正相关)。检测样本类型为:血液或肿瘤组织;检测方法为:待定。
8,T细胞炎症微环境:可以预测或/和预后 ICIs 反应,并且可以作为泛癌种免疫治疗的标志物(正相关)。检测样本类型为:肿瘤组织;检测方法为:RNA-seq或免疫染色。
9,SERPINB3/SERPINB4基因突变:可以预测 ICIs 反应,并且可以作为黑色素瘤免疫治疗的标志物(正相关)。检测样本类型为:肿瘤组织;检测方法为:WES。
10,肠道微生物多样性:可以预测 ICIs 反应,并且可以作为黑色素瘤免疫治疗的标志物(正相关)。检测样本类型为:口腔或肠道微生物;检测方法为:NGS或PCR方法。
11,特定肠道微生物种类:可以预测 ICIs 反应,并且可以作为黑色素瘤免疫治疗的标志物(正相关或负相关)。检测样本类型为:口腔或肠道微生物;检测方法为:NGS或PCR方法。
12,TGFβ表达:可以预测 ICIs 反应,并且可以作为结肠癌和尿路上皮癌免疫治疗的标志物(负相关)。TGF-β是具有包括免疫功能在内的多功能细胞因子,也是禁止T细胞进入肿瘤微环境的“哨兵”。检测样本类型为:肿瘤组织;检测方法为:RNA-seq或基因表达panel。
13,典型Wnt/β-catenin信号通路突变:可以预测 ICIs 反应,并且可以作为黑色素瘤免疫治疗的标志物(负相关)。检测样本类型为:血液或肿瘤组织;检测方法为:WES,NGS 大panel 或者RNA-seq。
14,JAK1/2突变(较罕见):可以预测 ICIs 反应,并且可以作为黑色素瘤免疫治疗的标志物(负相关),与耐药有关。检测样本类型为:血液或肿瘤组织;检测方法为:WES或 NGS 大panel测序。
15,B2M突变(较罕见):可以预测 ICIs 反应,并且可以作为黑色素瘤免疫治疗的标志物(负相关),与耐药有关。检测样本类型为:血液或肿瘤组织;检测方法为:WES或 NGS 大panel测序。
16,STK11突变(较常见):可以预测 ICIs 反应,并且可以作为非小细胞肺癌免疫治疗的标志物(负相关)。检测样本类型为:血液或肿瘤组织;检测方法为:WES或 NGS 大panel测序。
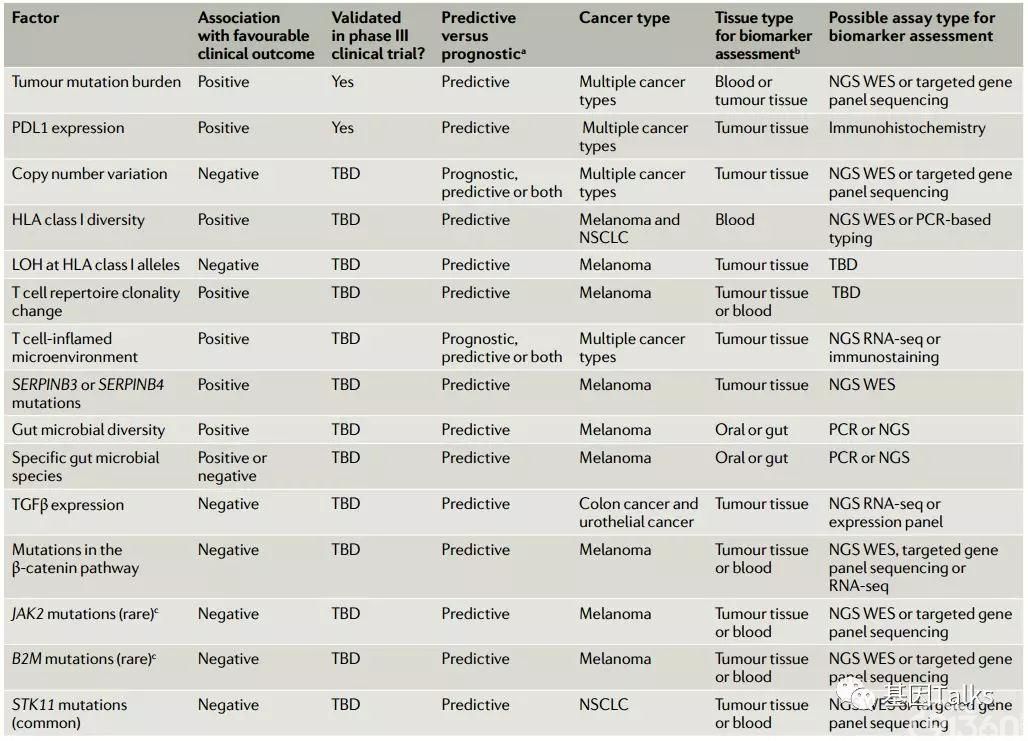
▲ 预测免疫检查点抑制剂治疗反应的因素
除了以上汇总的免疫检查点抑制剂生物标志物以外, 小编了解到的还有(临床待定状态,TBD):17,肿瘤浸润淋巴细胞(TIL):TIL密度(CD8+T细胞浸润量)与PD-L1的适应性上调和临床获益相关,可以预测 ICIs 反应,正相关;
18, TIL衍生的干扰素-γ(IFN-γ): IFN-γ一方面可以抑制肿瘤细胞增殖并增强免疫活性。另一方面,IFN-γ促进肿瘤细胞上的PD-L1表达,协助肿瘤细胞的免疫逃逸。可以预测 ICIs 反应,正相关;
19,肿瘤坏死因子-α(TNF-α):可以预测 ICIs 反应,正相关;
20,白细胞介素-6(IL-6):可以预测 ICIs 反应,正相关;
21,肿瘤新生抗原:可以预测 ICIs 反应,正相关;
22,POLD1基因突变:可以预测 ICIs 反应,正相关;
23,POLE基因突变:可以预测 ICIs 反应,正相关;
24,KRAS基因突变:可以预测 ICIs 反应,正相关;
25,TP53基因突变:可以预测 ICIs 反应,正相关;
26,PBRM1失活突变:可以预测 ICIs 反应,正相关;
27,肥胖:可以预测 ICIs 反应,正相关/无相关;
28,HIV等病毒感染:可以预测 ICIs 反应,正相关;
29,DDR基因突变:比如:BRCA1,BRCA2, BLM, FANCA,TP53,RAD51C,ATM,和MSH2基因等几十个基因。可以预测 ICIs反应,正相关;
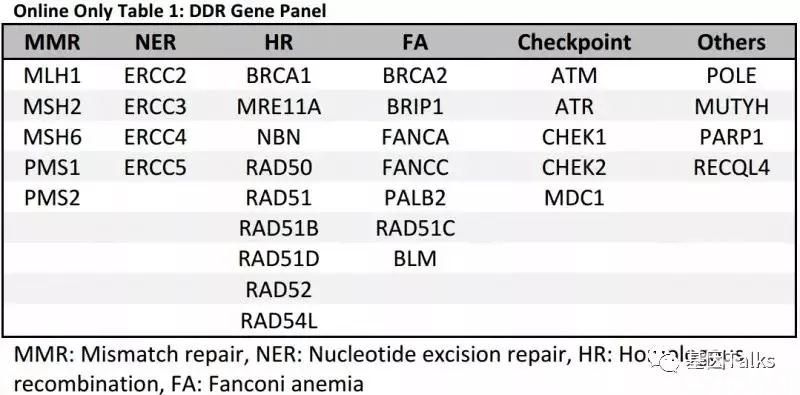
▲ DDR基因panel所包含的34个基因
肿瘤驱动基因的突变会影响PD-L1的表达,并进一步影响免疫抑制剂药物疗效:30,EGFR基因突变:可以预测 ICIs 反应,负相关;
31,ALK融合突变:可以预测 ICIs 反应,负相关;
32,ROS1融合突变:可以预测 ICIs 反应,负相关;
33,PTEN基因突变:可以预测 ICIs 反应,负相关;
34,MET基因突变:可以预测 ICIs 反应,负相关;
35,CCND1基因扩增:可以预测 ICIs 超进展,正相关;
36,FGF19基因扩增:可以预测 ICIs 超进展,正相关;
37,FGF3基因扩增:可以预测 ICIs 超进展,正相关;
38,FGF4基因扩增:可以预测 ICIs 超进展,正相关;
39,MDM2基因扩增:可以预测 ICIs 超进展,正相关;
40,MDM4基因扩增:可以预测 ICIs 超进展,正相关;
......
随着临床研究的深入,我们其实可以发现太多太多与免疫检查点抑制剂反应相关的生物标志物,因此建立由多种生物标志物组成的预测模型对于患者选择药物和精准医学是非常重要的。
不过,在目前缺乏确定的前瞻性研究数据的情况下(或三期临床验证),免疫检查点抑制剂生物标志物的应用还需谨慎,后续有必要进行前瞻性的研究来明确免疫检查点抑制剂生物标志物的临床应用地位。
