虽说有了CAR-T和PD-(L)1抗体这两种不错的免疫疗法,科学家们也从来没有停止过去寻找效果更好、副作用更少的新方法。
近日,中国第三军医大学和清华大学的科学家们发现,核受体NR4A1调控了T细胞的功能障碍,或可成为肿瘤免疫治疗的新靶点。而美国拉霍亚免疫学研究所的科学家更进一步,在CAR-T细胞中去除了NR4A家族,获得了更好的治疗效果,大幅延长荷瘤小鼠的生存时间。这两项研究在Nature上同期发表[1,2]。
免疫这活儿,实在是不好干,又要杀敌,又不能伤害正常组织。为了避免免疫系统和各种病原体、癌细胞的战争波及无辜的正常组织,各种免疫细胞上都有一些抑制性的免疫检查点,与正常组织上的相应配体作用,抑制过度的免疫反应,比如T细胞上著名的PD-1。
不过在肿瘤中,这一套避免过度的免疫反应的系统却被肿瘤劫持了,用来保护肿瘤自己逃避免疫系统的监视和绞杀。对此,PD-1抗体等免疫检查点抑制剂应运而生,阻断免疫检查点的抑制信号,释放免疫系统的潜能,杀死肿瘤。
但是目前的免疫检查点抑制剂,疗效虽好,有效率却不是很高[3],虽说可以通过肿瘤突变负荷来预测治疗效果,但要是能有疗效更好 ,适用范围更广的方法就更好了。
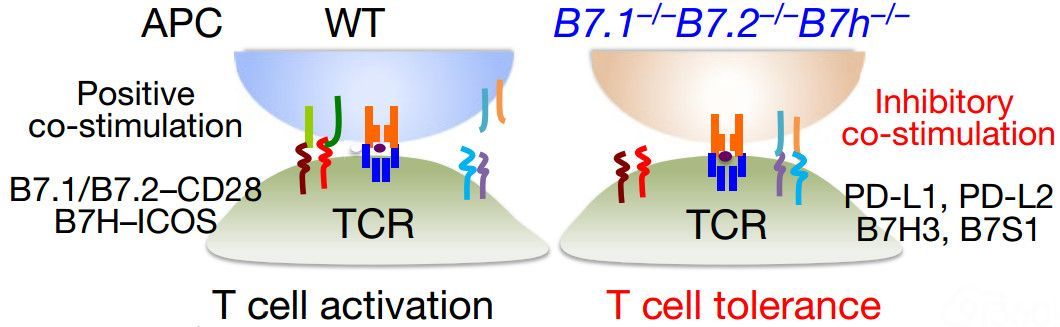
研究人员通过模拟免疫耐受,诱导T细胞功能障碍
对此,清华大学的董晨教授和他的研究团队,用他们自己开发的方法诱导出功能障碍的T细胞,并对其进行了全转录组和表观遗传学评估,试图找出一种更为彻底的释放免疫系统潜能的方法。
研究人员发现这些功能障碍的T细胞与正常的T细胞有着很大的差别,它们失能相关基因和转录抑制因子表达升高,而产生免疫作用的IL-2等效应因子和掌管蛋白质翻译核糖体相关基因表达下降。进一步的信号网络分析显示,核受体NR4A1可能与T细胞的耐受有着密切的联系。
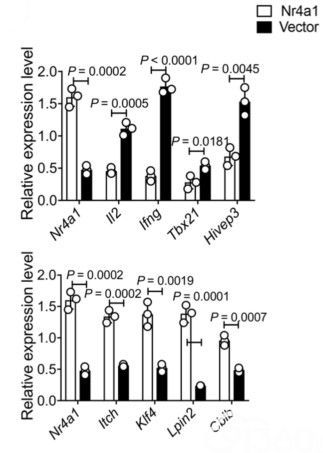
过表达NR4A1让分泌IL-2相关基因表达下降(上),T细胞失能相关基因表达上升(下)
有了目标,接下来就该去验证了。研究人员在CD4+T细胞中过表达了NR4A1,发现其生产的免疫因子IL-2减少了,失能相关基因表达升高了,还抑制了向Th1细胞和Th17细胞的分化。而在CD8+T细胞中过表达NR4A1,也让免疫因子IFN-γ的产量下降了。
反之,如果敲除掉T细胞中的NR4A1,IL-2和IFN-γ的产量都会提高,T细胞的增殖也会变快。如果把这些NR4A1缺失的T细胞接种到结肠炎小鼠上,小鼠的炎症也会加重,体重减轻更为明显。
而在荷瘤小鼠上,缺失NR4A1的肿瘤特异性T细胞,则能更有效的在肿瘤中浸润,杀灭肿瘤。而且这些T细胞表面,免疫检查点分子PD-1和TIM-3的表达也大为降低了。
而这个TIM-3的配体,经常会在接受PD-1阻断治疗后,在肿瘤里上调,正是肿瘤逃避免疫治疗的机制之一[4]。
NR4A1及其相关通路,很可能是一个有前途的肿瘤免疫治疗新靶点!
不过在治疗上,美国的团队走在了前面。他们分析了黑色素瘤小鼠中,T细胞衰竭的标志物,发现NF-AT和NR4A家族可能是导致T细胞衰竭的元凶。
随后,美国的科学家测试了敲除NR4A家族在CAR-T疗法中的作用。结果显示,敲除了NR4A1、NR4A2和NR4A3的CAR-T细胞,疗效好于普通的CAR-T,也好于单独敲除其中一种NR4A的CAR-T。
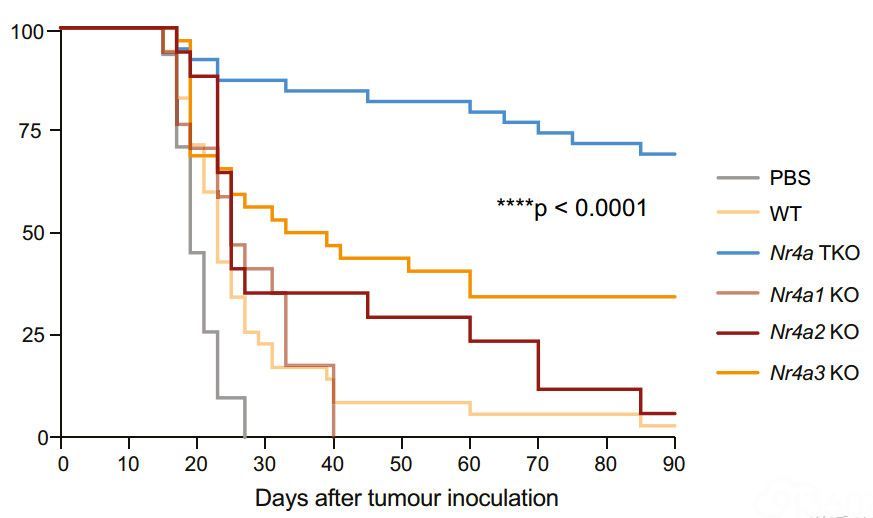
敲除NR4A家族后,CAR-T治疗效果明显改善
不过这篇论文的第一作者Joyce Chen也表示:“在这个研究结果和将其转化为临床治疗方法之间仍有许多步骤。在不确定安全后果的情况下,不可能随意地编辑人类细胞中的多个基因。然而,了解NF-AT和NR4A转录因子的作用可以解开免疫学中的一个谜,为癌症研究人员设计更好的治疗方案提供了一个新的目标。”
参考文献:
1. LIU X, WANG Y, LU H, et al. Genome-wide analysis identifies NR4A1 as a key mediator of T cell dysfunction[J]. Nature, 2019.
2. CHEN J, L PEZ-MOYADO I F, SEO H, et al. NR4A transcription factors limit CAR T cell function in solid tumours[J]. Nature, 2019.
3. Chen P L, Roh W, Reuben A, et al. Analysis of immune signatures in longitudinal tumor samples yields insight into biomarkers of response and mechanisms of resistance to immune checkpoint blockade[J]. Cancer discovery, 2016, 6(8): 827-837.
4. Koyama S, Akbay E A, Li Y Y, et al. Adaptive resistance to therapeutic PD-1 blockade is associated with upregulation of alternative immune checkpoints[J]. Nature communications, 2016, 7: 10501.
