免疫治疗是当前恶性肿瘤治疗的一个重要里程碑,改变了恶性肿瘤尤其是非小细胞肺癌的治疗模式。对于免疫治疗适宜人群的筛选和疗效预测的生物标志物虽然越来越多,但PD-L1仍然是目前应用最为广泛的生物标记。免疫组化检测是评估组织PD-L1表达状态的一种最常用方法,广泛应用于包括非小细胞肺癌(NSCLC)等各种恶性肿瘤中。IASLC 病理委员会对2019年肺癌中PD-L1检测相关文献进行了回顾性梳理和总结,并提出了IASLC病理委员会的观点。91360邀请陆军军医大学第一附属医院阎晓初教授针对IASLC关于PD-L1检测的内容进行解读。

1 本文开始就对靶向PD-1/PD-L1的免疫抑制剂用于晚期肺癌的治疗进行了归纳,您认为这些归纳说明了什么?
阎晓初教授:在本文的第一部分,IASLC总结了2019年肺癌免疫治疗的适应症,这些适应症包括转移性NSCLC的一线、二线或后线治疗;不能手术切除的局部晚期NSCLC一线治疗(美国和日本);转移性小细胞肺癌(SCLC)的三线或后线治疗;联合化疗用于转移性NSCLC和SCLC的一线治疗;单药用于放化疗后无进展的不能切除的局部进展期III期NSCLC的巩固治疗等。这些肺癌免疫治疗适应症的批准扩展了免疫治疗的应用范围,几乎涵盖了所有晚期肺癌,再次证明了免疫治疗的临床治疗效果,也突出表明需要继续深化和加强免疫治疗的作用。文中还对上述适应症相关的临床试验结果进行了较为详细的描述,在这些临床试验中都探索了PD-L1与疗效之间的关系,这也说明PD-L1表达水平对于免疫治疗方案的选择非常重要,也表明PD-L1仍然是免疫治疗中的一个重要生物标志物。
2 文章第二部分总结了PD-L1在免疫治疗疗效预测和患者预后的作用,请您结合个人经验谈谈PD-L1在预测和预后中价值。
阎晓初教授:目前肺癌开展的临床试验大多数是以肿瘤组织中PD-L1 TPS表达水平来进行的,而且这些临床试验也证实了PD-L1 TPS表达水平与免疫治疗具有一定的临床相关性,荟萃分析也表明不同PD-L1表达状态的患者经免疫治疗后可具有不同的生存获益。这些研究都证实了PD-L1表达可作为预测肺癌对免疫治疗疗效的一种有效的生物标志物。虽然PD-L1是一个比较好的预测免疫治疗疗效的生物标志物,但有些临床试验却未能获得相似的结果,而且,PD-L1表达与免疫治疗疗效尚未存在绝对的相关性,因此,PD-L1作为免疫治疗的预测生物标记物还不完美,需要进一步完善。也有研究表明PD-L1可作为肺癌预后的生物标志物,但因为不同研究中使用的队列设置,肿瘤分期,PD-L1截断值不相同,导致结果可能会有偏倚。本文还报道最新的荟萃分析和一项亚洲亚组分析显示PD-L1阳性患者预后差。因此,PD-L1表达的预后价值尚需要进一步研究,尤其是与目前作为预测性生物标记物的截断值结合可能更有临床价值。
3 目前PD-L1检测主要采用免疫组化方法,但影响因素较多;另外,临床检测标本类型多样,部位也不一样,PD-L1检测结果是否一致,一直是病理和临床医生关注的问题。请根据您的经验对本部分内容进行解读。
阎晓初教授:这部分内容应该说是这篇文章的中心内容,在这篇文章中,IASLC病理委员会对影响PD-L1检测结果的因素尤其是一般因素进行了具体分析,并根据美国临床肿瘤学会和美国病理医师学会的要求,对每个影响因素给出了最佳条件,具体见表1。
表1:PD-L1免疫组化最佳的分析前条件*
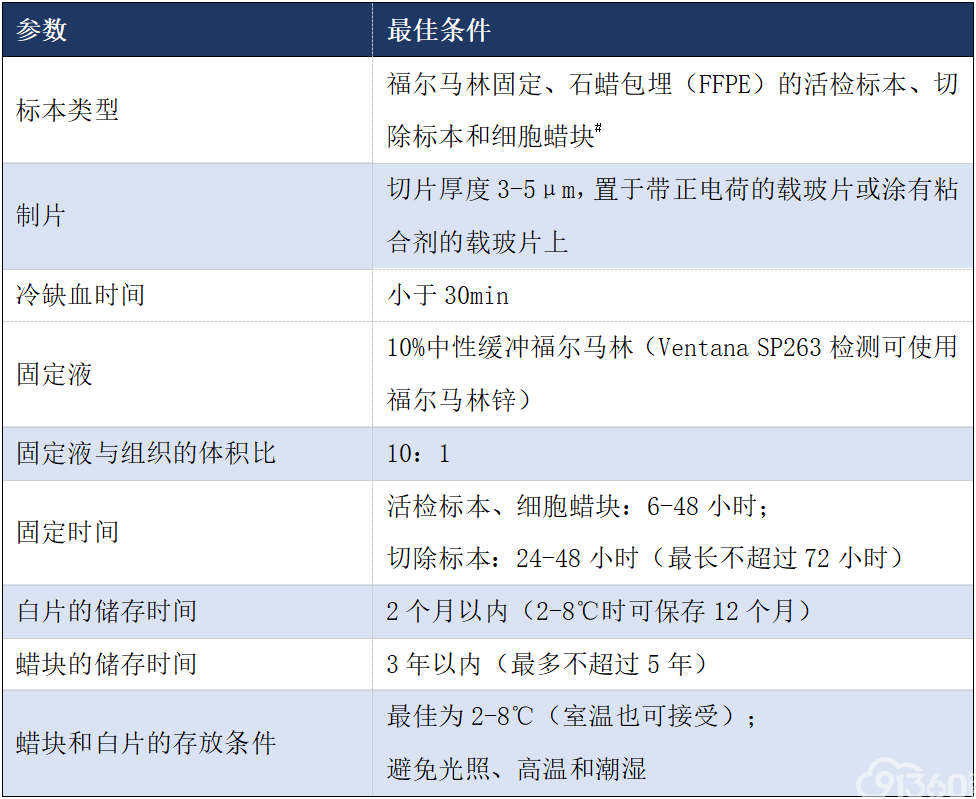
*:这些都是理想的条件,可在各个实验室进行验证,以获得较好的执行特征。
#:PD-L1免疫组化在脱钙组织和细胞学标本上可能获得验证。
在日常工作中,表里的每一个环节都影响着最终的PD-L1结果,这就要求我们在日常工作中应做好每一步,从标本离体开始就应关注标本的检测流程,应做到标准化,这样检测出来的结果才可靠。在这些影响因素中,我认为尤其要关注冷缺血时间、固定液种类、固定液与组织的体积比以及固定时间,因为这些影响因素和临床医生取样关系极大,也是病理科难以掌控的因素,这就需要加强病理科与相关科室的联系,加强多学科合作,设计好整个检测流程的标准操作程序,严格质控和监督,这样才能最大程度减少PD-L1检测结果不准确的机率。
在活检标本与手术切除标本PD-L1表达的比较中,准确反映肿瘤PD-L1状态的组织取样是一个重要问题。对于不能手术的NSCLC患者,是否可以进行免疫治疗可能往往根据小活检标本中PD-L1表达情况来决定。有研究显示,采用不同的截断值时,两种标本间PD-L1一致性不同,截断值越低,一致性越好。此外,最近的一项研究表明,为了评估PD-L1的表达并预测患者对nivolumab治疗的反应,一次活检标本中至少需要有100个肿瘤细胞。这些研究结果说明标本类型不同,PD-L1表达不一致,这也是我们在实际工作中面临的如何选择标本类型的问题:当有手术切除标本时,应优先选择手术切除标本,选择1个具有代表性蜡块进行PD-L1染色可以反映PD-L1在整个肿瘤中的表达;对于活检标本,标本中至少含有100个肿瘤细胞才能预测免疫治疗疗效;同时也建议临床医生在病情允许的情况下,尽量获取更多的组织进行病理学检测,才能更加准确地反映肿瘤组织中PD-L1的表达。
细胞学标本中PD-L1检测的价值在临床试验中尚未得到完全证实,但大多数基于细胞学标本(有或无细胞蜡块)的研究发现,细胞学标本和组织学标本之间的PD-L1表达水平存在良好的相关性,并且与免疫治疗的客观临床反应也存在相关性,这说明当无法获得组织标本的情况下,采用细胞学标本进行PD-L1检测也是一种可以接受的方法。但应首先对细胞学标本检测方案进行验证,并且做好质量控制。另外,值得关注的是,细胞学标本中肿瘤细胞含量可能达不到100个,细胞学标本中肿瘤细胞数量是否也要符合组织学标本中的最低值目前还没有相关的研究,尤其与临床治疗的相关性需要值得进一步研究。
原发灶与淋巴结转移和远处转移灶PD-L1比较研究中发现它们的一致性相对较低,尽管这些研究中病例数量、IHC检测方法和采用的截断值不同,但这些研究结果提示转移性肿瘤还是原发灶中PD-L1检测结果,哪一个更能作为免疫治疗的生物标记物目前尚不清楚。因此,我们认为加强这方面的研究可能对临床选择组织样本进行PD-L1检测具有指导意义。
化疗/放疗对肿瘤组织中PD-L1表达的影响同样值得关注,我们知道PD-L1是一种免疫相关分子,其表达水平会随着肿瘤微环境的变化而波动,有研究结果提示PD-L1在化疗/放疗前后存在表达差异,而且发现化疗后高PD-L1表达患者化疗反应差和预后较差。除了放化疗会影响PD-L1的状态,也有研究显示TKI治疗也会影响PD-L1的表达。所以我们说PD-L1不是一个完美的生物标志物,还有很多现实的问题需要解决。
4 目前FDA批准的PD-L1检测涉及到4种商业化抗体和2种检测平台,但国内很多单位并不同时具备上述2种检测平台,甚至有些单位采用实验室自建的检测技术(LDT)。请您结合文中有关内容谈谈您的建议。
阎晓初教授:PD-L1不同克隆号抗体和检测平台之间的一致性研究一直是大家比较关注的问题,不仅是肺癌,在其他恶性肿瘤如膀胱癌、胃癌等都有一些研究。本文第五章节IASLC病理委员会着重对FDA批准的4种商业化PD-L1 免疫组化检测抗体的一致性进行了相关的文献复习和总结。总的来说,这些比较研究结果显示22C3、28-8和SP263之间具有很好的一致性,而SP142在肿瘤细胞的染色上敏感性较低。
对于LDT检测平台,也有很多研究显示LDT的可行性,我认为这也是目前我们国内PD-L1检测面临的主要问题,目前国内获批的试剂盒只有DAKO的22C3和28-8 ,而DAKO的平台在我国的装机率并不是特别高,所以如何开展高质量的LDT检测是急需解决的问题。
质量控制是保证PD-L1检测结果可靠性的一个重要措施。除了做好室内质量控制,还应该积极参与外部质量保证计划,这是验证实验室质量控制的一个重要手段,只有达到并通过了外部质量验证,才能说明本实验室检测结果是可靠的,也更具有法规的保证。
5 PD-L1检测结果的判读也是PD-L1检测的一个重要环节。实际工作中,PD-L1判读存在差异,您认为如何减少这方面的差异?
阎晓初教授:PD-L1检测后期的一个重要工作是检测结果的判读。对于22C3、28-8和SP263采用TPS评分,而对于SP142则需要判读肿瘤细胞和浸润性免疫细胞,这些评分存在判读者自身及判读者之间的差异,尤其是SP142,这样可能会导致PD-L1检测结果在不同医院或不同医生之间存在差异。为了解决这个问题,我非常同意IASLC病理委员会的意见,即加强培训,通过各种线上或线下培训来提高病理医师对PD-L1判读的水平,这样提高检测结果的可重复性。如BluePrint 二期研究中,经过1.5天培训的24名肺病理学家(IASLC病理委员会成员)用5种经过试验验证的PD-L1检测方法对71例临床NSCLC样本进行评估,所有检测方法对PD-L1 TC评估均具有良好的一致性。另外,对于PD-L1检测,最好借鉴既往乳腺癌HER2和肺癌ALK检测和判读等培训经验,依托学会和协会组织不同级别和层次医院进行规范化培训,并开展相应室间质控,这样才能不断提升检测者的能力和水平,从而整体提高我国PD-L1检测结果的准确性。
最后,该病理委员会还对标准化报告和解释规则作出了推荐,主要包括一般信息,包括患者ID、标本ID、运行日期、肿瘤的组织学诊断、标本类型(活检、手术标本、细胞蜡块)、固定剂以及标本中是否有足够数量的肿瘤细胞。有关检测方法的信息应包括抗体克隆号、自动染色平台,以及是否为商业性检测或LDT。这样有利于临床医生根据检测结果结合相关临床试验进行解读并给予相应地治疗。
IASLC病理委员会对2019年肺癌组织中PD-L1检测进行了全面的文献回顾和总结,重点对影响PD-L1检测结果的分析前、分析中和分析后因素进行了分析,并提供了一些建议,这对于提高PD-L1检测结果的准确无疑具有重要作用。然而,不同国家或实验室具有不同的特点,制定适合于各地具有循证医学证据的检测指南对于提高PD-L1检测结果,更有利于指导临床筛选免疫治疗受益人群和预测免疫治疗疗效。
NP/IO/4625/04/28/20-04/28/22
