在过去的十年间,细胞病理学报告系统得到了飞速发展,不断出版并更新各领域的报告系统。比如:2015年修订第三版宫颈细胞学Bethesda报告系统,2018年更新第二版甲状腺细针穿刺细胞学Bethesda报告系统,随着2022年第五版WHO内分泌系统的更新,已于今年年初更新至第3版。但可惜的是,细胞病理学不同领域采用不同报告系统,到目前为止,还没有一套国际公认且相对统一的报告系统。为了实现这一目标,由国际细胞学学会(International Academy of Cytology,IAC)和国际癌症研究机构(International Agency for Research in Cancer,IARC)牵头,与世界卫生组织(World Health Organization,WHO)联合在2020年签署了一份协议,开发一套与组织学WHO蓝皮书相同的统一的细胞学报告系统。
经过两年的努力,WHO肺部细胞学和胰胆管细胞学章节已于2022年底完成并出版,2023年将进一步完成淋巴结、软组织、胸腺和脾脏部分,后续将继续编写肝脏、乳腺、肾/肾上腺等章节。今天将跟大家一起分享WHO细胞学报告系统第一章——肺部细胞学。
WHO肺部细胞学报告系统诊断类别及报告术语:经过两年的努力,WHO肺部细胞学和胰胆管细胞学章节已于2022年底完成并出版,2023年将进一步完成淋巴结、软组织、胸腺和脾脏部分,后续将继续编写肝脏、乳腺、肾/肾上腺等章节。今天将跟大家一起分享WHO细胞学报告系统第一章——肺部细胞学。
WHO肺部细胞学共分为5个诊断类别:(1)标本量不足/不充分/无法诊断;(2)良性病变;(3)非典型细胞;(4)可疑恶性肿瘤;(5)恶性肿瘤。
WHO肺部细胞学各类别诊断标准:
1、标本量不足/不充分/无法诊断:
定义:指在数量或质量上缺乏足够的材料来进行可靠诊断的标本。
与其它系统不同的是,可获取肺部细胞学标本的方法有多种,所以标本满意标准一直无法得到共识。WHO首次尝试在肺部细胞学根据不同标本来源采用不同的满意标准。其标本满意标准如下:
(1)肺细针穿刺(FNAB)标本:应包括肺泡成分,即含肺巨噬细胞(通常含有碳末和/或含铁血黄素),并尽可能包括塌陷的肺泡间隔;
(2)经支气管超声引导下穿刺(EBUS-TBNA)标本:如果为淋巴结穿刺,应含中等或丰富的淋巴细胞/吞噬碳末的巨噬细胞,具体讲:即细胞丰富区高倍视野下淋巴细胞数量≥40个;
(3)痰标本:可见少量肺泡巨噬细胞和纤毛柱状细胞(注意:并未规定具体细胞数量);
(4)支气管刷检(BB):可见丰富的支气管上皮和巨噬细胞(未限定具体细胞数量);
(5)支气管冲洗(BW)和支气管肺泡灌洗液(BAL):可见多量肺泡巨噬细胞(BAL标本:>10个肺泡巨噬细胞/HPF);支气管上皮细胞可能存在,但不应超过肺泡巨噬细胞的数量。
标本量不足/不充分/无法诊断见于以下几种情况:
(1)细胞数量少;
(2)制片、固定或染色不佳;
(3)被血液、炎症细胞或其他物质遮盖;
(4)玻片中可见大量良性细胞,但无法解释影像学上的肺部肿块或肺结节。这种情况也可使用“良性病变”这一术语,并同时在报告中备注该样本可能无法代表影像学上看到的病变。
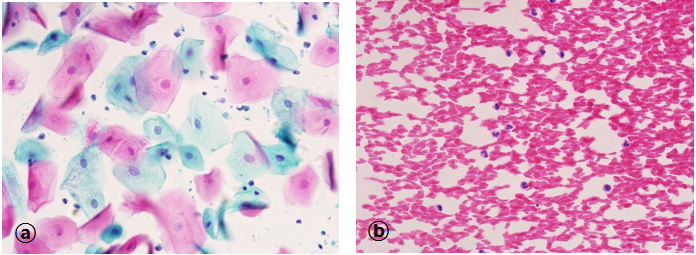
图1:标本量不足/不充分/无法诊断。图ⓐ:痰标本(巴氏染色×40)。图片中仅查见鳞状上皮和少量中性粒细胞,未见肺泡巨噬细胞和纤毛柱状上皮,提示并非肺深部痰,应咳深部痰重新送检;图ⓑ:纵隔穿刺标本(HE染色×40)。仅查见红细胞及少量中性粒细胞,未见淋巴细胞或巨噬细胞。
使用这个类别术语时需注意:
(1)为避免给临床医生造成混淆,一个实验室仅使用一种诊断术语即可,并注明诊断不足的原因及相应处理措施;
(2)出现任何非典型细胞,不应归为此类;
临床处理:
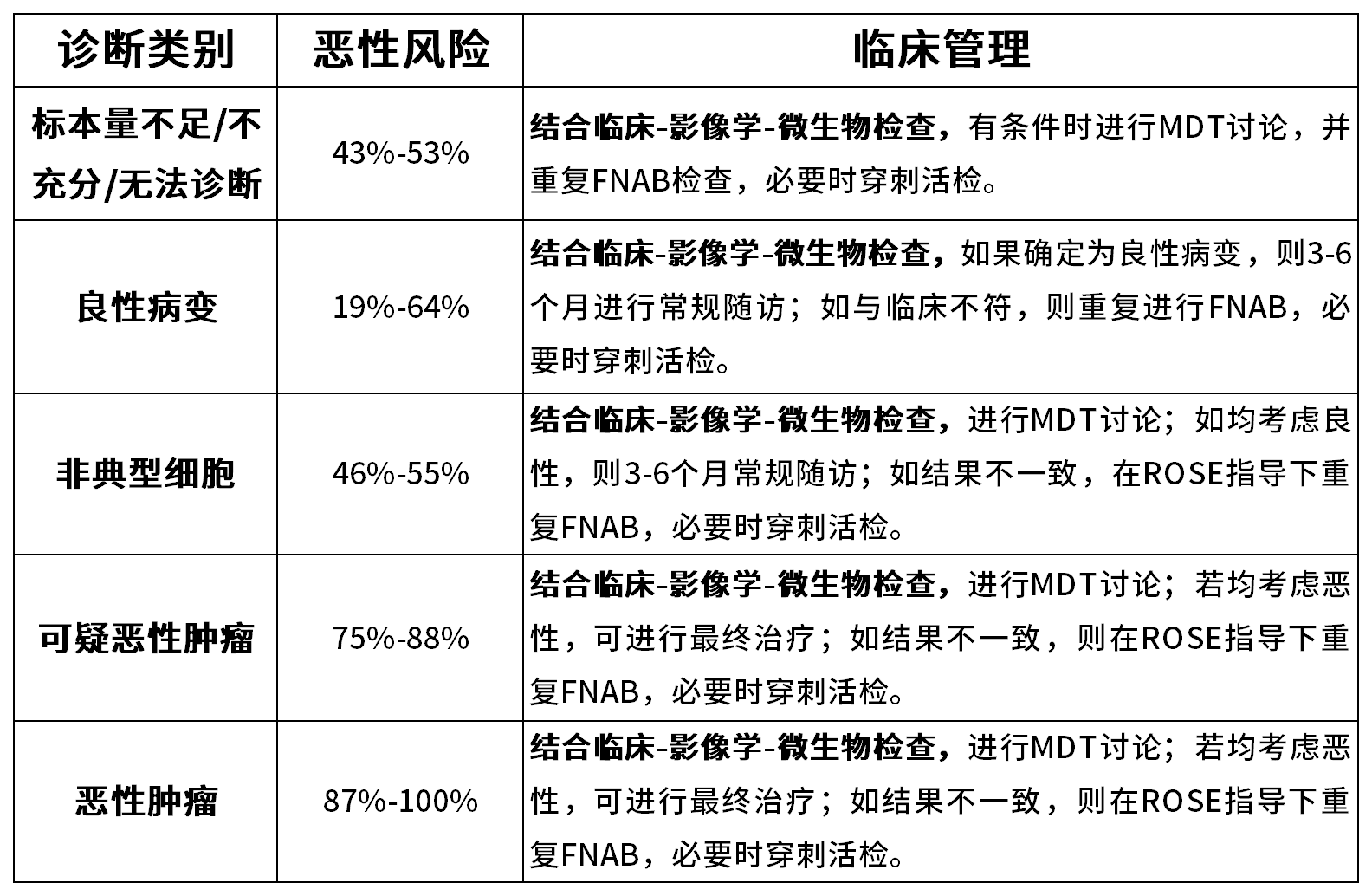
标本量不足/不充分/无法诊断这类诊断术语的恶性风险43%-53%(见表1),进一步处理依据诊断不足的原因及临床、影像和微生物检查结果,如送检为不满意的痰标本,则建议咳深部痰送检;如果影像学提示肺部肿块,经无创性检查痰、支气管刷检、支气管冲洗和支气管肺泡灌洗液等未获得满意标本时,可进行有创性EBUS-TBNA或纵隔镜等检查。
表1:WHO肺部细胞学报告系统:各诊断类别恶性风险及临床管理指南
2、良性病变:
定义:有明确的良性细胞病理特征,可能也可能不能诊断为特定的炎症或良性肿瘤。
见于以下几种情况:
(1)特定的炎症,如:化脓性或肉芽肿性炎;
(2)特定的肿瘤,如:肺错构瘤;
(3)肺正常细胞学成份,如:支气管上皮、巨噬细胞、肺泡间隔和2型肺泡上皮(如图3);
使用这个类别术语时需注意:
(1)此类诊断应结合影像学,如与影像学不符,应在报告中注明:细胞病理学结果可能不足以代表影像学上所看到的病变,并给出相应的处理建议;
(2)只要有可能,应尽可能报告具体类型;
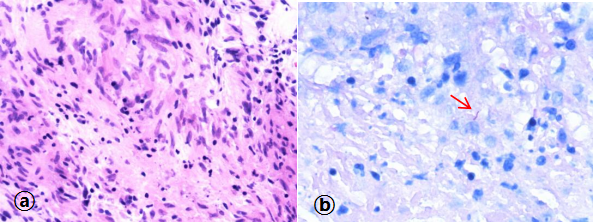
图2:良性病变。纵隔淋巴结穿刺。图ⓐ:可见肉芽肿性炎,中间可见干酪样坏死,提示为结核。(HE染色×20)。图ⓑ:抗酸染色×40,阳性证实为结核。
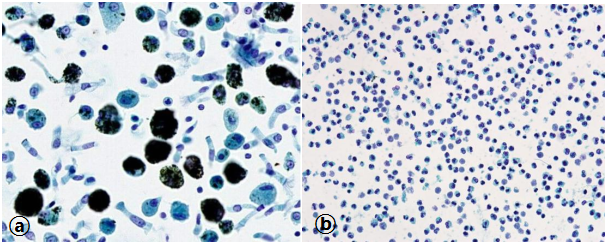
图3:良性病变。BAL,(巴氏染色×40)。图ⓐ:可见纤毛柱状上皮及多量吞噬碳末的巨噬细胞,符合临床尘肺病史。图ⓑ:查见大量中性粒细胞,与CT提示肺部阴影和临床考虑感染符合。
临床处理:
此类诊断术语的恶性风险为19%-64%,进一步处理需结合临床-影像学-微生物检查,若细胞学报告为良性且与临床符合,则3-6个月常规随访即可,若与临床不符,则进行重复FNAB或粗针活检。
3、非典型细胞:
定义:主要表现为良性病变,伴轻微的恶性病变可能,在数量或质量上不足以诊断为良性或恶性病变的标本。
非典型病变的主要原因如下:
(1)病变本身特征(反应性变化,如化生和增生、感染(特别是病毒性)、治疗后反应和急性呼吸窘迫综合征)
(2)操作者的专业知识;
(3)与制片相关的技术因素;
(4)病理医生的经验。
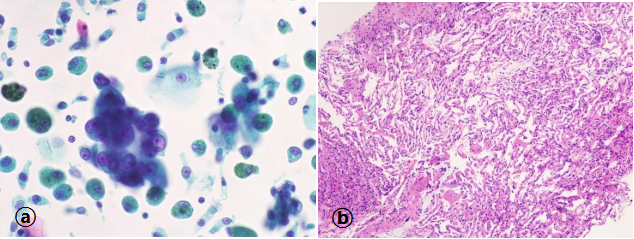
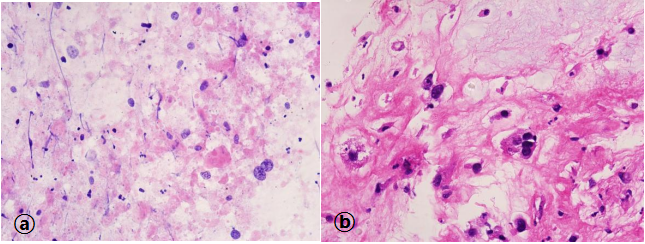
图4:非典型细胞。患者,男,34岁。CT提示肺部结节。图ⓐ:BAL,(巴氏染色×60)。可见一团三维立体细胞团,核增大,核仁明显。图ⓑ:该患者活检标本,未见肿瘤。
临床处理:
此类诊断术语的恶性风险为46%-55%,进一步处理需结合临床-影像学-微生物检查。如果影像学不典型或考虑恶性,则采用不同的取材方式进一步检查。如初次检查为痰标本,则下一步进行BW/BB;若非典型细胞来自BW/BB,则下一步进行EBUS-TBNA;若非典型细胞来自FNAB,可进行粗针穿刺活检。当然,如果影像学可以解释细胞学的非典型性,则定期随访即可。
4、可疑恶性肿瘤。
定义:细胞病理学特征提示恶性肿瘤,但因数量或质量不足而不能作出明确恶性肿瘤的诊断。
这一诊断术语具有一定的主观性,取决于病理医生的经验、标本类型及细胞的异型程度。快速现场评估(Rapid on site evaluation,ROSE)可降低可疑恶性肿瘤的诊断率。另外,免疫组化、分子检测等辅助检查有助于将“可疑恶性肿瘤”转为明确的“恶性肿瘤”。如当我们怀疑是小细胞癌的病例,可通过SYN、CD56、CgA及KI67免疫组化染色来证实。
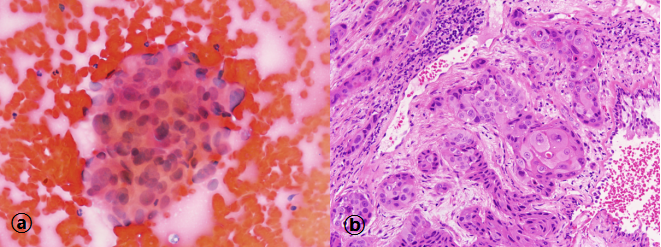
图6:可疑恶性肿瘤。图ⓐ:BB,(巴氏染色×40)。视野中央可见一团细胞,核大小不一,核形不规则,但因细胞退变显著,不足以直接诊断恶性。图ⓑ:该患者活检标本证实为鳞状细胞癌(HE染色×20)。
临床处理:
此类诊断术语的恶性风险为75%-88%,诊断为“可疑恶性肿瘤”并不是临床治疗的依据,应结合临床-影像-微生物检查,若均考虑恶性,可进行最终治疗;如果结果不一致,则需重复FNAB和/或穿刺活检。此外,辅助检查对于明确诊断具有一定的价值。
5、恶性肿瘤。
定义:具有明确恶性细胞病理学特征的标本。
使用这一诊断术语应尽可能进行亚分类,是原发性肿瘤还是继发性肿瘤,是腺癌、鳞癌、小细胞癌,还是少见的大细胞癌,亦或是肉瘤。
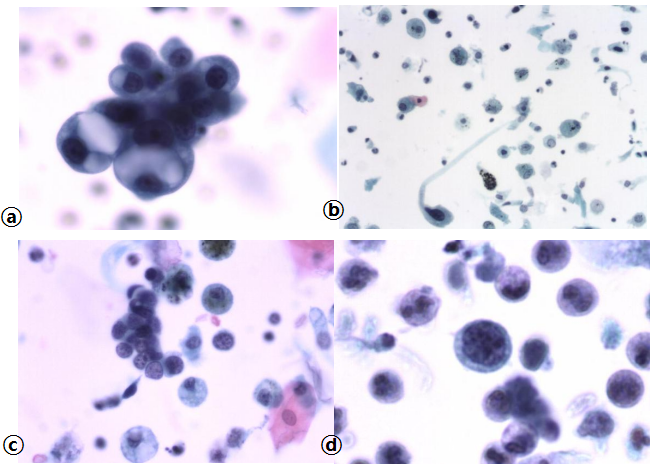
图7:恶性肿瘤。BAL,(巴氏染色×40)。ⓐ:腺癌。肿瘤呈典型的三维立体细胞团,细胞大小不一,胞浆内可见黏液空泡。ⓑ:鳞癌。可见异型拖尾的鳞状细胞。ⓒ:小细胞癌。肿瘤细胞呈小团状,胞浆少呈裸核状,镶嵌状排列,核染色质呈椒盐样。ⓓ:淋巴瘤。视野中央一个肿瘤细胞,胞浆较少,核浆比高,核膜不规则,染色质粗,活检证实为弥漫大B细胞淋巴瘤。
临床处理:
此类诊断术语的恶性风险为87%-100%,进一步处理与“可疑恶性肿瘤”相同,需结合临床-影像-微生物检查,如果均支持恶性,根据结果进行治疗,如果不一致,则需重复FNAB和/或穿刺活检。
总结:
WHO报告系统首次尝试在细胞病理学中使用标准化诊断术语和统一的报告系统,具有以下特点:
(1)提供详细的结构化报告模板供病理医生参考,为细胞病理报告的统一鉴定基础(表2);
(2)每个诊断类别对应不同的ROM以及诊断管理建议,从而改善临床医生和细胞病理学家之间的沟通;
(3)每个标准化术语建立细胞病理学关键诊断标准,增加诊断者之间的一致性;
(4)提供免疫组化、分子病理等辅助检测的指导意见,以利于个性化医疗;
(5)提供取样和制片方式的最佳建议,以优化细胞病理学样本的前期处理和制备过程;
(6)通过IARC网站直接将细胞病理学链接到第五版WHO肿瘤分类蓝皮书,为细胞病理学和组织病理学建立一个动态联系。
表2:WHO肺部细胞学标准化报告模板

1、Canberk S, Field A, Bubendorf L, et al.A brief review of the WHO reporting system for lung cytopathology. J Am Soc Cytopathol. 2023 Jul-Aug;12(4):251-257.
2、Schmitt FC, Bubendorf L, Canberk S,et al. The World Health Organization Reporting System for Lung Cytopathology. Acta Cytol. 2023;67(1):80-91.
3、Cree IA. Editorial: The new WHO cytopathology reporting systems-extending the WHO classification of tumors. J Am Soc Cytopathol. 2023 Jul-Aug;12(4):239-242.
4、Nigam JS, Bharti JN, Rath A, et al. A Comprehensive Review of the Newest World Health Organization (WHO) Cytopathology Reporting Systems. Adv Anat Pathol. 2023 Jul 6.




 苏公网安备 32011402011742
苏公网安备 32011402011742