WHO胰胆管细胞学报告系统是在2015年巴氏细胞病理学会(Papanicolaou Society of Cytopathology,PSC)出版的胰胆管细胞学报告系统的基础之上进行了修订和更新,同时借鉴了第5版消化系统WHO肿瘤分类。其更新内容包括以下几点:(详见表1)。
1、从诊断类别来看,原PSC报告系统包括6个诊断类别,WHO报告系统包括7个诊断类别。
2、从诊断术语来看,总体变化不大,主要体现在将原PSC中的第IV类进行了重新分类和定义。具体为:
(1)原PSC系统中第IV类:肿瘤,可进一步分为:良性和其它。其中良性肿瘤,如浆液性囊腺瘤和淋巴管瘤,在WHO报告系统中属于2类(良性/未见恶性肿瘤细胞);
(2)原PSC系统中第IV类的其它肿瘤包括两大类:导管内病变和Pan-NET(胰腺神经内分泌肿瘤,pancreatic neuroendocrine tumors )、SPN(实性假乳头肿瘤,solid-pseudopapillary neoplasms)。其中,导管内病变可进一步分为
- 黏液性肿瘤:
MCN(黏液性囊性肿瘤,mucinous cystic neoplasm)
- 上皮内瘤变:
BilIN(胆管上皮内瘤变,biliary intraepithelial neoplasia)
- 导管内肿瘤:
ITPN(导管内管状乳头状肿瘤,intraductal tubulopapillary neoplasm)
在WHO报告系统中,IPMN、MCN、PanIN、BilIN被进一步分为低级别和高级别,其中低级别在WHO系统中被分类为第IV类,低风险/低级别肿瘤;而高级别IPMN、MCN、PanIN、BilIN和 IOPN、ITPN在WHO系统中属于第V类,高风险/高级别肿瘤,这一分类符合第5版消化系统WHO胰腺肿瘤的分类;
(3)原PSC系统中属于第IV类其它肿瘤中的Pan-NET和SPN在WHO胰胆管细胞学报告系统中属于第VII类,恶性肿瘤。
(4)WHO报告系统将IPN-B(胆管导管内乳头状肿瘤,intraductal papillary neoplasm of the bile duct)进一步分为低级别和高级别两组,分别属于WHO报告系统第IV类和第V类,但因其与支架、结石、炎症和高分化腺癌的胆管上皮的反应性和修复性变化之间细胞形态学重叠,目前尚缺乏明确的诊断标准。
表1:PSC&WHO胰胆管细胞学报告系统
| PSC系统 | WHO系统 | ||
| 诊断类别 | 诊断示例 | 诊断类别 | 诊断示例 |
| Ⅰ.无法诊断 |  无黏液性病变证据 无黏液性病变证据 良性胰腺实质,但影像学提示明确肿块 良性胰腺实质,但影像学提示明确肿块 胃肠道污染 胃肠道污染 |
Ⅰ.标本量不足/不充分/无法诊断 | 无变化 |
| Ⅱ.未见恶性肿瘤细胞 |  急性胰腺炎 急性胰腺炎 自身免疫性胰腺炎 自身免疫性胰腺炎 良性胰腺实质,但影像学上未发现明确肿块 良性胰腺实质,但影像学上未发现明确肿块 慢性胰腺炎 慢性胰腺炎 副脾 副脾 淋巴上皮囊肿 淋巴上皮囊肿 假性囊肿 假性囊肿 |
Ⅱ.良性/未见恶性肿瘤细胞 |  急性胰腺炎 急性胰腺炎 自身免疫性胰腺炎 自身免疫性胰腺炎 良性胰腺实质,但影像学上未发现明确肿块 良性胰腺实质,但影像学上未发现明确肿块 慢性胰腺炎 慢性胰腺炎 副脾 副脾 淋巴上皮囊肿 淋巴上皮囊肿 假性囊肿 假性囊肿 淋巴管瘤 淋巴管瘤 浆液性囊腺瘤 浆液性囊腺瘤 神经鞘瘤 神经鞘瘤 |
| Ⅲ.非典型细胞 | Ⅲ.非典型细胞 | 无变化 | |
| Ⅳ.肿瘤:良性 |  淋巴管瘤 淋巴管瘤 浆液性囊腺瘤 浆液性囊腺瘤 神经鞘瘤 神经鞘瘤 |
Ⅳ.低风险/低级别肿瘤 | 低级别IPMN、MCN、PanIN、BilIN IPN-B |
| Ⅳ.肿瘤:其它 |  IPMN、MCN、PanIN、BilIN、IOPN、ITPN (任何级别) IPMN、MCN、PanIN、BilIN、IOPN、ITPN (任何级别) Pan-NET、SPN Pan-NET、SPN |
Ⅴ.高风险/高级别肿瘤 |  高级别IPMN、MCN、PanIN、BilIN、IPN-B 高级别IPMN、MCN、PanIN、BilIN、IPN-B IOPN、ITPN IOPN、ITPN |
| Ⅴ.可疑恶性肿瘤 | Ⅵ.可疑恶性肿瘤 | 无变化 | |
| Ⅵ.恶性肿瘤 |  导管腺癌 导管腺癌 腺泡细胞癌 腺泡细胞癌 胆管癌 胆管癌 神经内分泌癌 神经内分泌癌 胰母细胞瘤 胰母细胞瘤 转移性 转移性 |
Ⅶ.恶性肿瘤 |  导管腺癌 导管腺癌 腺泡细胞癌 腺泡细胞癌 胆管癌 胆管癌 神经内分泌癌 神经内分泌癌 胰母细胞瘤 胰母细胞瘤 转移性 转移性 Pan-NET Pan-NET SPN SPN |
WHO胰胆管细胞学各类别诊断标准:
1、标本量不足/不充分/无法诊断:
定义:与WHO肺部细胞学一样,指因数量或质量不足而无法对目标病变进行可靠诊断的标本。
与PSC系统不同的是,这一类别在WHO系统中列出了3个诊断术语,但强调一个实验室仅使用一种诊断术语即可,以免给临床医生造成混淆。
出现这类诊断的原因有两方面:
(1)技术因素,包括操作者的经验、穿刺针的选择、是否进行术中快速现场评估(rapid on-site evaluation,ROSE)以及制片因素导致的目标细胞被血液、炎症细胞或其他物质遮盖;
(2)病变本身:如慢性和自身免疫性胰腺炎造成广泛纤维化;
在胰胆管细胞学中,并未明确规定上皮细胞数量,这主要是由于胰胆管细胞学的诊断不仅需观察细胞学形态,还应结合影像学及囊液生化结果综合分析。
比如:对于一个影像学提示为囊性病变的病例,即使玻片中仅见黏蛋白成分或囊液CEA水平升高,而无上皮成分,也不应使用标本量不足/不充分/无法诊断这一诊断术语。而对于镜下仅见良性细胞成分的病例,如果影像学提示明确肿块,则建议报告标本量不足/不充分/无法诊断,而如果影像学未提示明确肿块,则建议使用第II类,良性/未见恶性肿瘤细胞。
使用标本量不足/不充分/无法诊断这类诊断术语时需满足:
(1)无黏液性病变证据;
(2)无细胞非典型性;
(3)影像学提示明确肿块,仅见良性细胞成分,如胰腺实质、胃肠道污染;
注:对于影像学提示明确肿块,而镜下仅见良性胰腺腺泡和/或导管上皮细胞的病例,细胞病理学家的意见尚不一致。有些病理学家认为将其诊断为标本量不足/不充分/无法诊断,另一些病理学家将其归类为“良性”,并在报告中备注:该样本可能不具有代表性;
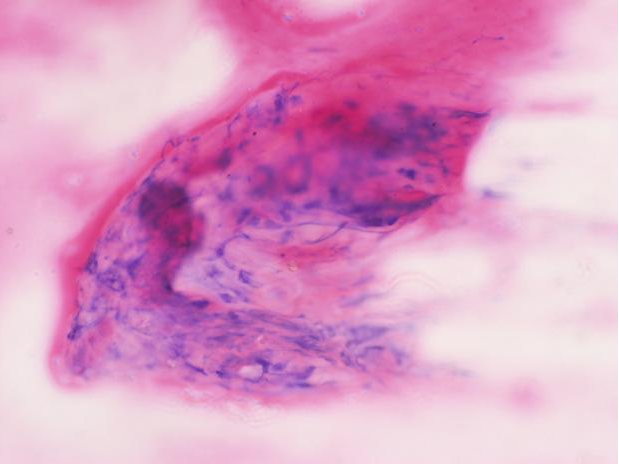
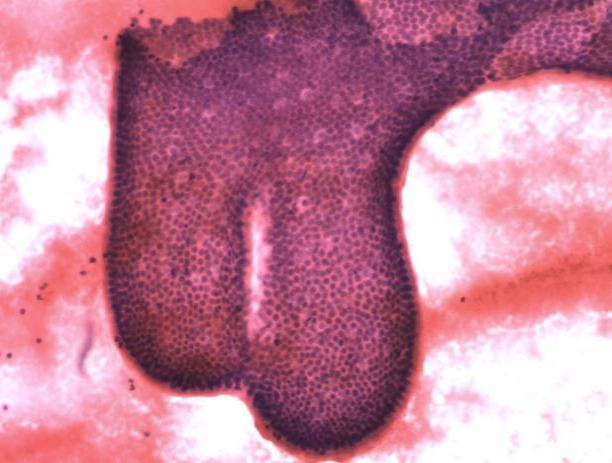
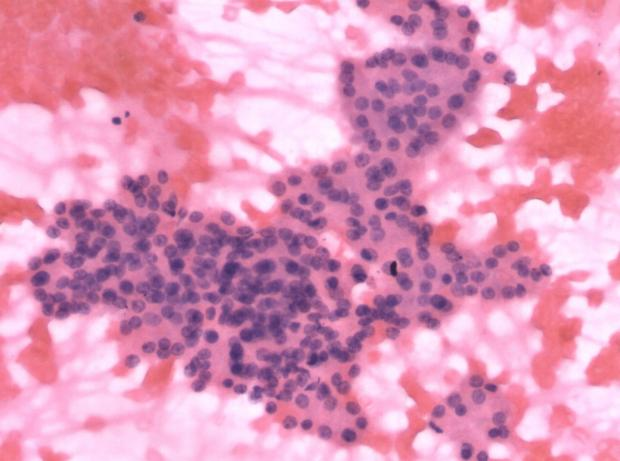
ⓑ标本量不足/不充分/无法诊断。胰腺EUS-FNA(HE染色×20):查见十二指肠上皮细胞。ⓒ胰腺EUS-FNA(HE×20):镜下仅见良性胰腺腺泡,但影像学提示占位,报告为标本量不足/不充分/无法诊断,也有学者认为,可诊断为“良性/未见恶性肿瘤细胞”;并在报告中注明:该样本可能不具有代表性。
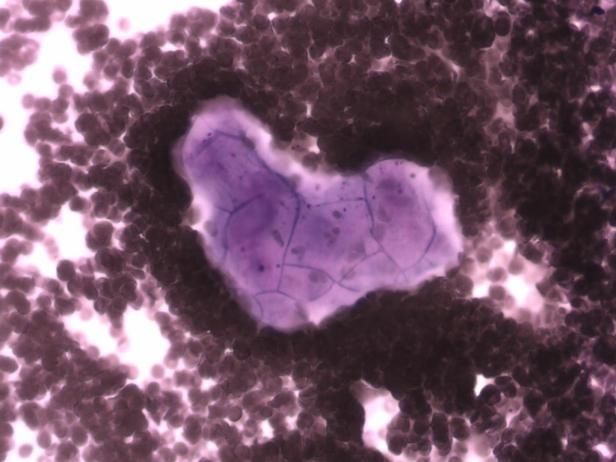
ⓓ胰腺EUS-FNA(MGG染色×40):虽然涂片中几乎无上皮细胞,但可见黏蛋白成分,结合影像学表现为囊性病变,囊液CEA水平升高,不应将此类病变归为无法诊断。
恶性风险及临床处理:
WHO胰胆管细胞学报告系统强调胰腺与胆管的恶性风险(risks of malignancy,ROM)不同,且胆管的ROM明显高于胰腺。标本量不足/不充分/无法诊断这类诊断术语在胰腺的ROM为5%-25%(见表2),而胆管刷检的ROM更高,可达28-69%。进一步处理依据诊断不足的原因并结合临床和影像学结果。如因病变纤维化而导致细胞量过少,可采用带凹槽针头以获取足够的组织来帮助明确诊断。而对于因涂片制片不佳而造成的无法诊断可重复使用液基的方法来协助诊断。
表2:WHO胰胆管细胞学报告系统各诊断类别恶性风险及临床处理
| 诊断类别 | 恶性风险 | 临床处理措施 |
| 标本量不足/不充分/无法诊断 | 胰腺:5%-25% | 重复FNAB |
| 胆管:28-69% | 重复ERCP胆管镜、刷检和活检 | |
| 良性/未见恶性肿瘤细胞 | 胰腺:0-15% | 结合临床其它检查 |
| 胆管:26-55% | ||
| 非典型细胞 | 胰腺:30-40% | 重复FNAB,MDT讨论,ROSE及辅助检测 |
| 胆管:25-77% | 重复ERCP胆管镜、刷检和活检,结合FISH或NGS等辅助检测。 | |
| 低风险/低级别肿瘤 | 胰腺:5-20% | 结合临床其它检查 |
| 胆管:NA* | NA | |
| 高风险/高级别肿瘤 | 胰腺:60-95% | 适合手术的患者进行手术,不适合手术的可保守治疗。 |
| 胆管:NA | NA | |
| 可疑恶性肿瘤 | 胰腺:80-100% | 结合临床、影像及其它辅助检测,如果支持恶性,则手术; 如需术前治疗,则重复检查。 |
| 胆管:74-100% | ||
| 恶性肿瘤 | 胰腺:99-100% | 根据具体类型及分期 |
| 胆管:96-100% |
2、良性/未见恶性肿瘤细胞:
定义:有明确的良性细胞病理特征,可能、也可能不能诊断为特定病变或良性肿瘤。
包括:
(1)非肿瘤性病变:
Ø 急性胰腺炎
Ø 慢性胰腺炎
Ø 自身免疫性胰腺炎
Ø 胆管炎
Ø 副脾
Ø 假性囊肿
Ø 淋巴上皮囊肿
(2)肿瘤性病变:
Ø 浆液性囊腺瘤
Ø 淋巴管瘤
Ø 神经鞘瘤
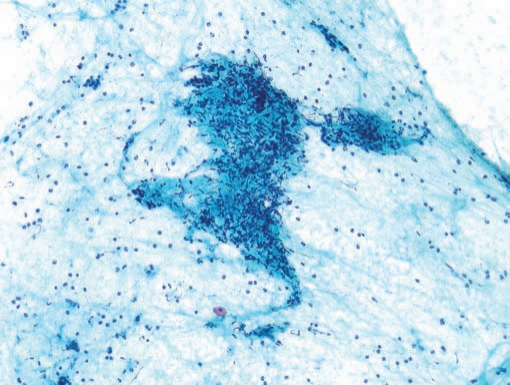
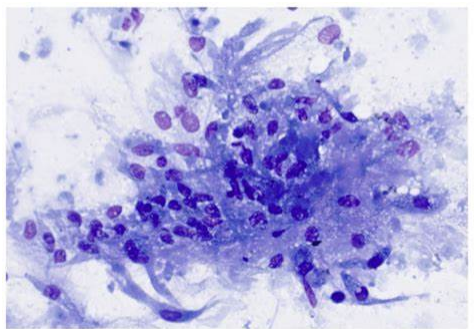
ⓑ:胰腺结核。胰腺EUS-FNA(Diff-Quik染色×20):小灶上皮样细胞,提示慢性肉芽肿性炎。
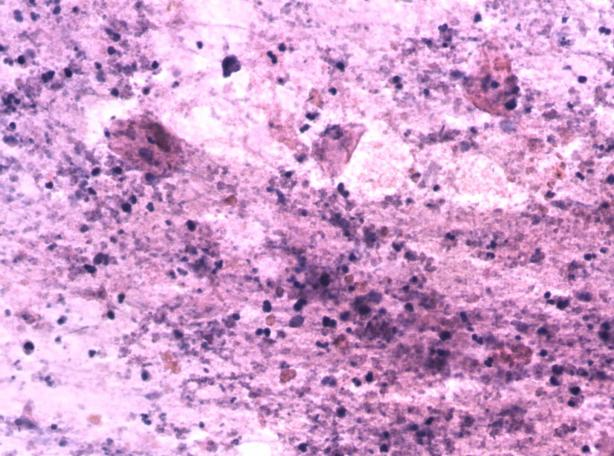
ⓒ:胰腺假性囊肿。胰腺EUS-FNA(HE染色×40):查见坏死的细胞碎屑及淋巴细胞。
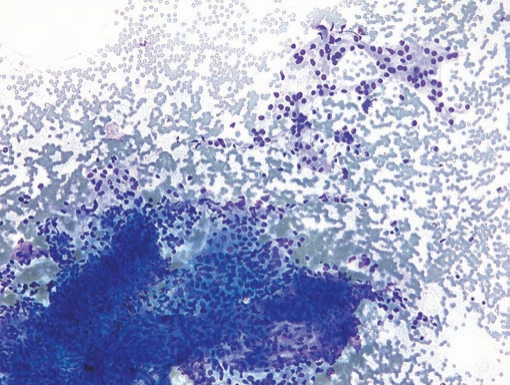
ⓓ:浆液性囊腺瘤。胰腺EUS-FNA(Diff -Quik染色×10):干净的背景下可见小而一致的细胞。
恶性风险及临床处理:
良性胰腺 FNAB的ROM范围为0-15%,而“良性”胆管刷检的ROM高达 55%。进一步处理与临床病因相关,对于胰腺假性囊肿可选择引流囊液,急、慢性胰腺炎的患者主要需查清潜在病因及改善营养,而皮质类固醇激素常被用于自身免疫性胰腺炎。
3、非典型细胞:
定义:主要表现为良性病变和轻微的恶性病变可能性特征,在数量或质量上不足以诊断为良性、低风险、高风险肿瘤和恶性病变。
主要原因:
(1)技术因素,如:操作者的经验、是否ROSE协助、制片原因导致的目标细胞被遮盖或退变;
(2)病变本身因素,如非典型性不明显或病变部位较深,无法获得满意的标本时;
(3)细胞数量少;
(4)病理学家的经验;
恶性风险及临床处理:
胰腺 FNAB非典型类别的ROM为 30-40%,而胆管刷检非典型类别的ROM约25-77%。对于这一类别的处理包括:多学科讨论、重复检查、使用ROSE协助诊断以及进行FISH或NGS等基因检测协助诊断。文献报道在胆管刷检中使用上清液进行分子检测,其敏感性可提高到93%。
4、胰胆管肿瘤:低风险/低级别(PaN-Low):
定义:导管内和/或囊性肿瘤伴上皮低级别异型增生(原轻-中度异型增生)。
包括:
(1) 低级别IPMN:起源于主胰管或其分支,故与主胰管相通,多见于胰头部。其特点是导管扩张,粘液柱状上皮呈导管内增生,伴或不伴导管内乳头;细胞轻-中度异型,通常表现为胃和/或肠型上皮。主要鉴别诊断:胃肠道污染。
(2) 低级别MCN:与胰管不相通,多见于胰体尾。镜下与低级别IPMN相似,且具有独特的上皮下卵巢样间质。
(3) 低级别PinIN/BilIN:
(4) 低级别IPN-B:可分为两种类型,一种类似于胰腺IPMN,主要发生在肝内导管,另一种不同于胰腺IPMN,发生在肝外导管。目前尚缺乏明确的诊断标准。
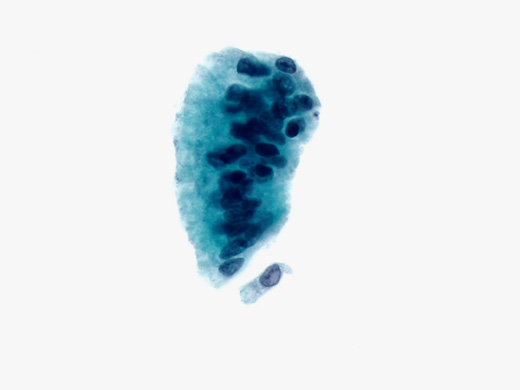
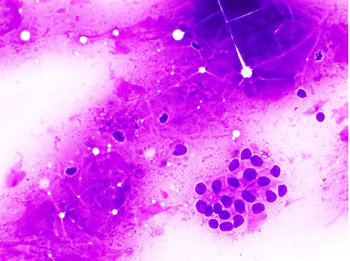
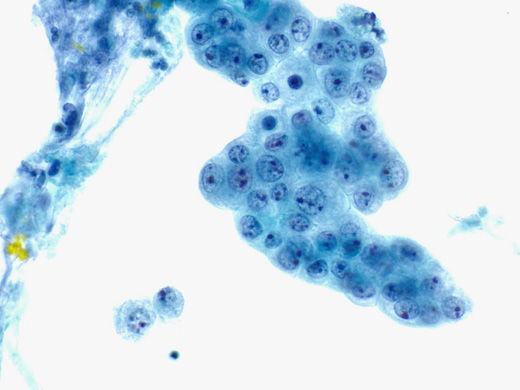
图4:ⓐ:低级别IPMN。胰腺EUS-FNA(巴氏染色×60):一团黏液柱状上皮核拉长、深染,核膜轻度不规则。
ⓑ:低级别IPMN。胰腺EUS-FNA(Diff-Quik染色×40):背景中可见厚重的黏蛋白,右下角见一团细胞呈低级别异型增生。
这一类诊断相对困难,需结合影像学及囊液生化检测,同时分子检测也助于其诊断。以下几点将有助于提高此类诊断:
(1)背景中的黏蛋白提示IPMN和MCN的诊断;
(2)囊液CEA检测有助于IPMN和MCN的诊断,当囊液CEA>192ng/mL时提示肿瘤性;
(3)尽量获取足够多的囊壁组织以观察卵巢样间质,可帮助诊断MCN;
(4)GNAS和KRAS突变有助于IPMN的诊断,KRAS突变仅在少部分MCN中检测到,且低级别IPMN和MCN不存在其他如TP53和SMAD4突变。
恶性风险及临床处理:
胰腺 FNAB低风险肿瘤的ROM为 5-20%,对于这类病变的患者可根据临床和影像学特征选择定期随访监测。而由于缺乏胆管癌前病变的细胞学标准,故目前尚无胆管低风险肿瘤的相关ROM数据及临床处理建议。
5、胰胆管肿瘤:高风险/高级别(PaN-High):
定义:导管内和/或囊性肿瘤伴上皮高级别异型增生。
包括:
(1)高级别IPMN/MUN
(2)高级别PinIN/BilIN
(3)IOPN、ITPN
(4)高级别IPN-B
PaN-High的关键细胞病理学特征:细胞较小(<十二指肠上皮细胞),核浆比高,核形不规则,染色质异常(低或深染),核仁显著,胞浆内可见黏液,伴/不伴坏死或炎症。
此类病变应与可疑恶性和恶性鉴别,其鉴别要点包括以下两点:
(1)PaN-High影像学往往提示为囊性或导管内病变;
(2)PaN-High为导管或胆管起源,不包括:Pan-NET、SPN、腺泡细胞癌、胰母细胞瘤等肿瘤。
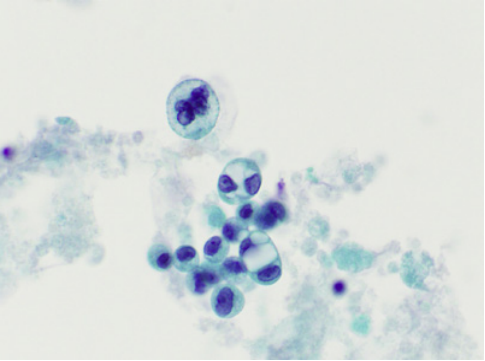
图5:高级别IPMN。胰腺EUS-FNA(巴氏染色×60):细胞体积较小(<十二指肠细胞),核质比高,胞浆内可见黏液,核膜不规则,背景可见坏死。
恶性风险及临床处理:
胰腺 FNAB高风险肿瘤的ROM为 60-95%,对于这类病变的患者最佳的处理方式是手术,但当手术风险较高,特别是影像学的恶性风险较低时应可选择保守治疗。而由于缺乏胆管癌前病变的细胞学标准,故目前也无胆管高风险肿瘤的相关ROM数据及临床处理建议。
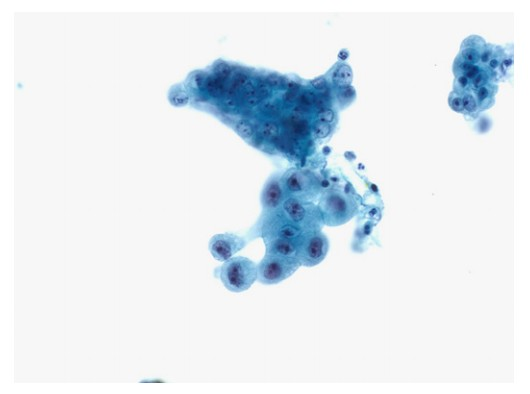
6、可疑恶性肿瘤。
定义:显示一些细胞病理特征提示恶性肿瘤,但在数量或质量上不足以作出明确的恶性诊断。
导致这类诊断的原因较多,如之前提到的:临床及病理医生的经验、制片因素、细胞量少,有细胞学形态学谱系,除此之外,还包括合并胰腺炎、支架置入、结石、无法进行辅助检测等。
恶性风险及临床处理:
胰腺 FNAB可疑恶性肿瘤的ROM为 80-100%,而胆管刷检可疑恶性肿瘤的ROM约74-100%。对于这一类别的处理可重复取样或进行辅助检测,如果证实是恶性,则直接治疗。也可结合临床及影像学,若都支持恶性肿瘤,则可直接进行手术。
7、恶性肿瘤。
定义:具有显示明确的恶性肿瘤的细胞病理学特征。
这类肿瘤包括原发性和继发性。其中以原发性多见,而胰腺导管腺癌(PDAC)和胆管癌占原发性恶性肿瘤的绝大多数。此类别相较于原PSC系统即将Pan-NET、SPN纳入到这一类别。这与WHO 第 5 版中的胰腺肿瘤分类相一致。胰腺常见肿瘤细胞病理特征及鉴别诊断见表3:
表3:胰腺常见肿瘤细胞病理学特征及鉴别诊断
| 诊断 | 关键细胞学特征 | 免疫组化 |
| 导管腺癌 | -高分化:背景干净; 有黏附性; 核膜轻度不规则; 染色质浅; 核大小不一轻微; -低分化:背景脏、坏死; 黏附性差; 核膜卷曲; 染色质深; 核大小不一显著; |
CK7 |
| 神经内分泌肿瘤 | -细胞排列松散或单个散在; -核偏位,呈浆细胞样; -血管丰富 -核呈圆形/椭圆形 -染色质呈椒盐样或胡椒粉样 |
SYN、CgA、 INSM1 |
| 腺泡细胞癌 | -葡萄簇状或单个散在 -丰富的颗粒状胞质 -核呈圆形,核仁明显 |
BCL10、胰/糜蛋白酶 |
| 实性假乳头状肿瘤 | -涂片中见大量含纤维血管的细胞碎片,也可见单个散在细胞 -毛细血管周围可见黏液样间质 -胞质泡沫状或透明 -核呈椭圆形,可见核沟,无明显核仁 |
CD10、β-catenin CyclinD1、CD99(斑点状) |
| 胰母细胞瘤 | -小的未分化细胞 -可见特征性的鳞状小体 -异源性成分 |
BCL 10,胰/糜蛋白酶 鳞状小体中β-catenin核阳性 |
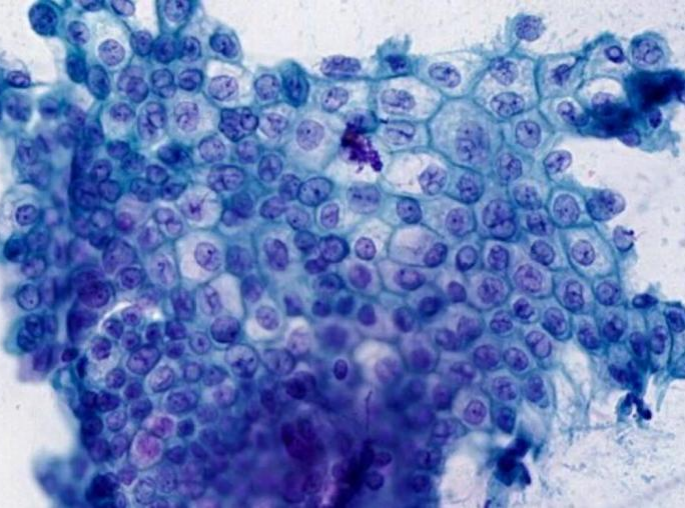
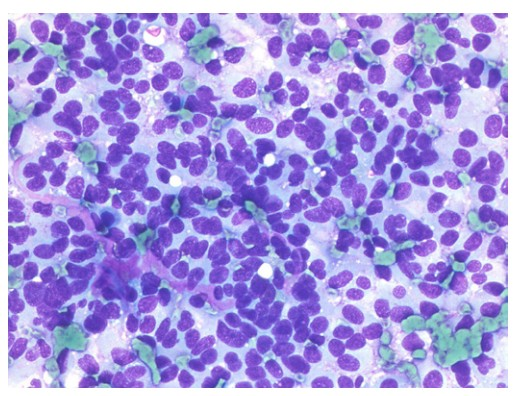
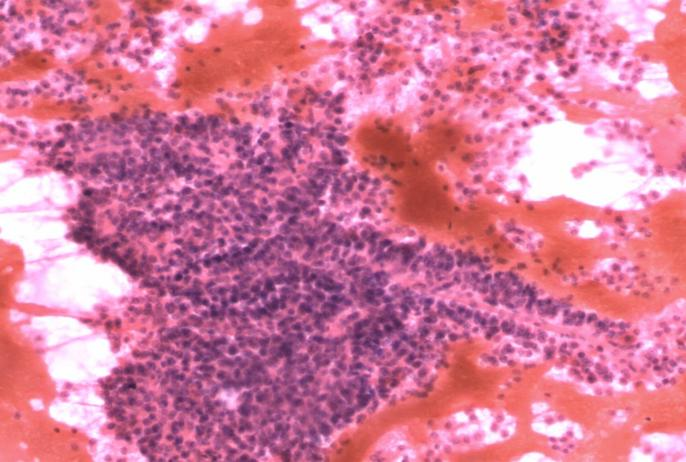
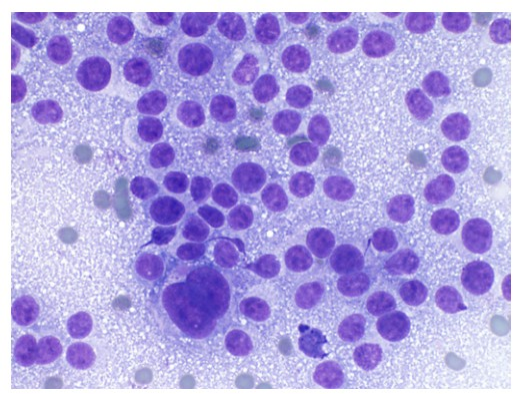
图7:ⓐ:胰腺导管腺癌,高分化。胰腺EUS-FNA(巴氏染色×60):镜下肿瘤细胞间间距不等(如喝醉的蜂巢),核大小不一(>1:4),染色质粗、核仁明显。
ⓑ:胰腺神经内分泌肿瘤。胰腺EUS-FNA(Diff-Quik染色×40):肿瘤细胞均匀分布,其间可见小血管,细胞核圆至椭圆形,核色质细腻。
ⓒ:胰腺实性假乳头状肿瘤。胰腺EUS-FNA(HE染色×40):肿瘤细胞单个散在分布或围绕血管生长。细胞大小较一致。
ⓓ:胰腺腺泡细胞癌。胰腺EUS-FNA(Diff -Quik染色×60):肿瘤细胞呈小腺泡样或单个散在,核呈圆形,胞浆呈颗粒状。
恶性风险及临床处理:
胰腺 FNAB可疑恶性肿瘤的ROM为 97-100%,而胆管刷检可疑恶性肿瘤的ROM约96-100%。手术治疗是胰胆管恶性肿瘤的一线治疗方法。而对于小于2cm、 Ki-67< 3%的Pan-NET可不进行手术,选择临床监测。对于局部晚期的PDAC患者可先进行新辅助治疗,然后再切除,对于不可切除的患者通常采用化疗和放疗联合治疗。
总结:
WHO胰胆管细胞学报告系统与其它细胞病理学报告系统一样,旨在改善临床医生和细胞病理学家之间的沟通,具有以下特点:
(1)每个诊断类别对应不同的ROM以及诊断管理建议,为临床提供更精确的指导意见;
(2)每个标准化术语建立细胞病理学的关键诊断标准,增加诊断者之间的一致性;
(3)主张将影像学、生化检查及分子病理纳入最终诊断,如胰腺囊肿液的生化(CEA和淀粉酶)和分子检测结果;
(4)同一诊断类别胆管比胰腺的恶性风险高;
(5)提供取样和制片方式的最佳建议,以促进细胞病理学样本的处理和制备;
(6)通过IARC网站将细胞病理学链接到第五版WHO分类蓝皮书,为细胞病理学和组织病理学建立一个动态联系。
参考文献:
1、Pitman MB, Centeno BA, Reid MD, et al. The World Health Organization Reporting System for Pancreaticobiliary Cytopathology. Acta Cytol. 2023;67(3):304-320.
2、Hoda RS, Arpin RN 3rd, Rosenbaum MW, et al. Risk of malignancy associated with diagnostic categories of the proposed World Health Organization International System for Reporting Pancreaticobiliary Cytopathology. Cancer Cytopathol. 2022 Mar;130(3):195-201.
3、Gocun PU, Simsek B, Ekinci O, et al. Risk of Malignancy Using the Diagnostic Categories Proposed by the World Health Organization International System for Reporting Pancreaticobiliary Cytopathology. Acta Cytol. 2022;66(6):475-485.
4、Cree IA. Editorial: The new WHO cytopathology reporting systems-extending the WHO classification of tumors. J Am Soc Cytopathol. 2023 Jul-Aug;12(4):239-242.
5、Field AS, Pitman M, Cree IA, Canberk S, Bubendorf L, Mahrotra R, Schmitt F. The rationale for the development and publication of the World Health Organization reporting systems for cytopathology and a brief overview of the first editions of the lung and pancreaticobiliary systems. Cancer Cytopathol. 2023 Sep 13.
6、Ali SZ,Erozan YS, Hruban RH.Atlas of Pancreatic Cytopathology.2009.
7、Hoilat GJ, Abdu M, Hoilat J, et al. A Rare Case of Pancreatic Tuberculosis Diagnosed via Endoscopic Ultrasound-Guided Fine Needle Aspiration and Polymerase Chain Reaction. Cureus. 2020 Jun 24;12(6):e8795.




 苏公网安备 32011402011742
苏公网安备 32011402011742