性别:女
年龄:47岁
临床表现:患者3周前无明显诱因感尿频、尿急、尿不尽,自行购买“左氧氟沙星、金刚藤、三金片”口服,症状无明显缓解,1周前下腹坠痛,呈阵发性,遂至医院就诊。
专科检查:外阴经产型,子宫及双侧附件触诊不满意,盆腔内可触及一大小14.0cmx10.0cm的包块,活动度尚可。辅助检查:超声示:子宫右后方可见13.9cmx10.5cmx9.8cm的囊实性肿块,考虑囊腺瘤。CT示:子宫右后方巨大囊实性肿块影,大小约11.9cmx11.6cmx10.8cm,以囊性为主,增强扫描可见强化,囊腺瘤及囊腺癌待鉴别。
大体所见:右侧卵巢包块,囊壁组织一块,大小10.8cmx5.5cmx2.5cm,囊壁厚0.3-1.2cm,局部囊内壁可见乳头状肿物,肿物大小2.8cmx1.8cmx1.5cm,切面灰白色,实性。
镜下形态:肿瘤呈腺管状、乳头状和大小不一的囊状结构,乳头为纤细的乳头,无复杂分枝,囊内可见蓝染的黏液样物,部分大囊内可见微乳头结构。肿瘤细胞呈鞋钉状、多角形、立方形、柱状、胞质嗜酸性。细胞核圆形、卵圆形,具有异型性明显,核分裂可见(<5个/10HPF)。
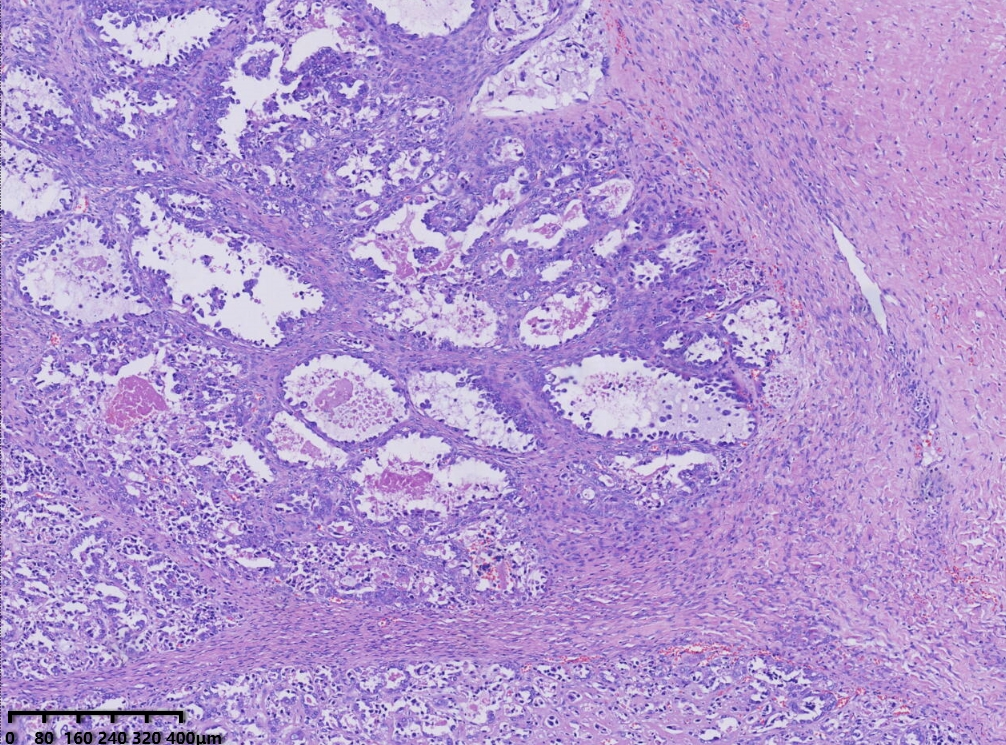
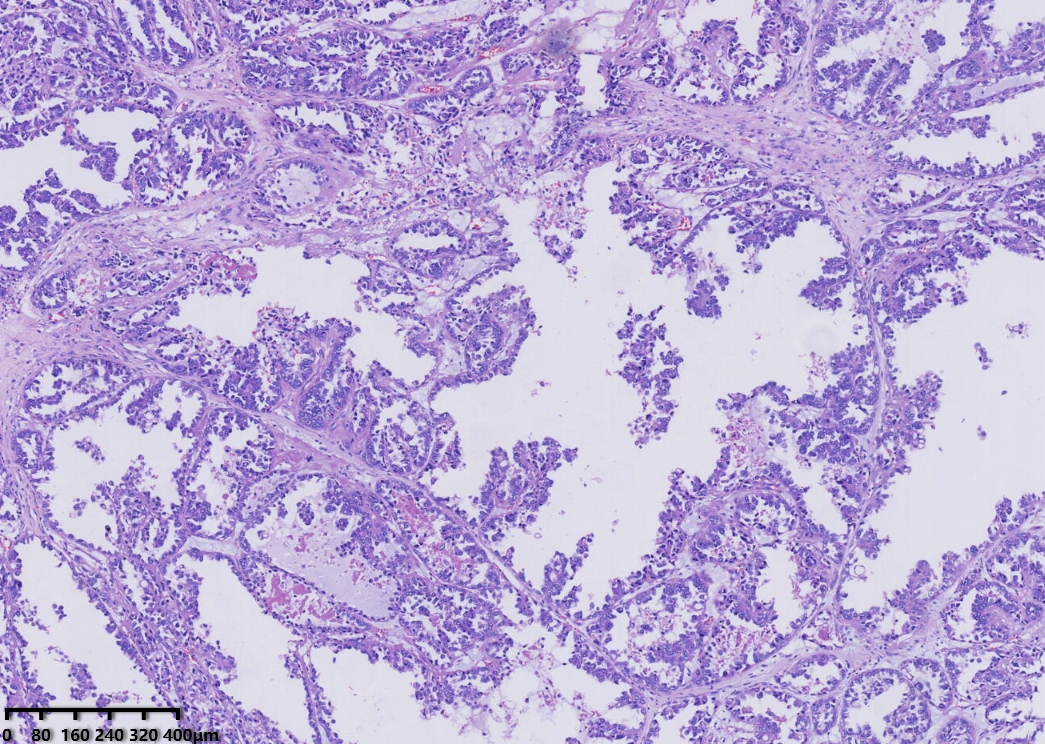
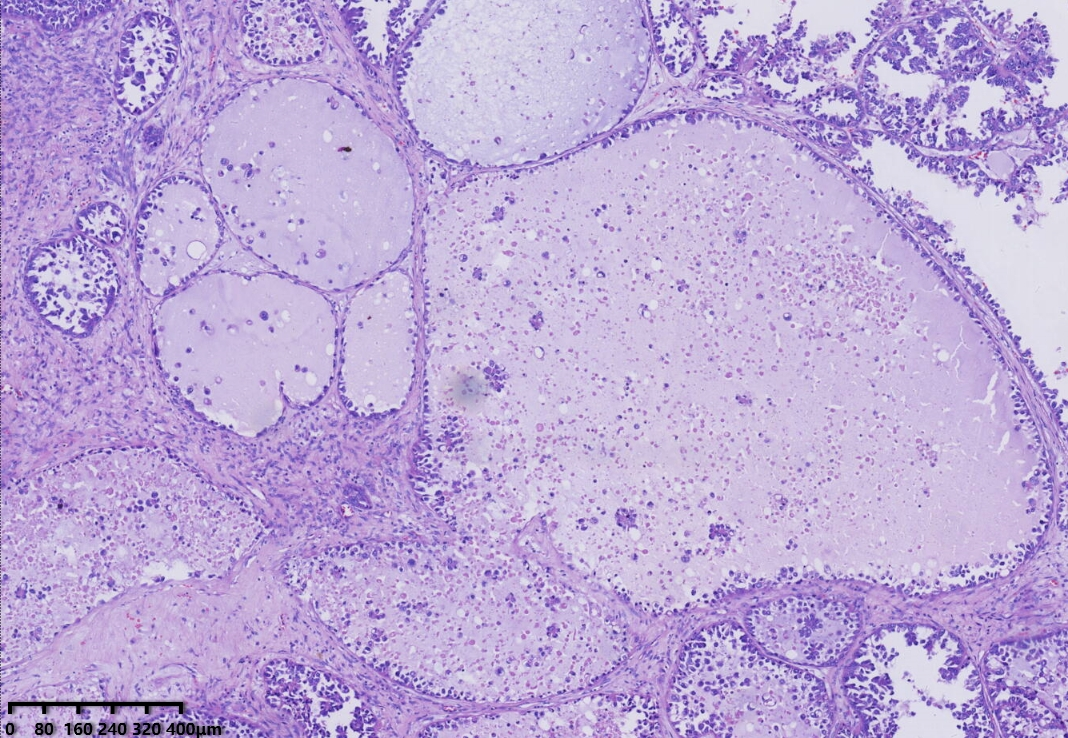
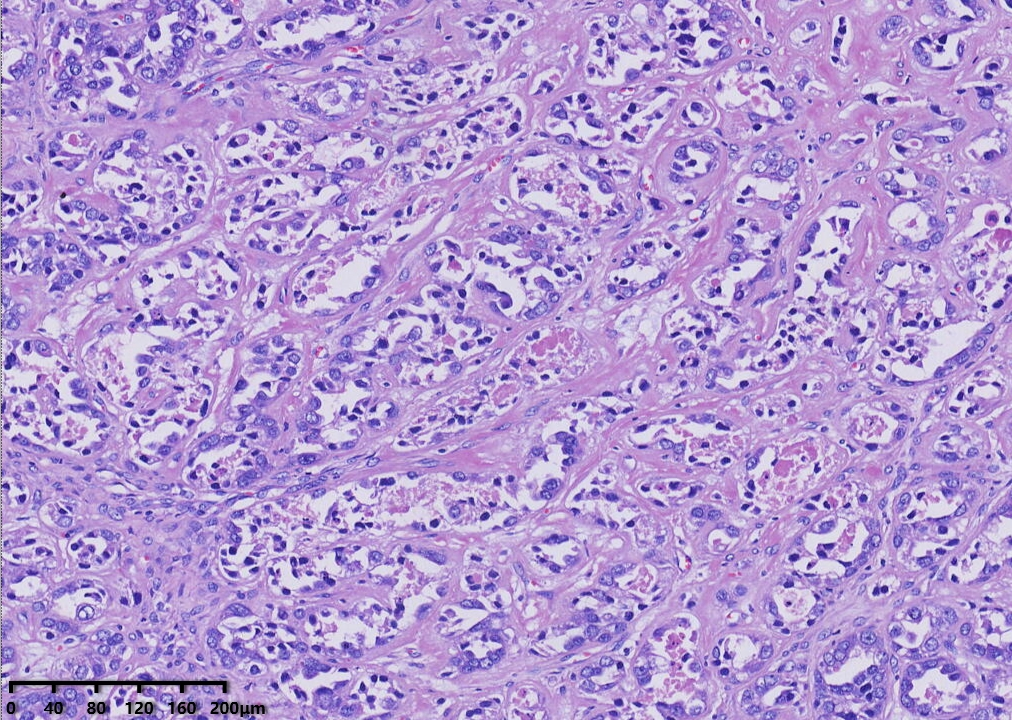
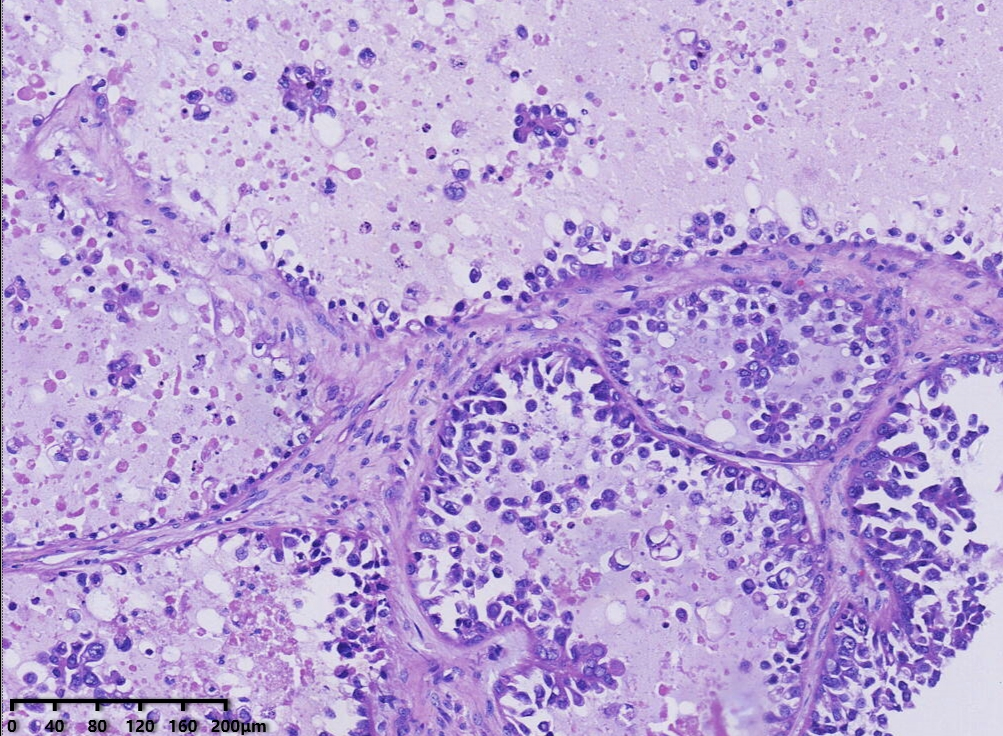
低倍镜,腺管大小相对一致,囊状结构为大小不一的囊,其内可见淡蓝色黏液样物及微乳头结构。
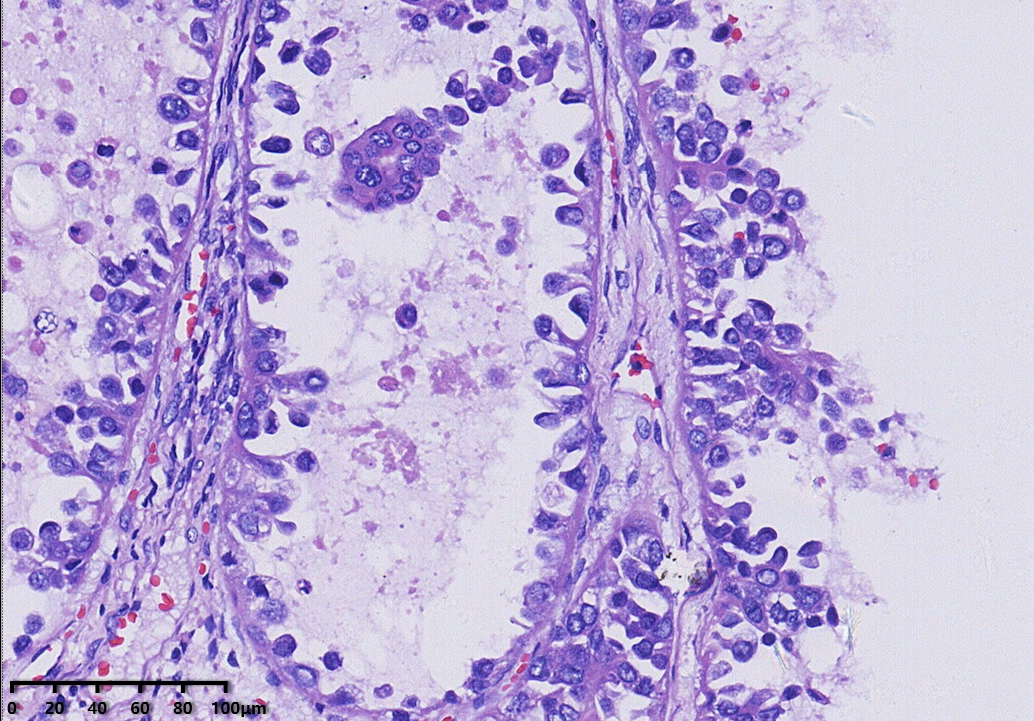
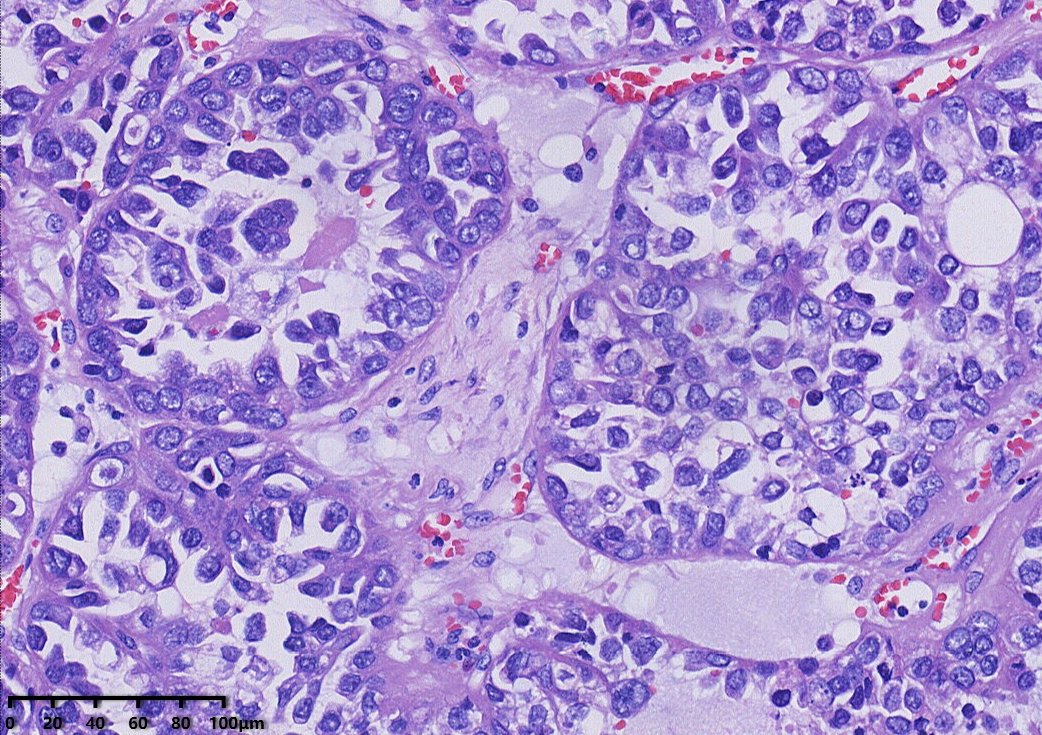
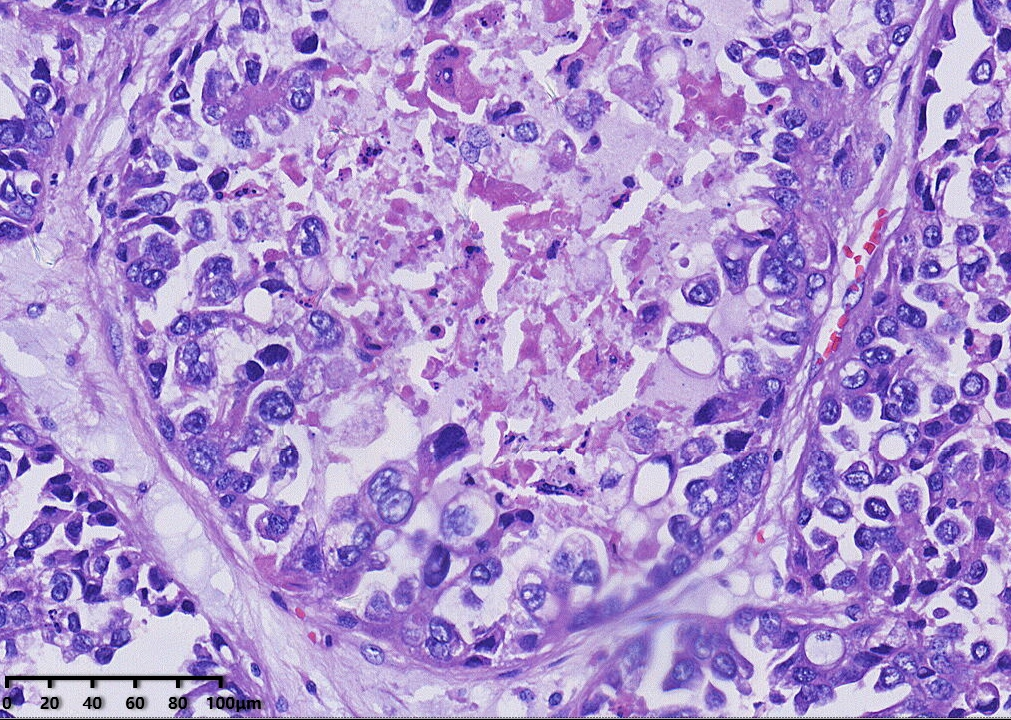
免疫组化结果:CK7(+),PAX-8(+),NapsinA(+),HNF1-β(+),P504S(+),P16部分(+),CA-125部分(+),P53野生型表达,ER(-),PR(-),WT-1(-),CK20(-),CD10(-),Ki67阳性率约15%。
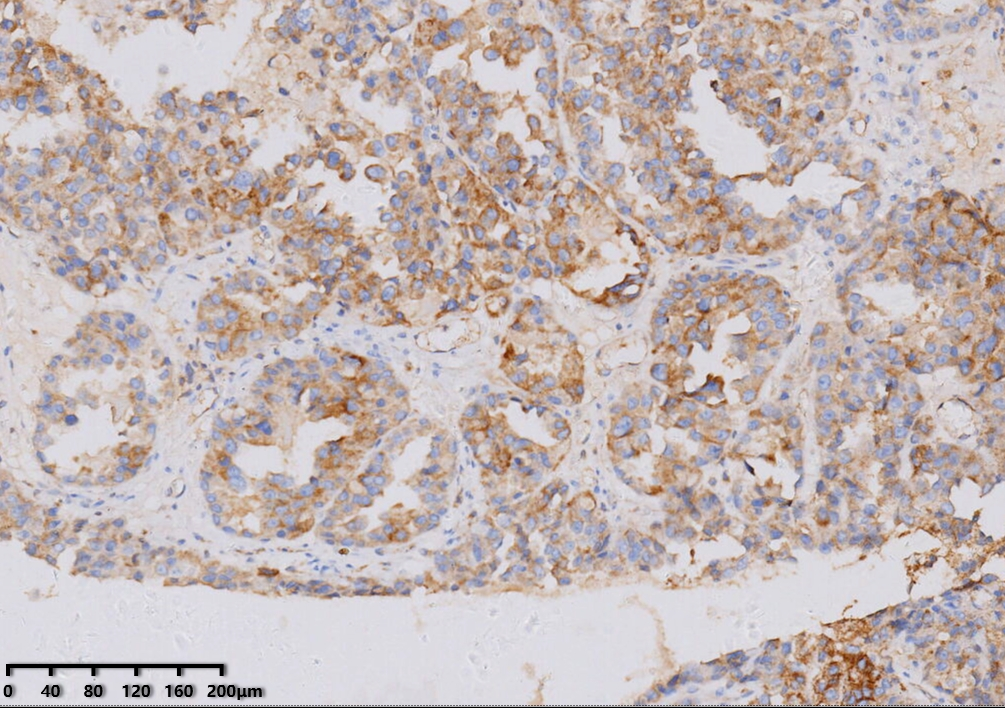
NapsinA(+)
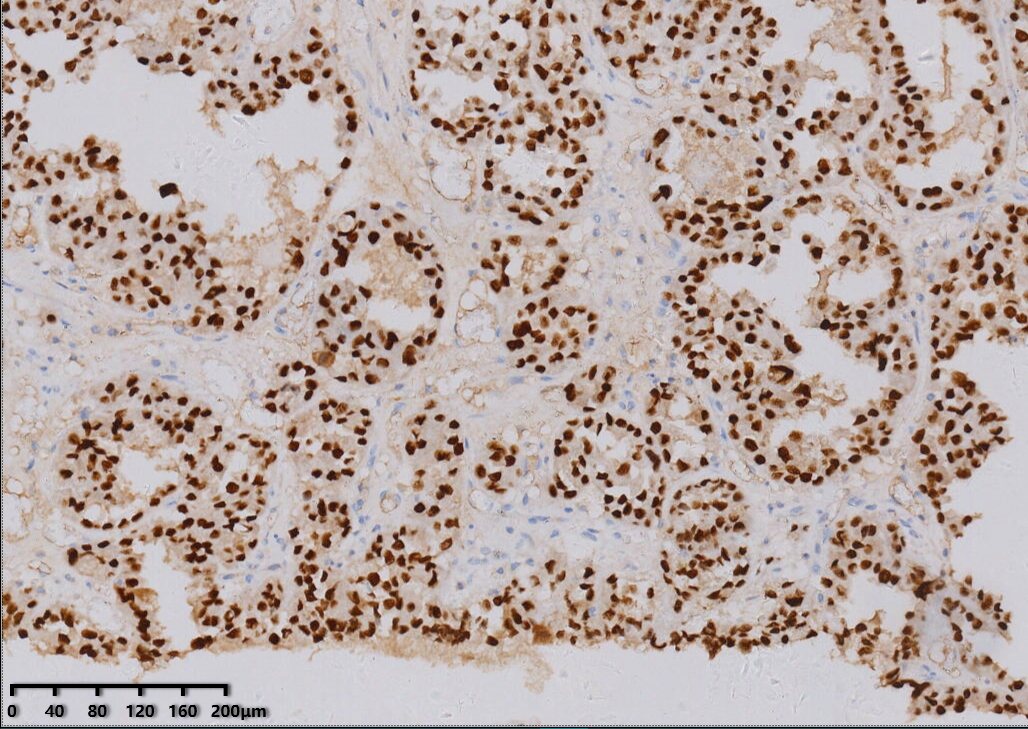
HNF1-β(+)
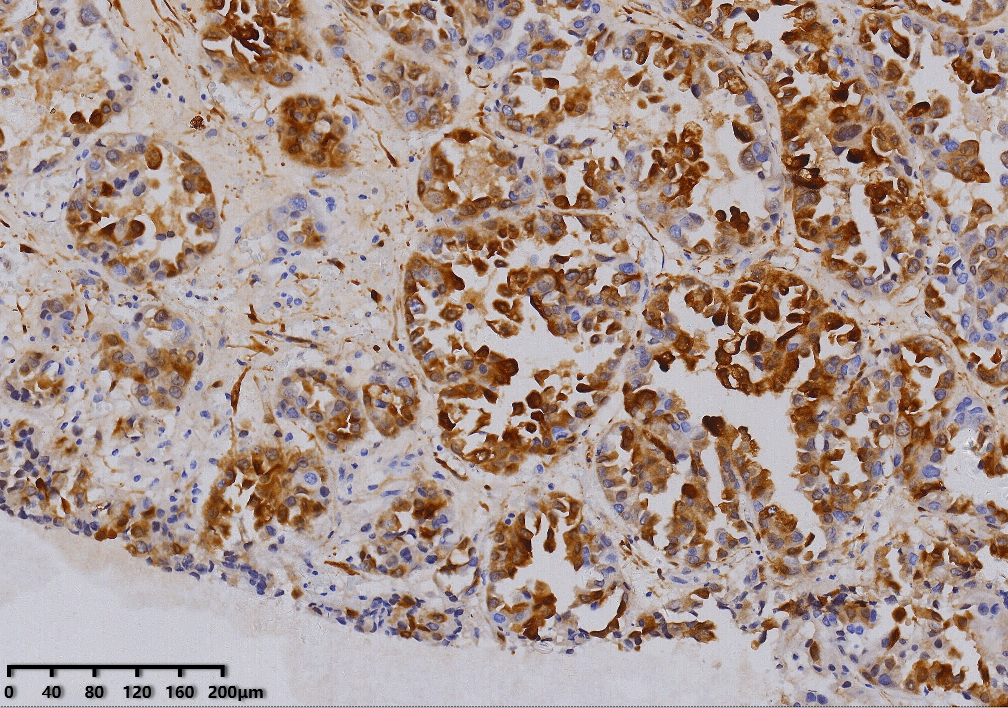
P16(+)
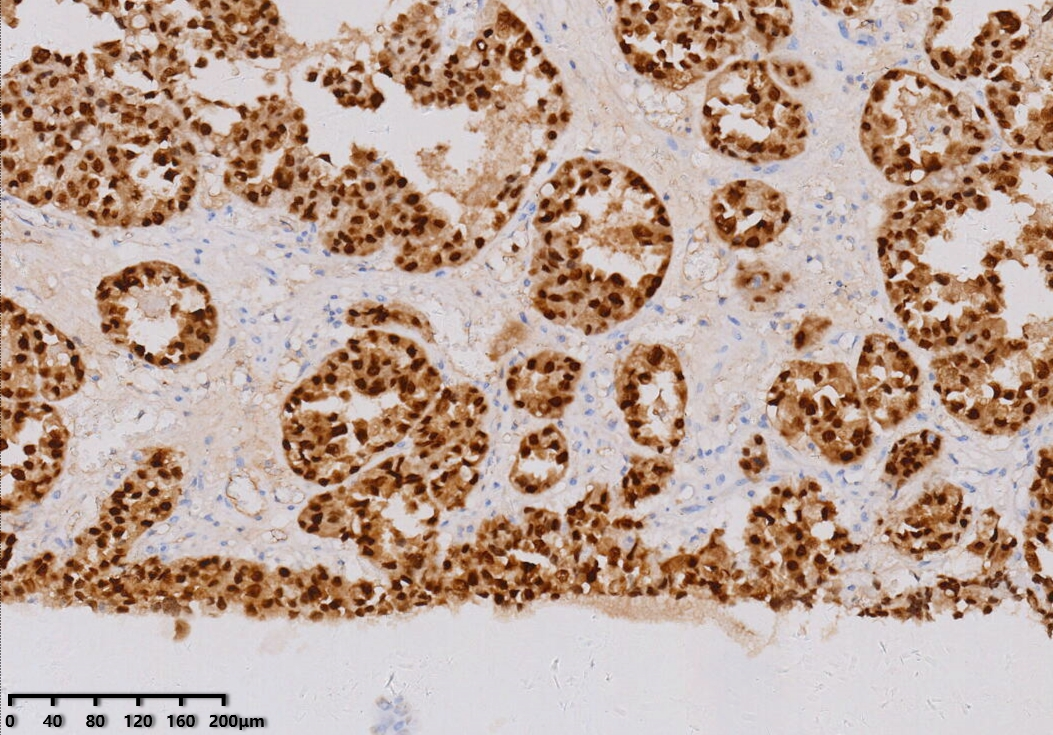
PAX8(+)
病理诊断:卵巢透明细胞癌病例2
性别:女
年龄:49岁
临床表现:患者20天前无明显诱因出现腹胀不适,口服消化药后症状稍微缓解,10天前出现双下肢水肿,遂入院治疗。
辅助检查:CT示:腹部盆腔内可见大小约14.5cmx14.0cmx12.8cm的囊实性混杂密度影,边界尚清,密度不均匀,增强扫描,实性结构可见强化,囊性结构未见强化。
大体所见:右侧卵巢包块,灰白色肿块一个,大小16.8cmx15.5cmx9.5cm,切面灰白色,囊实性。
镜下形态:肿瘤呈腺管状、乳头状结构为主,部分管腔内可见淡粉染无定型物质。肿瘤细胞呈鞋钉状、多角形、立方形、柱状、以胞质淡染,空亮的透明细胞为主。细胞核圆形、卵圆形,异型性明显,核分裂可见(<5个/10HPF)。未见明显坏死。
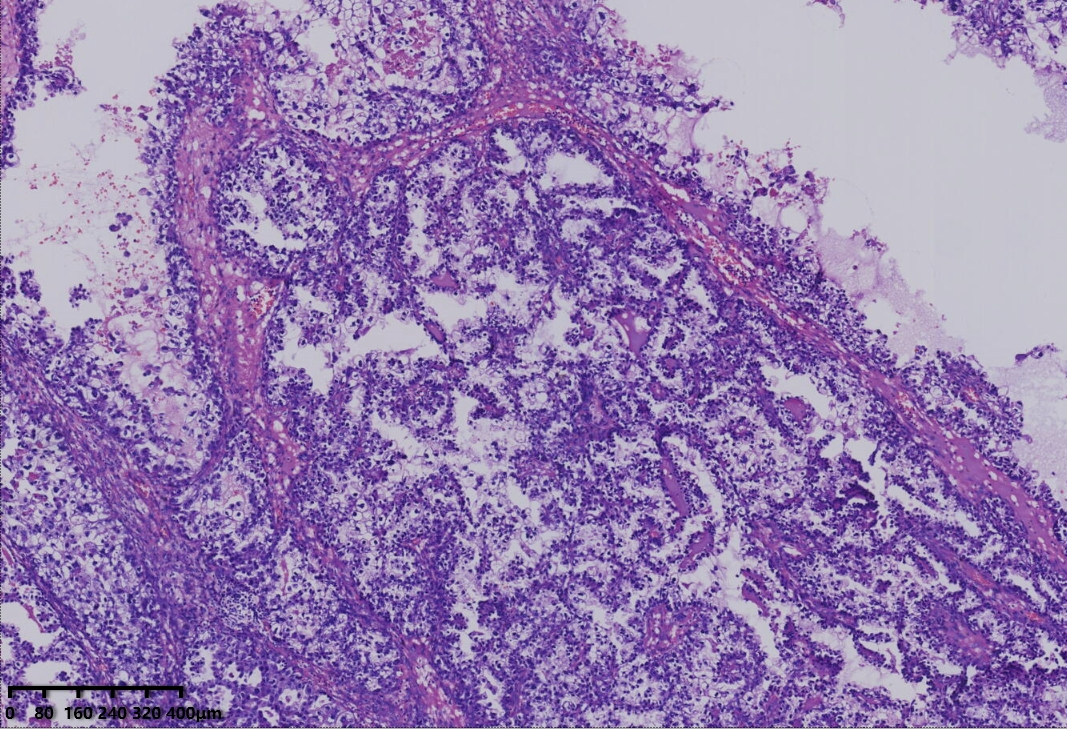
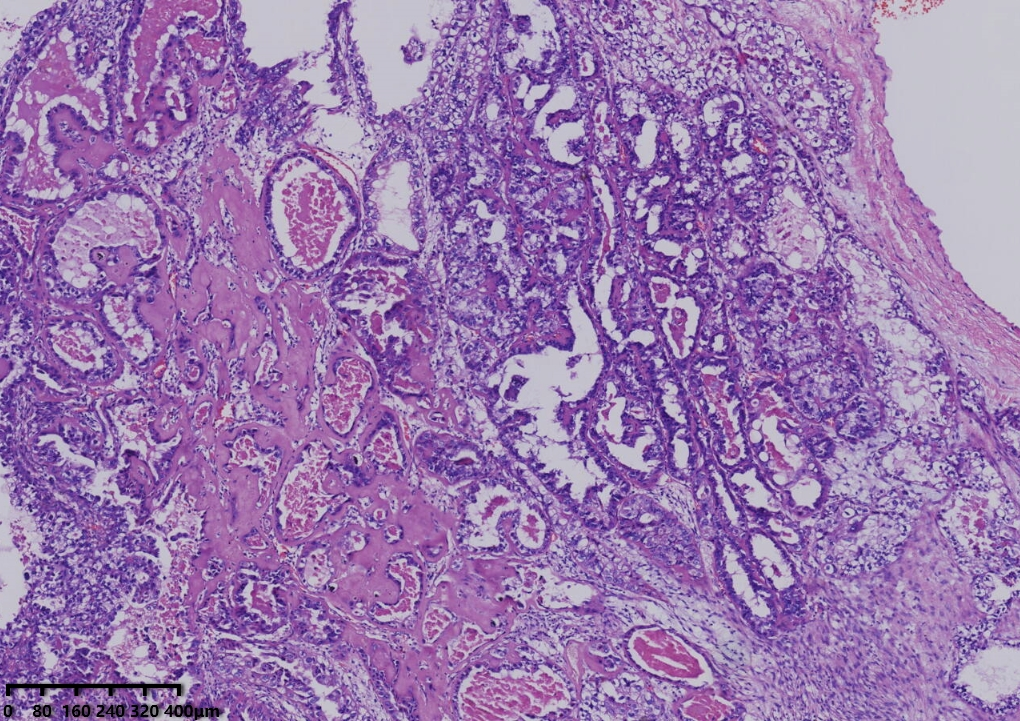
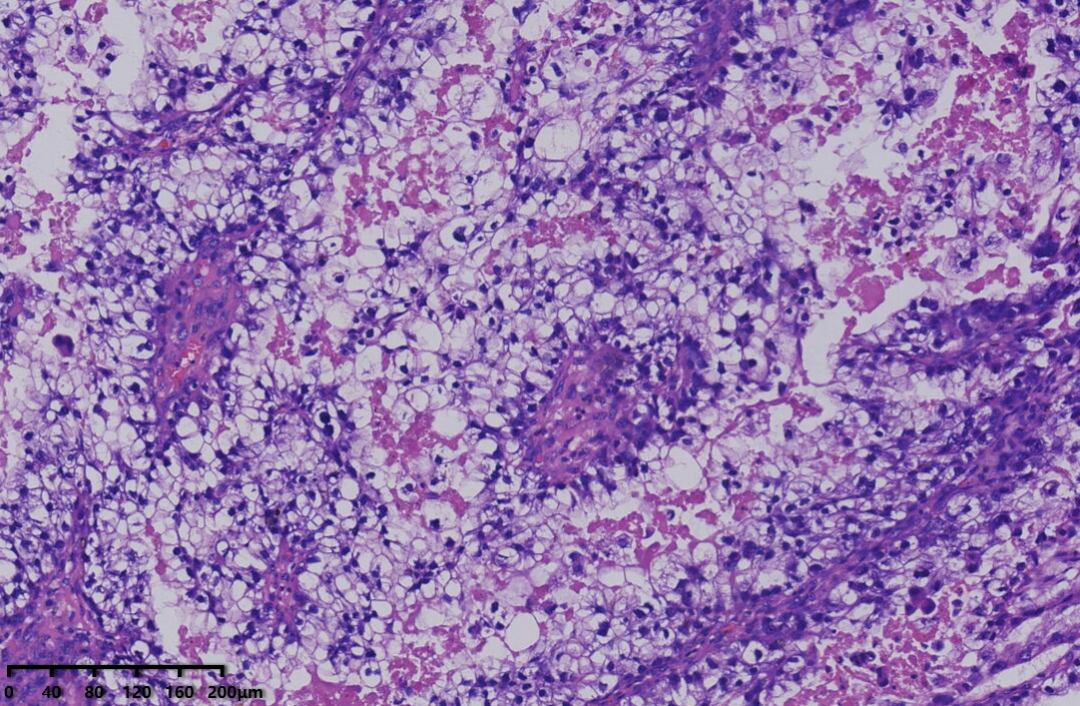
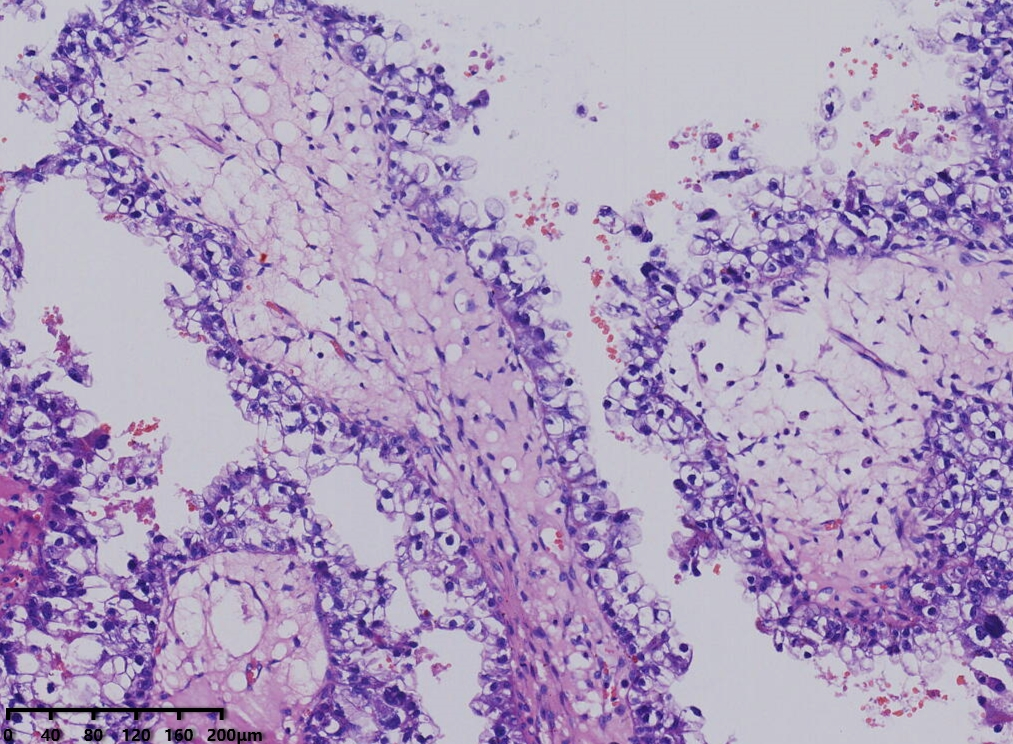
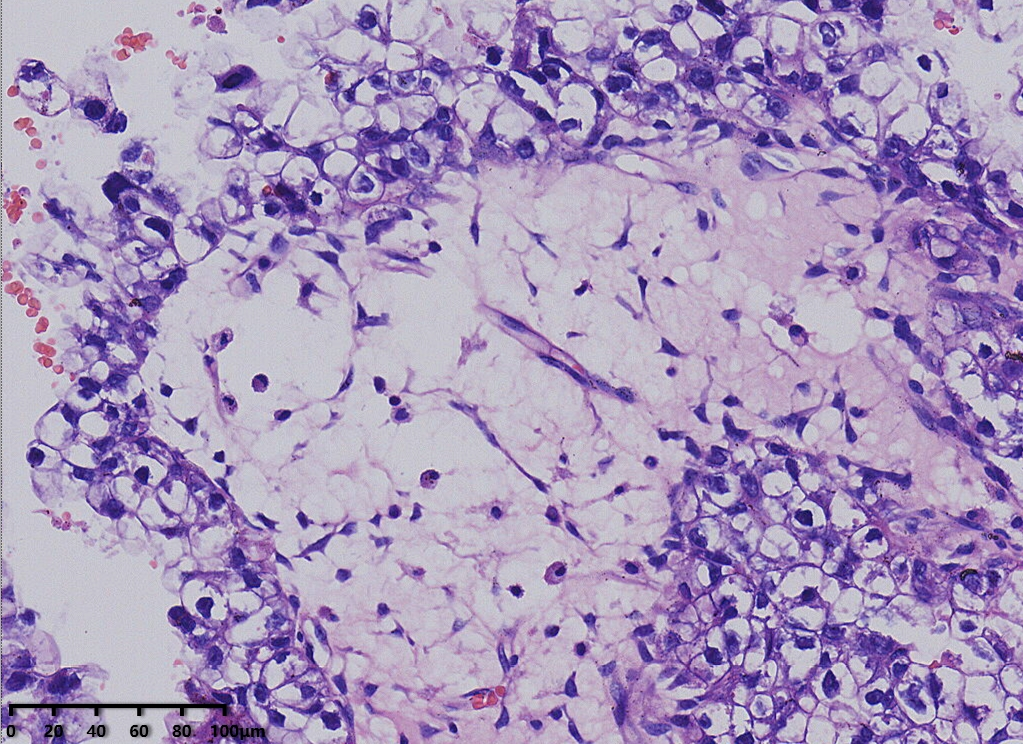
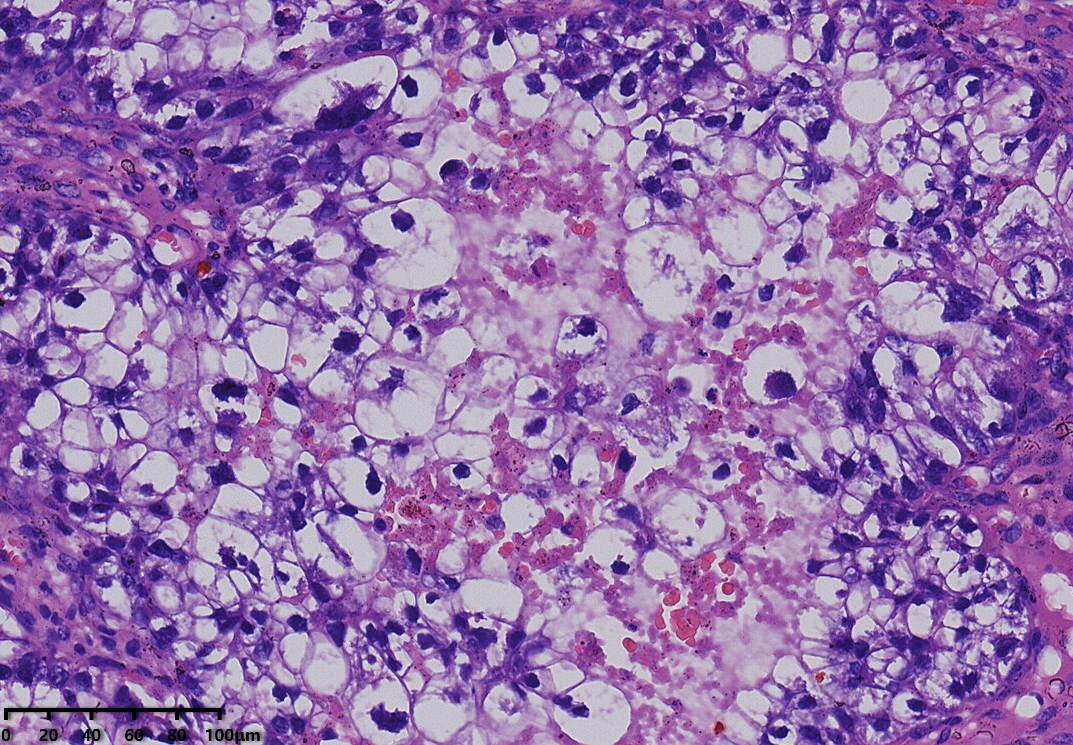
病理诊断:卵巢透明细胞癌
例1以胞浆嗜酸的肿瘤细胞为主,例2以胞质透明的肿瘤细胞为主。
讨论
定义:一种由透明、嗜酸性和靴钉样细胞组成,伴管状、囊状、乳头状和实性结构组合而成的恶性肿瘤。
ICD-O编码:8310/3
临床特征:
卵巢透明细胞癌占卵巢恶性上皮源性肿瘤的5%~25%,仅次于高级别浆液性癌,其发病具有明显的地域差异,亚洲是透明细胞癌的高发地区,尤其是日本,占比约15%~25%,而北美仅为1%~2%。子宫内膜异位症是重要的危险因素,约50%~70%的卵巢透明细胞癌与子宫内膜异位相关。患者平均年龄55岁,合并子宫内膜异位的患者相对年轻,临床表现以腹部肿块为主,当肿瘤侵及周围脏器,会出现相关的临床表现。
病理学特征:
1. 大体特点
肿瘤多累及单侧卵巢,一般较大,直径10~30cm,肿瘤可为囊性,囊实性或者实性,以囊实性为主,但单纯的囊性少见。可为多房或者单房,囊内常见乳头状肿物,实性区域切面为灰白色,鱼肉样。
2. 镜下表现
多种排列方式,管状,囊状,乳头状,微乳头状或实性等结构,以不同比例混合存在,也可以某一种形态为主。乳头为纤细的简单乳头,缺乏复杂的分枝,部分乳头粗大,伴间质玻璃样变,囊内可见蓝色的黏液样物。肿瘤细胞呈鞋钉样,多角形或者立方状,肿瘤细胞胞浆嗜酸性或者为透明的胞质。核圆形或者不规则型,核仁可见。核分裂不常见,一般小于5个/10HPF。卵巢透明细胞癌往往表现为高级别核级以及复杂的组织形态,因此透明细胞癌不作组织学分级。
3. 免疫表型
肿瘤细胞PAX-8、HNF1-β、P504S、NapsinA、CK7阳性,WT-1、CK20等阴性,P16一般为部分阳性,P53多数为野生型表达,绝大部分ER、PR为阴性。HNF1-β敏感度高,NapsinA特异性高,P504S特异性及敏感性一般,因此建议3个抗体联合使用。
分子遗传学:
卵巢透明细胞癌无特异的分子改变,但约50%病例ARIDIA突变,PIK3CA突变率约为30%~40%,PTEN突变率约为8.3%。ARIDIA突变与PIK3CA突变常合并存在,且为肿瘤的早期分子改变。研究发现,在卵巢透明细胞癌也发现有高水平的微卫星不稳定性。
预后:
透明细胞癌通常为高级别肿瘤,最重要的预后因素是肿瘤的临床分期,I期的预后非常好,5年生存率90%,II期为55%,III期和IV期预后较差,仅为14%和4%,合并子宫内膜异位的肿瘤分期相对较早,且患者相对年轻,预后更好。
鉴别诊断:
1. 高级别浆液性癌:卵巢最常见的恶性上皮源性肿瘤,常表现为乳头状及实性结构,但胞浆透明的细胞少见。肿瘤细胞核浆比高,多形性明显,坏死常见,核分裂象易见。肿瘤细胞通常为WT1、CA-125阳性,P16弥漫强阳性,P53为突变型表达,ki67增殖指数高。而卵巢透明细胞癌通常为WT1阴性、p53野生型表达,HNF1β、Napsin A、P504S阳性表达。
2. 低级别浆液性癌:大体以囊实性为主,囊内壁可见乳头状物。镜下肿瘤以乳头状结构为主,分枝状乳头常见,部分乳头水肿明显,具有典型的纤维血管轴心,被覆上皮细胞形态温和,大小相对一致,呈立方状,无明显透明胞质。免疫组化CA-125、P16、WT-1、ER、PR阳性,HNF1β、Napsin A阴性。
3. 转移性肾透明细胞癌:肾透明细胞癌具有纤细的血管网,一般无囊状或乳头状结构,无鞋钉样细胞,且缺乏玻璃样变的间质。低级别肾透明细胞癌,胞浆透明,细胞核小,高级别肾透明细胞癌,胞浆常为嗜酸性,核大,可见核仁。免疫组化通常CK7阴性,CD10阳性表达,此外有肾细胞癌病史有助于鉴别诊断。
4. 无性细胞瘤:卵巢无性细胞瘤呈实性片状或团巢状排列,肿瘤细胞胞质淡染,部分空亮,类似于卵巢透明细胞癌,但无性细胞瘤好发于年轻患者,肿瘤间质富于淋巴细胞,肿瘤细胞核仁明显,免疫组化表达SALL4、CD117、PLAP、OCT3/4,而CK7、HNF1β、Napsin A、P504S阴性。
5. 卵黄囊瘤:多见于年轻女性,大多数患者血清AFP升高,肿瘤具有多种组织学形态,疏松的网状、微囊状(常见形态)、迷路状或乳头状结构,间质疏松黏液变,典型病例可见S-D小体(血管-乳头结构)。免疫组化卵黄囊瘤表达SALL4、Glypican3、AFP,一般不表达CK或局灶表达。
6. 卵巢甲状腺肿伴癌变:卵巢甲状腺肿癌变为乳头状癌,可见乳头状结构及滤泡状结构,类似于卵巢透明细胞癌中的管状、乳头状形态,卵巢甲状腺肿可见正常的甲状腺滤泡及滤泡内的胶质成分,乳头状癌区域可见毛玻璃样核,免疫组化TG、TTF1阳性可帮助鉴别。
参考文献:
[1] 郑文新.沈丹华.郭东辉。妇产科病理学(第2版).
[2] Fadare O, Parkash V.Pathology of Endometrioid and Clear Cell Carcinoma of the Ovary. Surg Pathol Clin. 2019;12(2):529-564.
[3] Gadducci A, Multinu F, Cosio S, et al. Clear cell carcinoma of the ovary: Epidemiology, pathological and biological features, treatment options and clinical outcomes. Gynecol Oncol. 2021;162(3):741-750.
[4] Iida Y, Okamoto A, Hollis RL, et al. Clear cell carcinoma of the ovary: a clinical and molecular perspective. Int J Gynecol Cancer. 2021;31(4):605-616.




 苏公网安备 32011402011742
苏公网安备 32011402011742