患者男性,35岁。病人主因打鼾半年,咽异物感1月入院。核磁显示:鼻咽后壁与头长肌之间占位性病变,行肿物切除术。
大体检查:
灰白不整形软组织1块,大小3.5x2.5x1cm。
形态学特征:
低倍下肿瘤周边呈分叶状、结节状结构,肿瘤细胞片状、条索状排列。高倍下肿瘤胞浆透明或嗜酸性,可见“空泡状”细胞,细胞核圆形,轻度异型,局灶肿瘤细胞呈上皮样,胞核中度异型,间质广泛粘液变性。
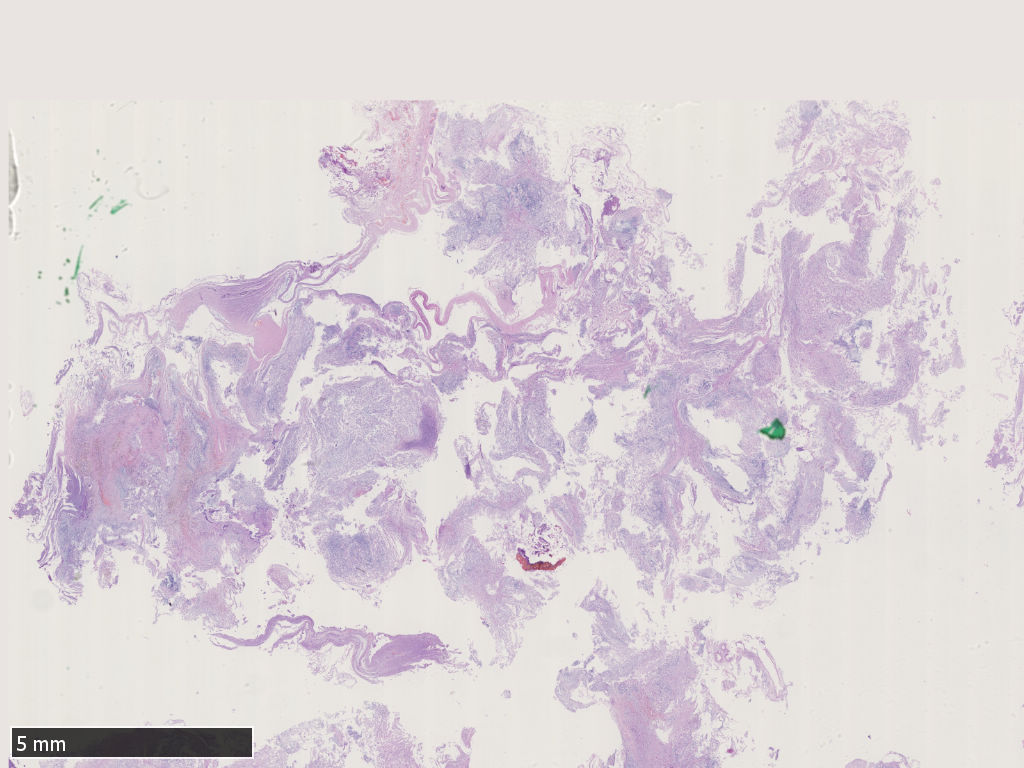
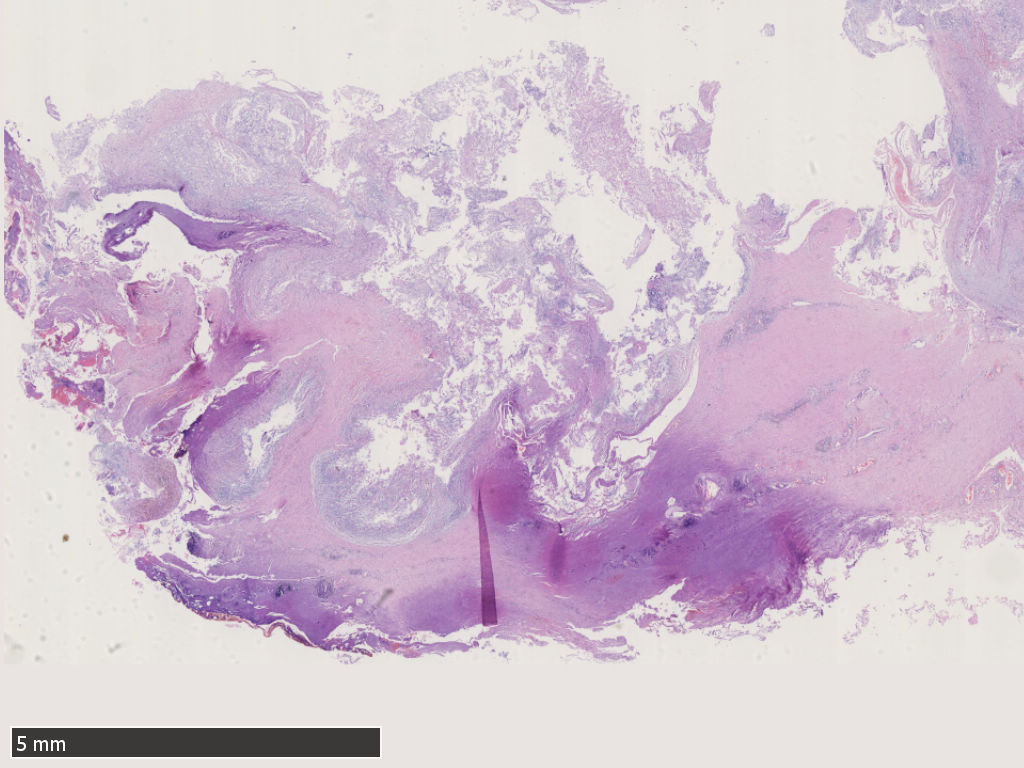
低倍镜下,肿瘤周边呈分叶状、结节状结构,肿瘤内被纤维组织分隔。
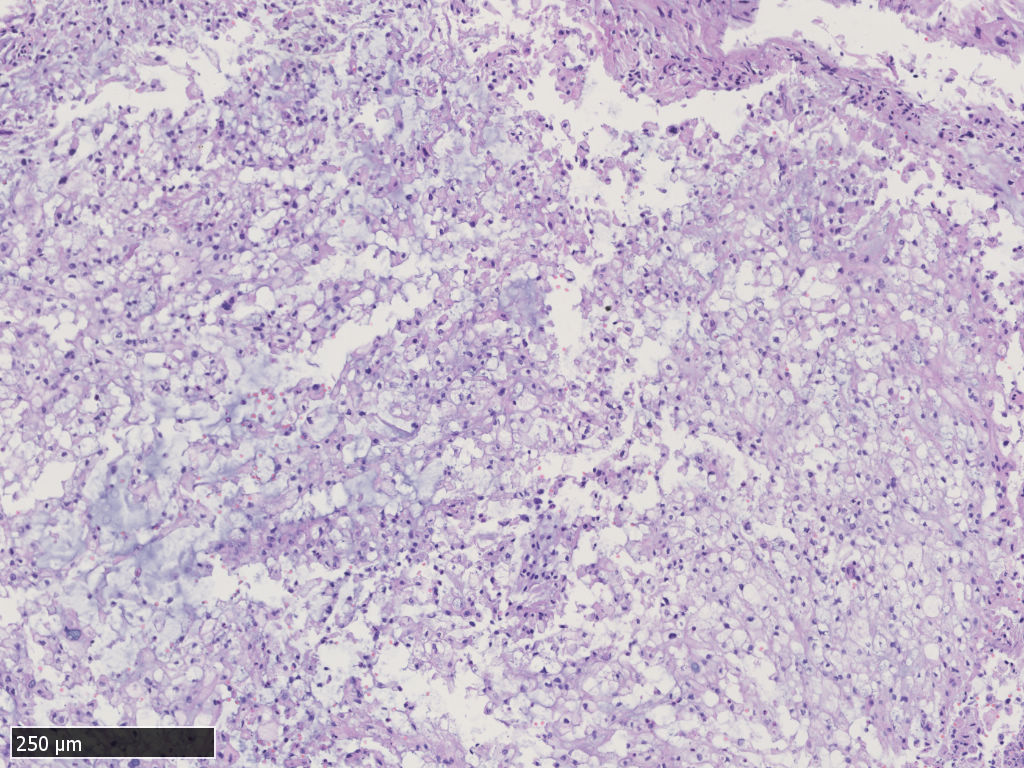
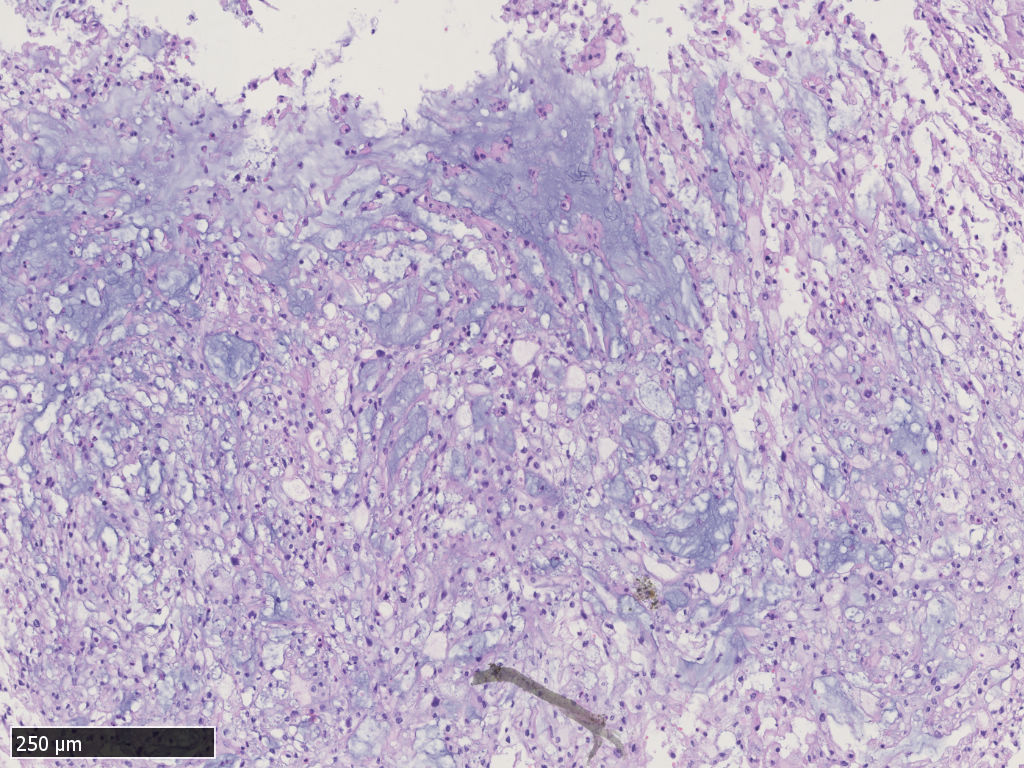
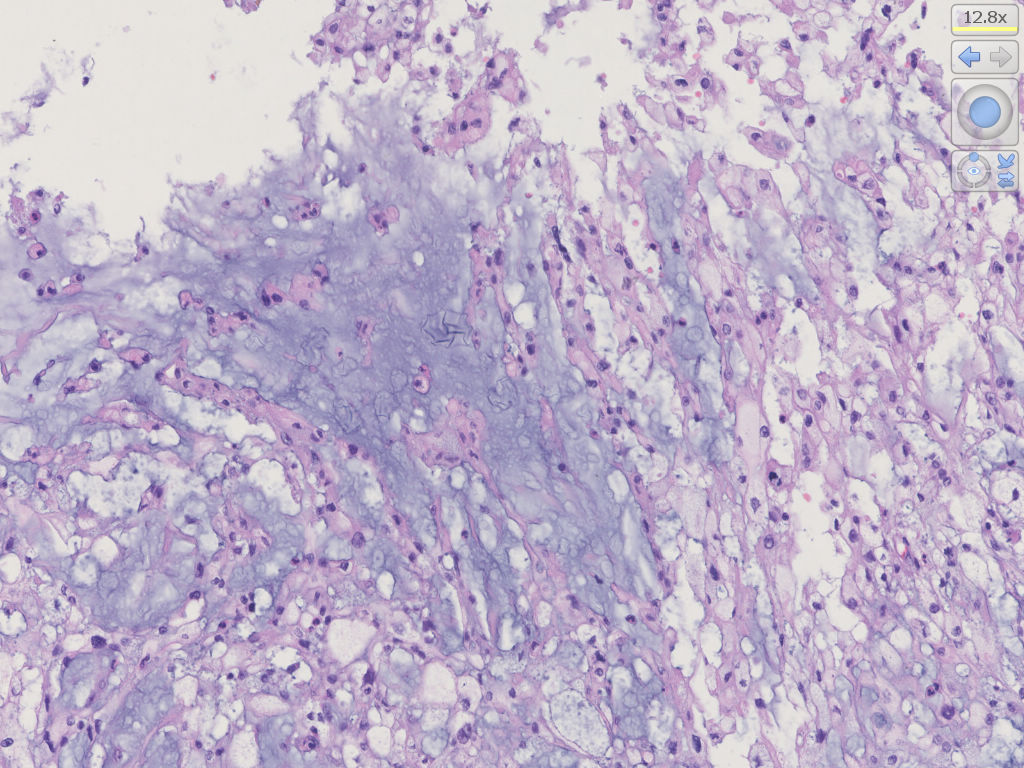
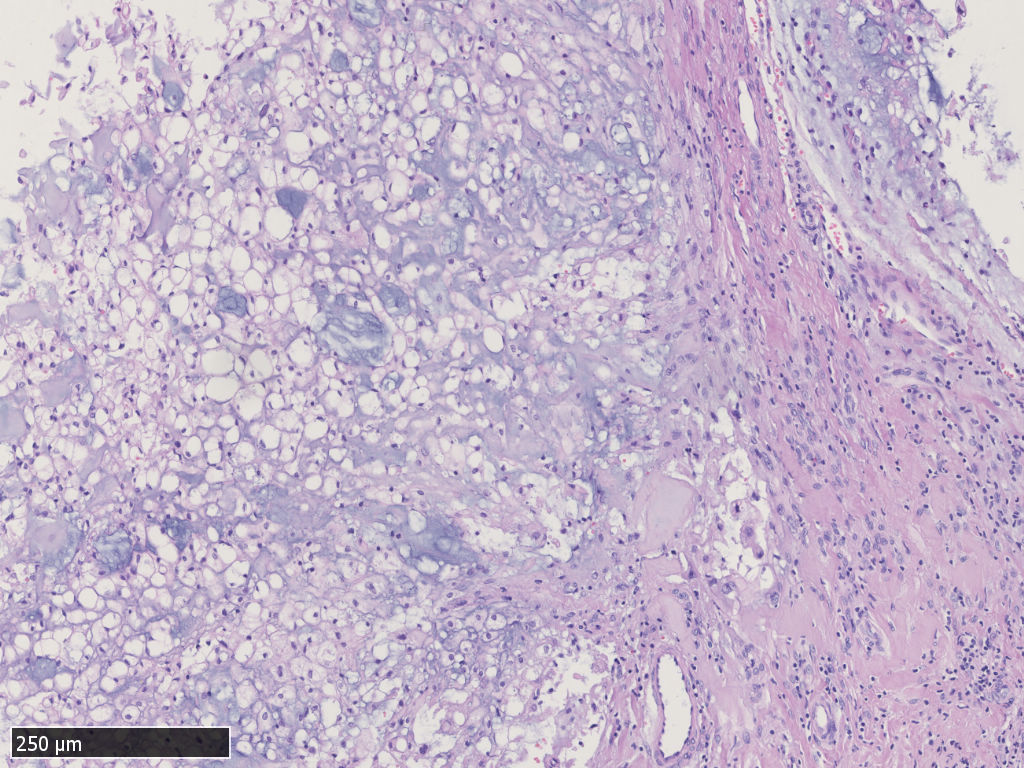
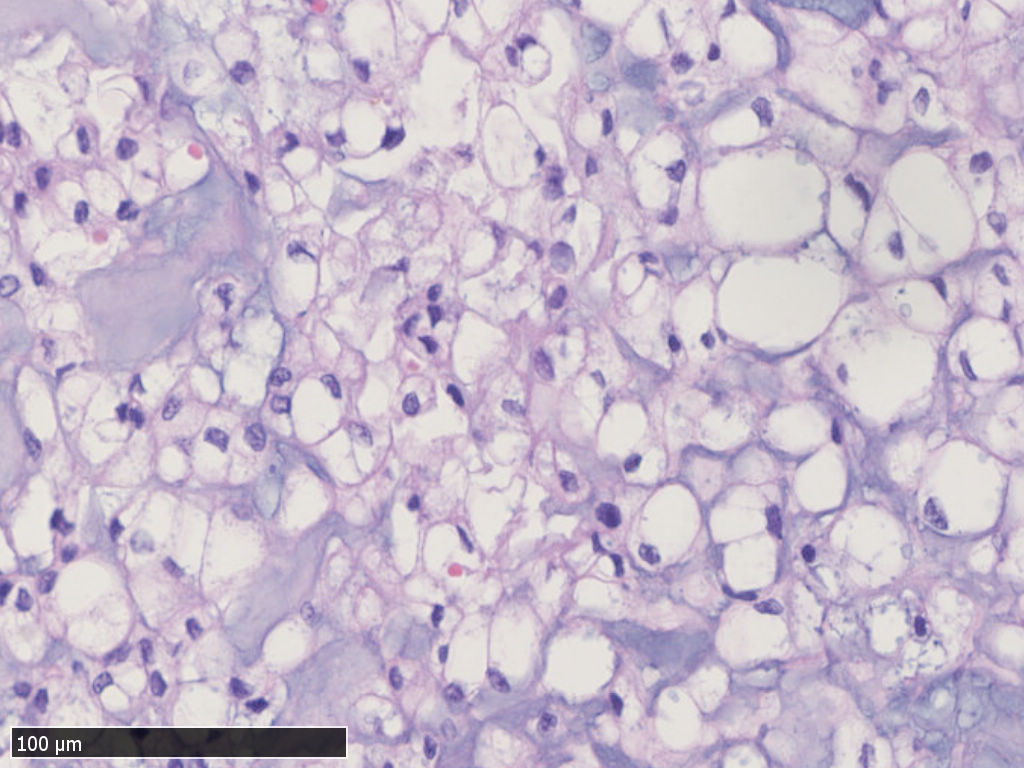
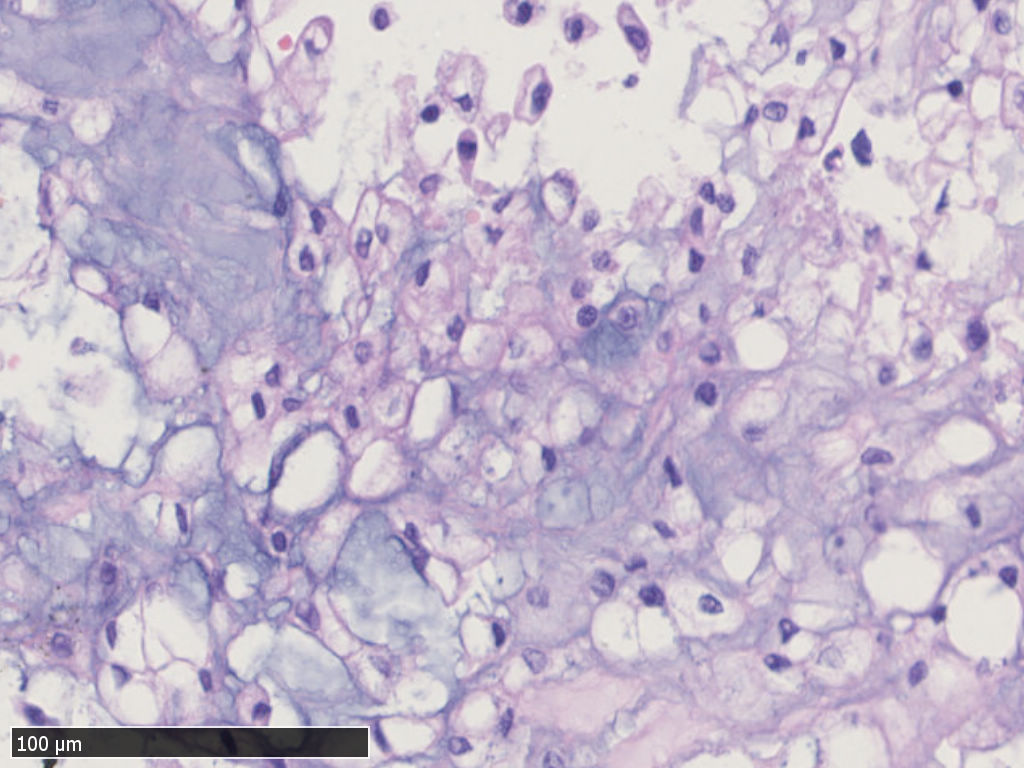
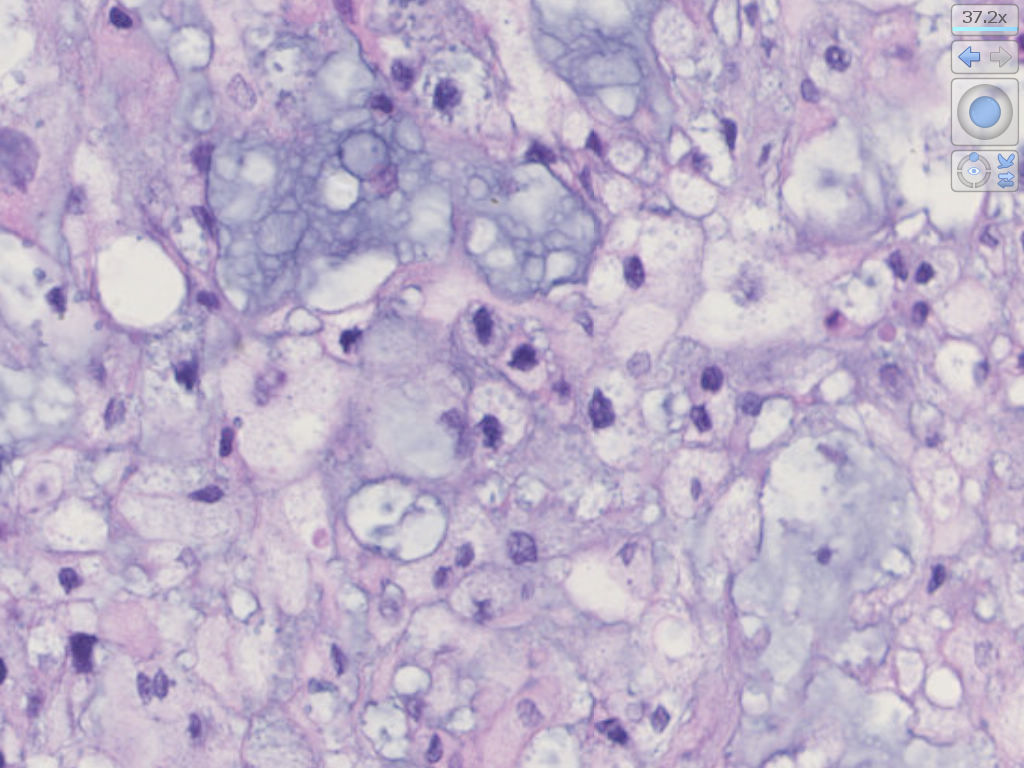
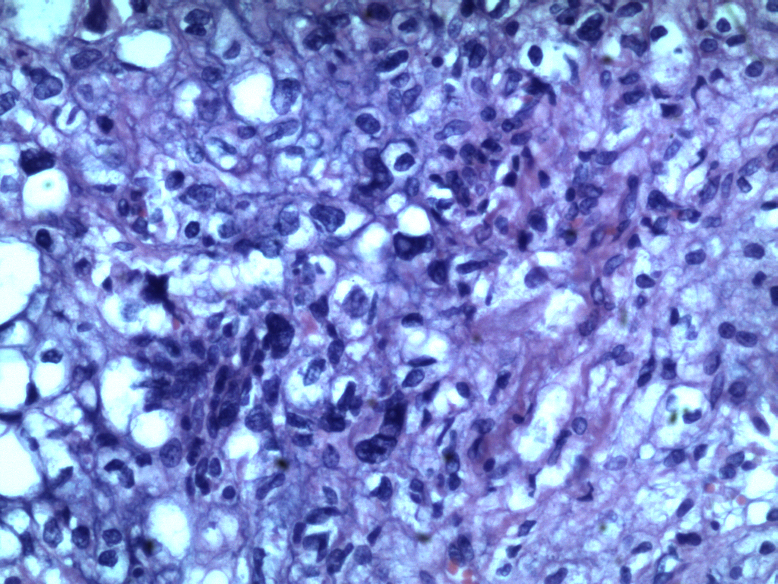
中-高倍镜,肿瘤细胞呈片状、条索状或散在分布于黏液样间质中,可见“泪滴样”细胞,细胞核圆形,轻度异型性,核分裂不易见。部分瘤细胞类似于上皮样细胞,胞浆嗜酸性,非空泡状。
免疫组化结果:
CK+,VIM+,EMA +,S-100 +,KI-67指数约20%。
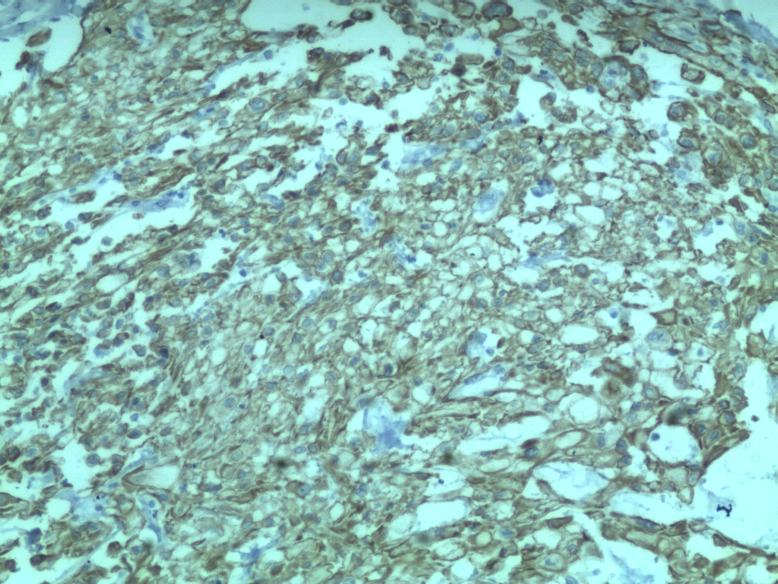
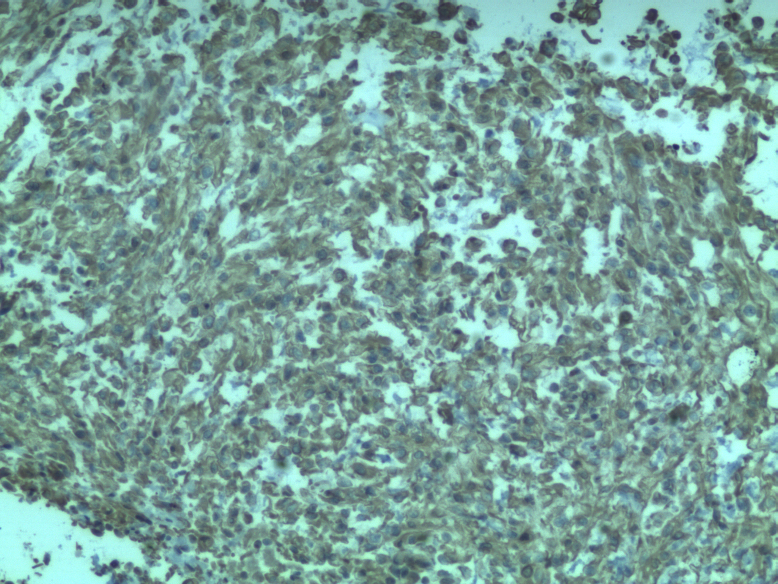
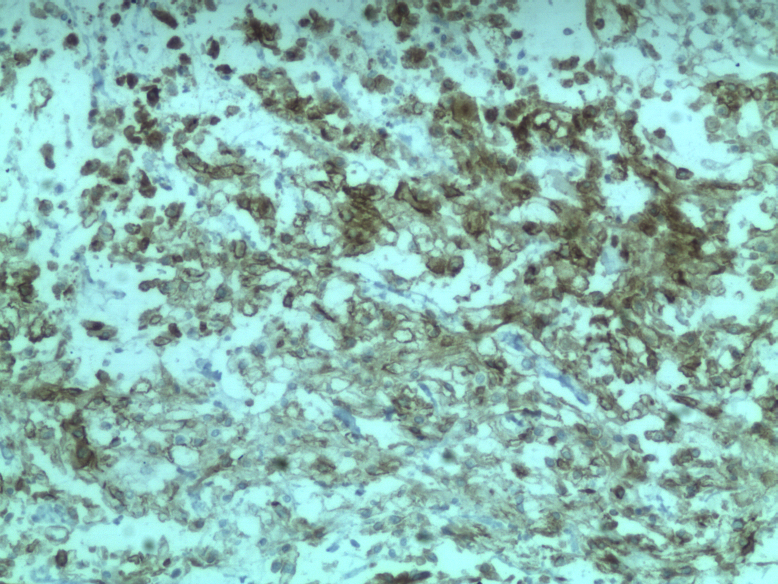
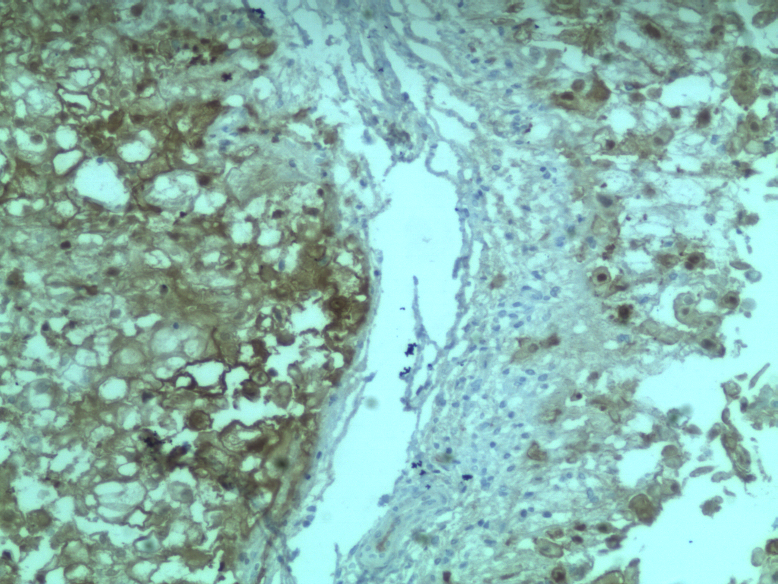
病理诊断:
(咽后壁)经典型脊索瘤。
讨论
定义:
经典型脊索瘤是一种恶性肿瘤,其表型与脊索相似,通常发生在中轴骨的骨骼中。
ICD-O 编码:93700/3
发生部位:
脊索瘤主要位于中轴骨,涉及从颅底到尾骨的骨骼,32%是颅骨,32.8%在脊柱,29.2%在骶骨和尾骨。仅报告了少量轴骨外脊索瘤。儿童和年轻人的肿瘤更容易发生在颅底和上颈部。
临床特征:
脊索瘤最常见的症状是疼痛和与部位相关的神经系统症状。
病理形态:
1.大体特征
脊索瘤表现为小叶状实性肿块,呈凝胶状,破坏骨骼并延伸至周围软组织。骶尾部肿瘤往往比其他部位的肿瘤大,很可能与较长的无症状期有关。
2.镜下特征
第五版WHO骨肿瘤分类将脊索瘤分为三个亚型:经典型脊索瘤(Conventional chordoma)、差分化脊索瘤(Poorly differentiated chordoma)、去分化脊索瘤(Dedifferentiated chordoma)。
经典型脊索瘤
·镜下表现为典型的分叶状结构,其间被纤维性条带分隔,肿瘤细胞呈片状、条索状或散在分布于黏液样间质中。
·脊索瘤的细胞俗称为"泪滴样“细胞,因胞质内含有多少不一的黏液而类似于印戒细胞或呈空泡状或气球样,还可存在红染的、非空泡样的胞质,类似于上皮样细胞,但这些细胞并不代表去分化表现。
·细胞核圆形,轻度异型性,核分裂不常见。
·术语“软骨样脊索瘤”是指脊索瘤的大面积基质模仿透明软骨肿瘤。
去分化脊索瘤
去分化脊索瘤是一种具有双相外观的脊索瘤。其特征是同时存在传统脊索瘤和高级别梭形和/或多形性肉瘤。这两种成分通常会突然分离,但也可以混合在一起。可以看到骨肉瘤和横纹肌肉瘤的分化。
差分化脊索瘤
·差分化脊索瘤是一种具有脊索分化的低分化肿瘤,通常发生在轴骨中,其特征是SMARCB1表达缺失。主要见于儿童和年轻成人患者,预后不良。
·差分化脊索瘤由成片的上皮样细胞巢构成,通常具有局灶性横纹肌样形态。有相对丰富的嗜酸性细胞质和分散的细胞质液泡,让人想起印戒细胞。
·细胞核圆形至卵圆形,染色质泡状,显示轻度至中度多形性,有丝分裂活性增加。
·地图样坏死常见。
免疫组化:
脊索瘤肿瘤细胞可表达Brachyury、CK、EMA、Vimentin、S-100。去分化脊索瘤可显示局灶性细胞角蛋白表达,但不表达Brachyury。差分化脊索瘤表达细胞角蛋白和Brachyury,S100呈可变阳性,诊断特征是SMARCB1(INl1)表达缺失。
鉴别诊断:
1. 良性脊索细胞瘤 是一类显示脊索分化的良性肿瘤,多于体检或尸检时偶然发现。良性脊索细胞瘤境界清楚,没有溶骨性破坏。显微镜下肿瘤细胞呈空泡状,细胞核小而扁平,常被挤压在细胞周围,似成熟脂肪细胞。鉴别主要依靠核异型性和浸润性生长方式,免疫组化指标Brachyury 和Ki-67 增殖指数并不是鉴别的要点。
2. 软骨肉瘤 多发生于老年人,显微镜下肿瘤呈分叶状生长,可见黏液样基质,肿瘤小叶浸润和包绕先前存在的骨小梁(软骨包骨),肿瘤细胞密度较丰富,细胞核大小不一、深染,双核细胞易见。免疫组化指标D2-40 表达阳性,而Brachyury、EMA 和PCK 阴性表达。在分子遗传学方面,大约半数的软骨肉瘤存在异柠檬酸脱氢酶突变。
3. 脊索瘤样脑膜瘤 是一类少见亚型脑膜瘤,多见于儿童,位于幕上,与脑膜关系密切。显微镜下肿瘤细胞排列呈条索状分布于黏液样基质中,空泡细胞存在使其形似脊索瘤,但局灶漩涡状结构,肿瘤细胞核圆形、卵圆形似脑膜皮细胞,免疫组化指标PCK 阴性可鉴别。
4. 横纹肌样瘤 差分化脊索瘤需要和横纹肌样瘤进行鉴别,两者在形态学和免疫表型有重叠,但横纹肌样瘤不表达Brachyury。
5. 黏液乳头状室管膜瘤 室管膜瘤的特殊亚型,起源于终丝、马尾、圆锥的神经胶质细胞。当脊索瘤有丰富的黏液样基质且发病部位位于骶尾部时,需与脊索瘤鉴别。但黏液乳头状室管膜瘤有特征性假乳头结构、血管周围无核区和微囊,且免疫组化GFAP 阳性可辅助鉴别。
6. 转移性癌 当脊索瘤上皮样特征明显、异型性增加、细胞核分裂象增多时,可考虑转移性癌可能,此时应注意寻找原发病灶。转移性癌有其特有的形态学特点及免疫表型,可供鉴别。
分子遗传学特征:
FISH 显示11q13重排,导致MENI基因纯合性丢失和PPPICA的杂合性丢失。冬眠瘤强烈表达棕色脂肪标记基因UCP1;未检测到HMGA2、CDK4或MDM2的重排、扩增或表达增加。
治疗和预后:
·经典型脊索瘤总体中位生存时间为7年。多达40%脊索瘤发生在颅底以外的部位转移。转移部位包括肺、骨、淋巴结和皮下组织。最佳的治疗方法是根治性手术切除,但考虑到解剖位置的原因,复发率较高,复发或转移时经常需要辅助放疗。
·去分化脊索瘤预后极差;转移率和死亡率高。化疗或放疗的益处似乎微不足道。手术是唯一的选择。
·差分化脊索瘤治疗包括手术、放射治疗和化疗的组合。文献中报道的病例不到60例,但这种类型的脊索瘤预后较差,比传统脊索瘤更差。
参考文献:
1. 梁春梅,管雯斌等,差分化脊索瘤8 例临床病理分析并文献复习。诊断病理学杂志 2022年12月第29卷第12期。
2. 李美蓉,冉龙燕等,脊索瘤30 例临床病理分析及文献复习。肿瘤预防与治疗 2023年4月第36卷第4期J Cancer Control Treat ,April 2023,Vol. 36,No.4.
3. WHO Classification of Tumours Editorial Board. WHO classification of tumours of soft tissue and bone[M]. 5th ed.Lyon, France: IARC Press; 2020.
4. Yeter H G, Kosemehmetoglu K, Soylemezoglu F. Poorly differentiated chordoma: Review of 53 cases[J]. APMIS, 2019,127(9):607-615.
5. 丁宜,黄啸原,临床病理诊断与鉴别诊断—骨与关节疾病[M], 人民卫生出版社, 2021.




 苏公网安备 32011402011742
苏公网安备 32011402011742