肺篇(2)
未分化和不常见的肺癌
诊断条件:手术切除标本+CK标志物确定上皮起源+缺乏腺细胞和鳞状细胞分化或神经内分泌形态+ ADC(TTF1 或 napsin A)和 SCC(p40、p63 或 CK5/6)的 IHC 标志物均应为阴性+粘蛋白染色阴性或少于5个阳性细胞每2个高倍视野。
Ø LCC是一种未分化的NSCLC,不能在小活检或细胞学标本上做出诊断,是一种排除性诊断。
Ø 如果不存在神经内分泌形态,则不推荐使用神经内分泌标志物。但是,如果形态学上未分化的NSCLC(CK 阳性、TTF1 阴性、p40 阴性)显示神经内分泌标志物染色阳性,则应将其称为具有神经内分泌分化的LCC。
Ø 一些LCC中多mRNA的表达模式可能与分化的SCC或ADC中的模式相匹配。在LCC中可能发现ADC相关的分子改变(EGFR、KRAS、BRAF、MAP2K1/MEK1、NRAS、ERBB2/HER2和ALK)或SCC相关的突变(PI3K和AKT1),但是不符合ADC或SCC的IHC染色谱。
Ø 尽管分子分析可以为将 LCC 细化为临床相关的ADC和SCC提供基础,但这些分子特征的特异性不足以取代LCC的组织学诊断,并且很大一部分LCC仍将是未分化癌。然而,如果观察到与ADC相关的致癌驱动因素(EGFR、BRAF和ALK)的基因改变,一些LCC的分子分析可以指导治疗。
肉瘤样癌(SC)
在世卫组织最新的肺癌分类中,肺SC是一种异质性肿瘤,涵盖多形性癌(PC)、癌肉瘤和肺母细胞瘤。
Ø PC是一种低分化NSCLC,含有1种或多种常规癌成分,其中至少10%的肉瘤样成分以梭形细胞或巨细胞为特征,或由纯恶性梭形细胞(梭形细胞癌)或纯肿瘤巨细胞(巨细胞癌)组成的癌。
Ø 只要常规癌成分明显,SC的诊断不需要梭形细胞和巨细胞成分中上皮标志物的表达。当肉瘤样成分占主导地位且 CK 表达非常微弱或缺失时,诊断可能非常具有挑战性,并且必须进行IHC检查以区分SC与其他梭形细胞肿瘤,包括肉瘤样间皮瘤、原发性或转移性肉瘤、转移性肉瘤样的肾细胞癌(RCC)和黑色素瘤。
- 黑色素瘤(S100、SOX10、Melan-A、HMB-45);
- 孤立性纤维瘤(STAT6和 CD34);
- 肌源性肿瘤(SMA、desmin和其他肌源性抗体);
- 滑膜肉瘤 (SS)(TLE1 、CD99、BCL2、SS18-SSX和SSX C);
- 血管肿瘤(CD31、ERG和 FLI1);
- 周围神经鞘瘤(SOX10、S100 和 H3K27me3 缺失)。
胸部SMARCA4缺陷型未分化肿瘤(SMARCA4-dUT)
主要特征:
高度侵袭性+SMARCA4(BRG1)缺失+未分化的圆细胞或横纹肌样形态+30-59岁的年轻患者+男性好发,男女比例为9:1+与吸烟密切相关+最常受累部位是纵隔,其次是肺和胸膜。
免疫组化:
- SMARCA4和SMARCA2 缺失,SMARCB1(INI1)表达;
- SOX2、CD34 和 SALL4强阳性;
- CK(pan细胞角蛋白或 EMA)局灶性弱阳,claudin 4基本上呈阴性;
- Syn可呈阳性,极少数病例显示p63、TTF1、p40和WT1阳性。
- SMARCA4缺陷型NSCLC:SMARCA4缺陷型NSCLC含有形态上与SMARCA4-dUT不同的鳞状和实性成分,不表达SMARCA4-dUT中的SOX2、CD34和 SALL,从而可以区分这两种实体。
- SMARCA4-dUT对结蛋白、NUT和S100呈阴性,其标志性的SMARCA4缺失有助于与NUT癌、黑色素瘤或某些低分化或未分化癌相鉴别。
NUT癌
主要特征:
NUT基因重排+低分化癌+片状和巢状的小至中等大小的单一、原始外观的肿瘤细胞+突然的角化灶。仅形态学表现经常导致NUT 癌误诊为基底样鳞状细胞癌、SCLC、淋巴瘤或某些生殖细胞肿瘤。
免疫组化:
- NUT蛋白呈独特的斑点状核阳性,该独特表达模式仅限于NUT癌,这是诊断要求,也是与其他肿瘤鉴别的独特IHC特征;
- CKpan呈阳性,p40/p63 通常呈阳性,提示鳞状分化,TTF1很少阳性;
- NUT癌可以表达Syn、CgA;
- NUT癌通常CD34呈阳性。
- 生殖细胞肿瘤 特别是精原细胞瘤,是唯一表达NUT抗体的其他肿瘤,但染色较弱且局灶阳性,无斑点状图案,NUT癌对其他生殖细胞标志物呈阴性。
- NUT癌通常CD34呈阳性,这可能导致误诊为白血病。然而,NUT癌对其他淋巴造血系统标志物呈阴性。
- SMARCA4-dUT SMARCA4和NUT的IHC染色可以帮助鉴别二者。
- 当遇到低分化鳞状细胞癌或其他低分化癌时,需要考虑对NUT核表达的IHC评估。
原发性肺癌与各种转移性肺癌的鉴别
肺部转移性肿瘤比原发性肿瘤更常见,因为肺是远处转移的热门器官之一。原发性和继发性肺肿瘤的鉴别通常需要对肿瘤进行IHC染色以支持诊断。表3总结了不同器官部位的癌中CK7和CK20的染色谱,列出的肿瘤特异性标志物可以进一步帮助诊断原发性肺ADC或特定器官的转移性癌。
表3肺腺癌(ADC)与肺转移癌的鉴别标志物
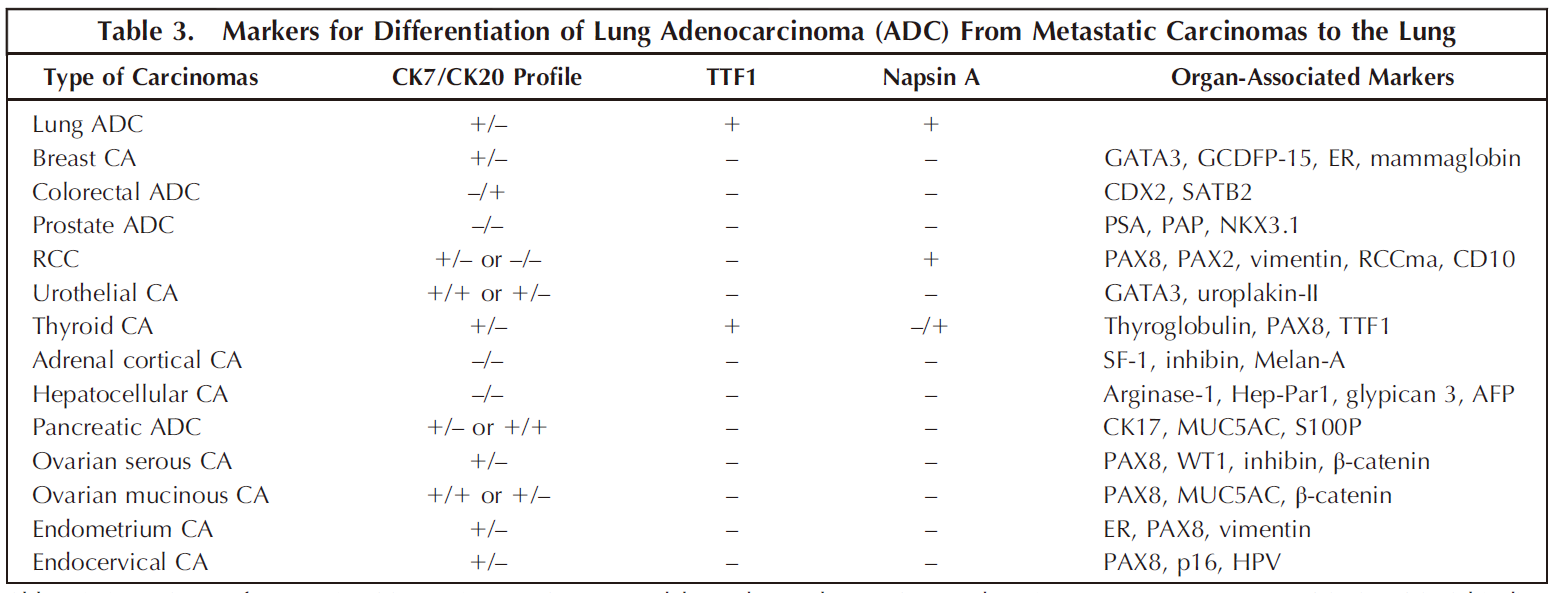
u 原发性肺腺癌 TTF1和/或napsinA对原发性肺ADC都具有高敏感性和特异性。在 TTF1的2个市售克隆中,单克隆抗体8G7G3/1在区分肺原发性和转移性癌方面优于 SPT24。甲状腺球蛋白、PAX8和 PAX2可以帮助排除甲状腺和肾脏源性肿瘤。
u 转移性乳腺癌 乳腺癌常见的IHC标志物包括GATA3、TRPS1、mammaglobin、GCDFP-15和雌激素受体。
- GATA3是确定乳腺起源的非常有用的标志物。在91%的乳腺导管癌、100%的乳腺小叶癌、86%的尿路上皮癌和0%-20%的原发性肺鳞状细胞癌中表达。在肺ADC中很少表达(0%-8%),因此,如果尿路上皮癌不在鉴别诊断中,GATA3的强核染色通常有利于乳腺原发性的判定(图4,A)。
- TRPS1是最近报道的乳腺癌(包括三阴性乳腺癌(TNBC))的高敏感性和特异性标志物。显著高于GATA3在化生(86% vs 21%)和非化生(86% vs 51%)TNBC中的表达。与GATA3 相比,TRPS1在尿路上皮癌或其他肿瘤类型(包括肺ADC、胰腺ADC、结肠和胃ADC、RCC、黑色素瘤和卵巢癌)中无表达或很少表达。
- Mammaglobin和GCDFP-15是非常特异性的乳腺标志物,但它们检测乳腺癌的敏感性并不理想,分别为40%-60%和20%-40%。GCDFP-15在肺ADC很少阳性(2%),Mammaglobin通常对肺ADC呈阴性,但在唾液腺型癌中可能呈阳性。
- 雌激素受体不是乳腺特异性标志物,但其阳性与其他乳腺特异性标志物的表达相结合,支持乳腺癌的诊断。
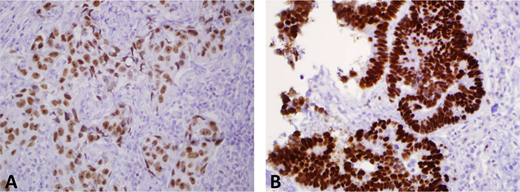
图4,A,转移性乳腺癌显示 GATA3 核染色。B,转移性结肠腺癌显示 SATB2 核染色(原始放大倍率×40 [A 和 B])。
u 转移性结直肠腺癌
肺黏液性ADC通常对TTF1和 napsin A呈阴性,而对CK20(局灶性或斑片状)和 CDX2通常呈阳性。此外,还发现TTF1在少数结直肠癌中呈阳性(0%-4.3%),具体取决于不同的TTF1克隆。因此,鉴别肺黏液腺癌和转移性结肠黏液腺癌非常具有挑战性。在这种情况下,SATB2(一种最近公认的高度敏感和特异性的结直肠标志物)将非常有用。研究表明,当SATB2用于诊断转移性结直肠癌时,比CDX2更具特异性(图 4,B),并可以排除黏液性肺ADC。
u 转移性胰腺黏液性腺癌
肺和胰腺的黏液性ADC的免疫特征相似,无法使用有用的IHC标志物鉴别。此外,据报道,形态学和分子检测的作用也有限。然而,在大约50%的胰腺黏液性ADC中报告的SMAD4(SMA 和 MAD 相关蛋白 4)表达缺失可能有助于区分黏液性肺ADC和黏液性胰腺ADC。
u 转移性前列腺ADC
前列腺腺泡腺癌通常对CK7和CK20均呈阴性,但前列腺导管癌除外,前列腺导管癌可能为CK7阳性。PSA和PSAP是前列腺敏感和特异性的标志物,可识别90%以上的转移性前列腺ADC,但两者在低分化肿瘤中都可能表现出较弱的表达。更新的抗体NKX3.1对高级别和转移性前列腺ADC具有接近100%的敏感性和特异性。
u 妇科来源的转移癌
p16(宫颈ADC)、WT1(浆液性癌)和 PAX8(苗勒管上皮肿瘤)具有很好的鉴别效用,因为它们在肺ADC中通常为阴性。然而,TTF1在子宫和卵巢癌的一个亚群中可能呈阳性。同样,在大多数卵巢和子宫内膜来源的透明细胞癌中可见napsin A阳性。
² 关于PAX8抗体,市售有2种PAX8抗体:兔多克隆抗体(P)和小鼠单克隆抗体(M)。
- 两种 PAX8 抗体在肾癌、甲状腺癌和妇科癌中均呈高百分比表达。与 PAX8(P)相比,PAX8(M)对甲状腺癌、肾癌和卵巢癌表现出更高的特异性和敏感性。
- PAX8(P)抗体也与B细胞、胰腺癌、胃肠道类癌和一些软组织肿瘤发生交叉反应。而PAX8(M)抗体则不发生类似的交叉反应,使PAX8(M)成为确认原发肿瘤部位和鉴别诊断的极好标志物。




 苏公网安备 32011402011742
苏公网安备 32011402011742