我国食管癌发病虽有明显的地区差异,但食管癌的病死率均较高。据报道,预计2012年全世界食管癌新发患者数455800例,死亡人数达400200例。在中国,近年来食管癌的发病率有所下降,但死亡率一直位居第四位。2017年陈万青等报道,2013年我国食管癌新发病例27.7万,死亡人数为20.6万,我国食管癌粗发病率为20.35/10万,城市粗发病率为15.03/10万,农村为30.73/10万;我国食管癌粗死亡率为15.17/10万,城市粗发病率为14.41/10万,农村为21.05/10万;发病率及死亡率分别列全部恶性肿瘤的第六和第四位。因此,食管癌一直是威胁我国居民健康的主要恶性肿瘤。我国食管癌高发地区山西阳城县、江苏扬中县和山西磁县的食管癌粗发病率高达109.5/10万、109.3/10万和103.5/10万(2003年),我国食管癌流行的特点是发病率男性高于女性,农村高于城市,高发区主要集中在太行山脉附近区域(河南、河北、山西、山东泰安、山东济宁、山东菏泽、安徽、江苏苏北区域)。其他高发区域与中原移民有关,包括四川南充、四川盐亭、广东汕头、福建福州等地区。因此,对高危人群和高发地区人群的筛查,早期发现和早期治疗阻断早期食管癌发展成为中晚期食管癌是提高食管癌生存效果和保证患者生活质量的根本出路。也是减轻我国政府和民众医疗负担的长期有效措施。另外,对于中晚期食管癌的规范诊断和治疗也是改善中晚期食管癌效果的有效措施,可使众多的食管癌患者受益,因此,食管癌筛查、早诊早治和规范化诊治是全国各级各类具备基本资质医疗机构及其医务人员的重要任务。
组织学类型上,我国食管癌以鳞状细胞癌为主,占90%以上,而美国和欧洲以腺癌为主,占70%左右。吸烟和重度饮酒是引起食管鳞癌的重要因素。流行病学研究显示:吸烟和重度饮酒是引起食管癌的重要因素。国外研究显示:对于食管鳞癌,吸烟者的发生率增加3~8倍,而饮酒者增加7~50倍。在我国食管癌高发区,主要致癌危险因素是致癌性亚硝胺及其前体物和某些真菌及其毒素。而对于食管腺癌,主要的危险因素包括胃食管反流和巴雷特食管(Barrett esophagus)。
食管癌的高危人群指居住生活在食管癌高发区,年龄在45岁以上,有直系家属食管癌或消化道恶性肿瘤病史或其他恶性肿瘤病史,有食管癌的癌前疾病或癌前病变者是食管癌的高危人群。对高危人群的筛查是防治食管癌的重点。
食管癌的预防措施主要包括避免一些高危因素如吸烟和重度饮酒,防霉,去除亚硝胺,改变不良饮食生活习惯和改善营养卫生。另外,对高发区高危人群进行食管癌筛查可以早期发现食管癌或癌前病变,起到早诊早治和预防的作用,改善食管癌患者的生存质量和提高治疗效果。
对于食管癌的治疗主要依据食管癌的分期早晚给予不同的治疗方法,早期位于黏膜层内的肿瘤主要应用腔镜下黏膜切除或黏膜剥离术治疗,而对于超出黏膜层侵及黏膜下层的早中期食管癌主要选择外科手术治疗为主。术后必要时给予辅助化疗或放疗,对于中晚期食管癌主要以手术为主的综合治疗为主。切除有困难或有2个以上肿大转移淋巴结者通常给予术前放化疗或放疗或化疗,然后给予手术治疗,术后必要时再给予化疗或放疗。
二、食管癌诊疗流程
食管癌诊断与治疗的一般流程见图1。
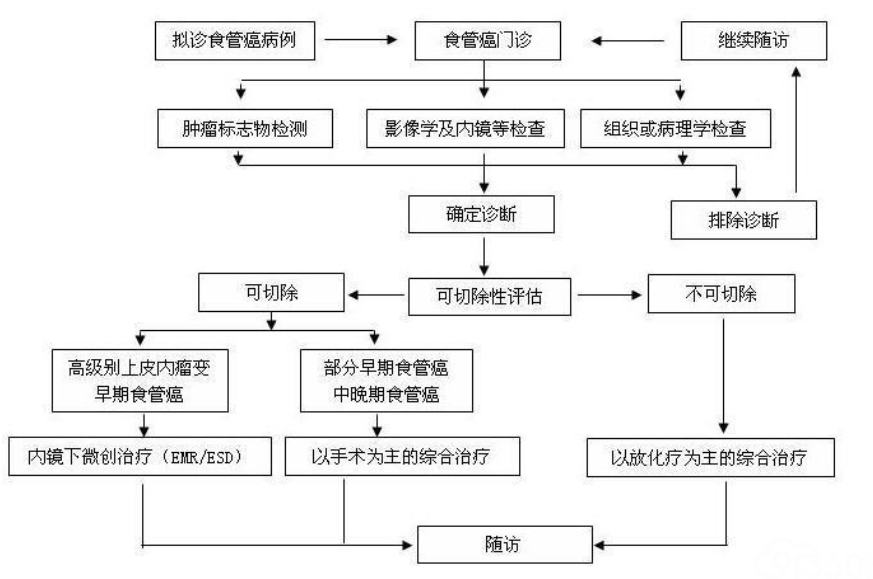
图1食管癌规范化诊疗流程
三、食管癌诊断规范
(一)临床诊断
1.食管癌高危因素和高危人群
高危因素:年龄40岁以上,长期饮酒吸烟、直系家属有食管癌或恶性肿瘤病史、具有上述癌前疾病或癌前病变者。
高危人群:具有上述高危因素的人群,尤其是生活在食管癌高发区,年龄在40岁以上,有肿瘤家族史或者有食管癌的癌前疾病或癌前病变者、长期饮酒和吸烟者。
2.食管癌的临床表现
(1)症状:吞咽食物时有哽咽感、异物感、胸骨后疼痛,或明显的吞咽困难等,考虑有食管癌的可能,应进一步检查。
早期食管癌的症状一般不明显,常表现为反复出现的吞咽食物时有异物感或哽咽感,或胸骨后疼痛。一旦上述症状持续出现或吞咽食物有明显的吞咽哽咽感或困难时提示食管癌已为中晚期。
当患者患者出现胸痛、咳嗽、发热等,应考虑有食管穿孔的可能。当患者出现声音嘶哑、吞咽梗阻、明显消瘦、锁骨上淋巴结肿大或呼吸困难时常提示为食管癌晚期。
(2)体征:查体时大多数食管癌患者无明显相关阳性体征。当患者出现有头痛、恶心或其他神经系统症状和体征,骨痛、肝大、胸腹腔积液、体重明显下降、皮下结节,颈部淋巴结肿大等提示有远处转移的可能,需要进一步检查确诊。
有上述症状和体征者需进一步进行以下检查进行确诊和鉴别诊断。
(二)辅助检查
1.血液生化检查
食管癌患者实验室常规检查的目的是为了评估患者的一般状况以及是否适于采取相应的治疗措施,包括血常规、肝肾功能、肝炎、梅毒、艾滋病等抗原抗体检查、凝血功能等其他必要的实验室检查。食管癌患者血液碱性磷酸酶或血钙升高考虑骨转移的可能;血液谷氨酰转肽酶、碱性磷酸酶、谷草转氨酶、乳酸脱氢酶或胆红素升高考虑肝转移的可能。进食不适感,特别是晚期吞咽困难的食管癌患者,可用前白蛋白和白蛋白水平评估患者营养状况。
2.肿瘤标志物检查
目前常用于食管癌辅助诊断、预后判断、放疗敏感度预测和疗效监测的肿瘤标志物有细胞角蛋白片段19(cytokeratin-19-fragment, CYFRA21-1)、癌胚抗原(carcinoembryonic antigen,CEA)、鳞状上皮细胞癌抗原(squarmous cell carcinoma antigen,SCC)和组织多肽特异性抗原(tissue polypeptide specific antigen,TPS)等。上述标志物联合应用可提高中晚期食管癌诊断和预后判断及随访观察的准确度。目前应用于食管癌早期诊断的肿瘤标志物尚不成熟。
3.影像学检查
(1)气钡双重对比造影:它是目前诊断食管癌最直接、最简便、最经济而且较为可靠的影像学方法,食管气钡双重对比造影可发现早期黏膜表浅病变,对中晚期食管癌诊断价值更大,对于食管癌的位置和长度判断较直观。但对食管外侵诊断正确率较低,对纵隔淋巴结转移不能诊断。
(2)电子计算机断层成像(CT):作为一种非创伤性检查手段,CT被认为是对食管癌分期及预后判断较好的方法之一,在了解食管癌外侵程度,是否有纵隔淋巴结转移及判断肿瘤可切除性等方面具有重要意义,CT的分辨率高,特别是多排螺旋CT,扫描速度极快,数秒内即可完成全食管扫描,避免了呼吸及心跳等运动伪影;进行多期动态增强扫描,最小扫描层厚为0.5mm,用于判断食管癌位置、肿瘤浸润深度、肿瘤与周围结构及器官的相对关系、区域淋巴结转移以及周围血管肿瘤侵犯,为临床上准确分期提供可靠的依据。推荐检查胸部+上腹部增强CT扫描,如果病变位于颈部或胸段食管癌距环咽肌<5cm,建议行颈部+胸部+上腹部CT扫描,如果患者有CT静脉造影的禁忌证,可以考虑(颈部)胸部/上腹腔平扫CT、颈部及腹部超声。CT检查特点,可以在术前明确病变范围、淋巴结有无转移、远处有无转移等情况,也可用于术后(放化疗后)疗效评价,不足之处有组织分辨率不高,无法准确评估肿瘤外侵情况及小淋巴结转移情况。关于临床分期,CT判断T分级的准确度58%左右,判断淋巴结转移的准确度54%左右,判断远隔部位如肝、肺等处转移的准确度37%~66%。
(3)磁共振成像:无放射性辐射,组织分辨率高,可以多方位、多序列成像,对食管癌病灶局部组织结构显示优于CT。特别是高场强磁共振设备的不断普及和发展,使磁共振扫描速度大大加快,可以和CT一样完成薄层、多期相动态增强扫描,对病变侵犯范围、与周围器官的关系及淋巴结的检出率均有提高。另外,功能成像技术(如弥散加权成像、灌注加权成像和波谱分析)均可为病变的检出和定性提供有价值的补充信息。磁共振检查组织分辨率高,多平面、多参数扫描,可以比CT更有效评估肿瘤分期;不足之处在于扫描时间较长,受呼吸及心跳伪影干扰较多,一般不用于疗效评价。
(4)超声检查:超声通常并不能显示食管病灶,食管癌患者的超声检查主要应用于颈部淋巴结、肝脏、肾脏等部位及脏器转移瘤的观察,为肿瘤分期提供信息。超声还可用于胸腔、心包腔积液的检查及抽液体前的定位。超声引导下穿刺可对颈部淋巴结、实质脏器的转移瘤进行穿刺活检获得标本进行组织学检查。
(5)正电子发射计算机断层显像(PET-CT)检查:正电子发射计算机断层显像(PET-CT)可确定食管癌原发灶的范围,了解周围淋巴结有否转移及转移的范围,准确判断肿瘤分期。与胃镜及螺旋CT相比,18F-FDG PET-CT 在食管癌病灶检测方面有更高的敏感度及特异度,因而能更精确地进行TNM分期。PET检查较胸部CT能发现更多的远处转移。在常规检查阴性的患者中,PET可以发现15%~20%的患者存在远处转移。另外PET-CT还可用于食管癌的疗效评价,术前放疗及化疗均推荐应用PET-CT检查,目前认为PET-CT是用于评估治疗效果和预后指标前景发展很好的检查工具。建议局部进展期食管癌在手术前、术前治疗时、根治性放化疗时,应用PET-CT或PET提高分期检查的准确度,和作为术前治疗、根治性放化疗后常规评价疗效手段的补充。但SUV的临界值和治疗后行PET-CT的时间尚没有统一标准化,治疗后行PET-CT的时间可能会影响PET-CT判断的准确度。因为在某些情况下如放射性食管炎和与活检相关的炎症发生时实施PET-CT可能影响对于病灶的判读。因此,建议在治疗后2周,且无任何活检检查的情况下进行PET-CT检查。对于无远处转移的患者来说,PET-CT评估范围为颅底至大腿根部。对于怀疑远处转移者应考虑全身检查。
上述几种重要的影像学检查技术,各有特点,优势互补,应该强调综合检查运用,全面评估。
4.内镜检查
(1)普通白光纤维胃镜:在普通胃镜观察下,早期食管癌可以表现为食管黏膜病灶,有以下几种状态:①红区,即边界清楚的红色灶区,底部平坦;②糜烂灶,多为边界清楚、稍凹陷的红色糜烂状病灶;③斑块,多为类白色、边界清楚、稍隆起的斑块状病灶;④结节,直径在1cm以内,隆起的表面黏膜粗糙或糜烂状的结节病灶;⑤黏膜粗糙,指局部黏膜粗糙不规则、无明确边界的状态;⑥局部黏膜上皮增厚的病灶,常遮盖其下的血管纹理,显示黏膜血管网紊乱、缺失或截断等特点。内镜医师应提高对上述形态特征的认识,在检查时注意观察黏膜的细微变化,对可疑病灶多点活检是提高早癌检出率的关键。然而,多数早期食管癌在普通内镜下表现不典型,可能会被漏诊,病灶范围亦不清晰,因而检查中结合色素或电子染色的方法进行观察有助于提高病变检出率。中晚期食管癌的内镜下所见比较明确且容易辨认,主要表现为结节状或菜花样肿物,食管黏膜充血水肿、糜烂或苍白发僵,触之易出血,还可见溃疡,部分有不同程度的管腔狭窄。如CT显示食管病变位于胸中上段或颈段,与气管膜部或左主支气管关系密切,应同时作纤维支气管镜检查,以观察气管、支气管是否受侵。
(2)色素内镜:将各种染料散布或喷洒在食管黏膜表面后,使病灶与正常黏膜在颜色上形成鲜明对比,更清晰地显示病灶范围,并指导指示性活检,以提高早期食管癌诊出率。色素内镜常用染料有碘液、甲苯胺蓝等,可单一染色,也可联合使用。
(3)超声内镜(Endoscopic ultrasound,EUS):EUS下早期食管癌的典型表现为局限于黏膜层且不超过黏膜下层的低回声病灶。EUS可清楚显示食管壁层次结构的改变、食管癌的浸润深度及病变与邻近脏器的关系,T分期的准确度可达74~86%,但EUS对病变浸润深度诊断的准确度易受病变大小及部位的影响。EUS诊断局部淋巴结转移的敏感度为80%,明显高于CT(50%)及PET(57%),但特异度(70%)略低于后二者(83%和85%)。EUS对食管癌腹腔淋巴结转移的诊断敏感度和特异度分别为85%和96%,均高于CT(42%和93%)。 EUS联合FNA可进一步提高对可疑淋巴结转移的诊断效能。由于超声波穿透力有限,EUS难以用于远处转移的评估,应结合CT、MRI或PET-CT等影像学检查。
5.其他检查
(1)心电图:术前筛查患者是否有心律失常及心肌梗死史。
(2)肺功能:术前筛查患者肺容量和肺通气功能及弥散功能。
(3)运动心肺功能:当上述检查不能判断患者的心肺功能是否可以耐受手术时,推荐做运动心肺功能检查进一步判断。
(4)超声心动图:对既往有心脏病史的患者推荐超声心动图检查,明确患者的心脏结构改变和功能状况。
(5)心脏冠脉造影:对高龄和有冠心病史者推荐行心脏冠脉造影检查以明确患者的心脏供血状况和评估手术风险。
(二)诊断
1. 临床诊断
根据上述临床症状、体征及影像学和内镜检查,符合下列之一者可作为临床诊断依据。
(1)吞咽食物时有哽咽感、异物感、胸骨后疼痛或出现明显的吞咽困难,食管造影发现食管黏膜局限性增粗、局部管壁僵硬、充盈缺损或龛影等表现。
(2)吞咽食物时有哽咽感、异物感、胸骨后疼痛或出现明显的吞咽困难,胸部CT检查发现食管管壁的环形增厚或不规则增厚。
临床诊断食管癌病例需经病理学检查确诊。不宜依据临床诊断做放化疗,也不提倡进行试验性放化疗。
2. 病理诊断
根据临床症状、体征及影像学和内镜检查,经细胞学或组织病理学检查,符合下列之一者可确诊为食管癌。
(1)纤维食管镜检查刷片细胞学或活检为癌。
(2)临床诊断为食管癌,食管外转移病变(锁骨上淋巴结、皮肤结节等)经活检或细胞学检查明确诊断为食管癌转移病灶。
(三)鉴别诊断
食管癌的诊断的主要手段为食管镜+组织学活检/细胞学,食管镜检查加活检病理检查为食管癌诊断的“金标准”。其他手段均为辅助手段,主要为了解部位、大小、期别和制订手术方式提供必要的信息。食管癌的鉴别诊断主要需与食管其他良恶性疾病和食管周围疾病对食管的压迫和侵犯所致的一些改变进行鉴别。
1.食管其他恶性肿瘤
食管其他恶性肿瘤很少见,包括癌肉瘤、平滑肌肉瘤、纤维肉瘤、恶性黑色素瘤、肺癌或其他恶性肿瘤纵隔淋巴结转移对食管的侵犯等。
(1)食管癌肉瘤(esophageal sarcoma): 影像表现与腔内型食管癌十分相似,多为带蒂的肿物突入食管腔内形成较粗大的食管腔内不规则的充盈缺损,病变段食管腔明显变宽。
(2)食管平滑肌肉瘤(esophageal leiomyosarcoma): 可以表现为息肉型或浸润型2种类型。息肉型多为较大的软组织肿物,向食管腔内突出,表面被覆食管黏膜,常有蒂与食管壁相连。浸润型同时向腔内、外生长,食管壁增厚、表面常伴有中央溃疡。X线胸片可见纵隔走行部位肿物影。食管造影见食管腔内巨大肿块,管腔狭窄偏位,也可呈局限性扩张,其内有大小不等的息肉样充盈缺损,黏膜平坦或破坏,中央可有龛影。
(3)食管恶性黑素色瘤(esophageal melanoma): 原发食管恶性黑色素瘤很少见,肿瘤表现为食管腔内的结节状或分叶状肿物,表面呈棕黑色或棕黄色,呈息肉状突入腔内,可有有蒂与食管壁相连。影像表现类似腔内型食管癌。
(4)食管转移瘤: 原发肿瘤常为气管肿瘤、甲状腺癌、肺癌、肾癌、乳腺癌等。这些癌通过直接侵犯或淋巴结转移而累及食管。食管镜检查常为外压性改变。由血行播散至食管壁的转移瘤罕见。其食管造影所见也与腔内型食管癌相似。
2.食管良性肿瘤和瘤样病变
食管良性肿瘤有平滑肌瘤、腺瘤、脂肪瘤、乳头状瘤、血管瘤等。瘤样病变包括息肉、囊肿、弥漫性平滑肌瘤病和异位症等。其中大部分为平滑肌瘤(50%~70%)。
(1)食管平滑肌瘤(esophageal leiomyoma): 食管镜下表现为食管壁在性结节状肿物,表面被覆有正常黏膜。触之似可在黏膜下滑动。可以单发或多发。常为单发肿物,呈圆型、卵圆型、哑铃型或不规则的生姜状。镜下由交错的平滑肌和纤维组织所构成,有完整的包膜。食管钡餐造影呈圆型或卵圆型的壁在性肿物,大小不一,边缘光滑锐利,正面观肿瘤局部食管增宽,表面黏膜皱襞消失,但其对侧黏膜正常。肿瘤表面黏膜常无钡剂覆盖,表现为均匀的充盈缺损,称之为涂抹征或瀑布征。切线位肿物与食管之交界呈钝角。肿物表面黏膜被展平或呈分叉状,邻近黏膜被推移。怀疑平滑肌瘤时不能活检,以免产生炎症粘连而导致手术切除时黏膜破损。
(2)其他壁在性良性肿物:如血管瘤、脂肪瘤、息肉等的食管造影所见与平滑肌瘤相仿。纤维血管性息肉好发于颈段食管且有蒂,有时可见其在食管腔内上下移动甚至返至口腔内。脂肪瘤质地较软,有一定的活动度,CT或MRI检查可见低密度或脂肪信号。
3.食管良性病变
(1)食管良性狭窄(bnign esophageal stricture): 患者有明确的误服强酸或强碱的病史。病变部位多在食管生理狭窄区的近端,以食管下段最多见,食管管腔长段狭窄,边缘光整或呈锯齿状,管壁僵硬略可收缩,移行带不明显。
(2)贲门失弛症(achalasia of cardia):患者多在年轻时起病,有长期反复进食下咽困难和需用水冲食物帮助吞咽的病史。食管造影显示贲门区上方食管呈对称性狭窄,狭窄段食管壁光滑呈漏斗状或鸟嘴状,其上方近端食管扩张明显。镜下可见有食物潴留、食管黏膜无破坏,镜子常可通过狭窄进入胃腔。但应与少数食管下段的狭窄型食管癌而导致的癌浸润性狭窄鉴别。
(3)消化性食管炎(peptic esophagitis): 患者有长期吞咽疼痛、反酸、胃灼热等症状,然后由于炎症反复,局部发生瘢痕狭窄而出现吞咽困难。食管钡餐造影示食管下段痉挛性收缩,黏膜增粗或模糊,有糜烂或小溃疡时可有小的存钡区或龛影。长期炎症病变可导致纤维化而出现管腔狭窄,但狭窄较对称。食管仍有一定的舒张度,镜下可见病变段食管黏膜糜烂和小溃疡形成,官腔轻度狭窄,与正常食管黏膜间的移行带不明显,常伴有食管裂孔疝和胃食管反流现象。病变黏膜的改变在服用抑制酸分泌药物如洛赛克等治疗一段时间后有明显改观,症状也会有明显改善。
(4)食管静脉曲张(esophageal varices): 患者常有肝硬化病史,无明显吞咽困难症状。造影表现为息肉样充盈缺损,重度病变黏膜增粗呈蚯蚓状或串珠状,但食管壁柔软,有一定的收缩或扩张功能,无梗阻的现象。镜下可见食管下段黏膜下增粗迂曲的静脉,触之较软。切忌活检,以免导致大出血。
(5)外压性狭窄: 食管周围良性肿瘤直接压迫或恶性肿瘤导致颈部和纵隔淋巴结肿大、大血管病变或变异及其他纵隔内病变如结合性淋巴结结侵犯食管壁均可造成食管受压而导致狭窄,镜下一般为外压性改变,局部黏膜光整无破坏。其边缘较清晰,但若恶性肿大淋巴结或结核性淋巴结侵及食管壁直至黏膜,可以导致局部黏膜破坏和溃疡形成。通过活检可以明确诊断。
(6)食管结核(esophageal tuberculosis):食管结核比较少见,临床表现患者多有进食发噎史,发病时年龄一般较年轻。食管结核感染途径可有:①由喉或咽部结核向下蔓延;②结核菌通过肺结核的痰液下咽时直接侵入食管黏膜;③脊柱结核侵及食管;④血行感染播散道食管壁内;⑤食管旁纵隔淋巴结核干酪性变侵蚀食管壁(临床最为常见)。食管造影所见病变部位稍窄发僵,常有较大溃疡形成,周围的充盈缺损及黏膜破坏等不如食管癌时明显。镜下可见较大而深的溃疡,没有食管癌时明显的黏膜糜烂和狭窄及多个结节样改变。通过活检可以进行鉴别诊断。
(四)食管癌的病理分类和分期
1.食管癌的分段
(1)颈段食管:上自下咽,下达胸廓入口即胸骨上切迹水平。周围毗邻气管、颈血管鞘和脊椎。内镜下测量距上切牙15~20cm。
(2)胸上段食管:上起胸廓入口,下至奇静脉弓下缘(即肺门水平之上)。其前面被气管、主动脉弓的3个分支及头臂静脉包围,后面毗邻脊椎。内镜下测量距上切牙20~25cm。
(3)胸中段食管:上起奇静脉弓下缘,下至下肺静脉下缘(即肺门水平之间)。其前方夹在两肺门之间,左侧与胸降主动脉为邻,后方毗邻脊椎,右侧游离直接与胸膜相贴。内镜下测量距上切牙25~30cm。
(4)胸下段食管:上起自下肺静脉下缘,下至食管胃结合部(即肺门水平之下)。内镜下测量距上切牙30~40cm。
2.食管癌的大体分型(附录A)
(1)早期食管癌:包括隐伏型、糜烂型、斑块型和乳头型。
(2)中晚期食管癌:包括髓质型、蕈伞型、溃疡型、缩窄型和腔内型(附录B)。
3.食管癌的病理分类及分型
(1)病理术语和定义
①食管癌(esophageal carcinoma):来源于食管黏膜上皮细胞的恶性肿瘤,主要有鳞状细胞癌和腺癌两种组织学类型。横跨食管胃交界部的鳞状细胞癌仍认为是食管癌。
②上皮内瘤变/异型增生(intraepithelial neoplasia/dysplasia):食管癌的癌前病变,包括鳞状细胞癌的癌前病变和腺癌的癌前病变,即鳞状上皮和腺上皮的上皮内瘤变/异型增生。上皮内瘤变和异型增生两个名词可通用。
鳞状上皮的上皮内瘤变/异型增生,是指以食管黏膜鳞状上皮内不同层次的异型鳞状细胞为特征的癌前病变,根据病变累及层次,分为低级别上皮内瘤变/异型增生(局限于鳞状上皮下1/2),高级别上皮内瘤变/异型增生(累及食管鳞状上皮超过下1/2)。
腺上皮的上皮内瘤变/异型增生,是指以食管腺上皮不同程度的细胞异型性和结构异常为特征的癌前病变,主要见于巴雷特食管,根据细胞异型性和结构异常的程度,分为低级别上皮内瘤变/异型增生和高级别上皮内瘤变/异型增生,分级标准同
③早期食管癌(early esophageal carcinoma):局限于黏膜层的食管浸润性癌,无论有无区域淋巴结转移。
④表浅食管癌(superficial esophageal carcinoma):局限于黏膜层或黏膜下层的食管浸润性癌,无论有无区域淋巴结转移。
⑤进展期食管癌(advanced esophageal carcinoma):浸润肌层或更深层次的食管浸润性癌。
⑥食管胃交界部腺癌(adenocarcinoma of the esophagogastric junction):食管胃交界部腺癌是横跨食管胃交界部的腺癌。解剖学上食管胃交界部是指管状食管变为囊状胃的部位,即食管末端和胃的起始,相当于腹膜反折水平或希氏角或食管括约肌下缘,与组织学上的鳞柱交界不一定一致。
⑦胃食管反流病(gastroesophageal reflux disease,GERD)及反流性食管炎(reflux esophagitis):胃食管反流病是指胃和(或)十二指肠内容物反流入食管,引起不适症状和(或)并发症的一种疾病。特征性的症状为胃灼热和反流。反流性食管炎是胃食管反流病的主要病理学表现之一,表现为食管黏膜的炎症、糜烂、溃疡形成,晚期甚至可出现纤维组织增生、食管狭窄等改变。
⑧巴雷特食管(Barrett esophagus):食管远端黏膜的鳞状上皮被化生的柱状上皮替代即为巴雷特食管。化生的单层柱状上皮可为胃型上皮也可为伴有杯状细胞的肠型上皮,伴有肠上皮化生者进展为腺癌的风险明显提高。按照中华医学会消化病分会巴雷特食管诊治共识建议,消化病理学组达成共识,即以食管远端存在柱状上皮化生作为巴雷特食管的定义和诊断标准,诊断报告必须详细注明柱状上皮化生组织学类型和是否存在肠上皮化生及上皮内瘤变/异型增生。
(2)病理诊断分类、分级和分期
①组织学分型(附录B):推荐使用2010版消化系统肿瘤WHO分类。
②组织学分级:鳞状细胞癌和腺癌依据分化程度分为高分化、中分化和低分化。
③食管癌分期(附录C):推荐使用美国癌症联合会(AJCC)TNM分期(第8版)。
(3)新辅助治疗后根治术标本的病理学评估(附录D)
新辅助治疗后病理学改变的基本特征包括:肿瘤细胞退变、消减,大片坏死;纤维组织增生、间质炎症细胞浸润、钙盐沉积等。鳞状细胞癌新辅助治疗后可能出现仅有角化物而无癌细胞残存,腺癌新辅助治疗后可能出现大的黏液湖而无癌细胞残存,均不能将其认为是肿瘤残存。
食管癌的疗效分级系统宜采用CAP(College of American Pathologists)/NCCN(The National Comprehensive Cancer Network)指南的标准。
4.标本类型及固定规范
(1)标本类型
常见标本类型包括:内镜活检标本、内镜下黏膜切除术/内镜下黏膜下剥离术标本(EMR/ESD)和根治切除术标本。
(2)标本固定
①应及时、充分固定,采用10%中性缓冲福尔马林固定液,应立即固定(手术切除标本也尽可能半小时内),固定液应超过标本体积的10倍以上,固定时间6~72小时。
②内镜活检标本:标本离体后,应由内镜医师或助手用小拨针将活检钳上的组织立即取下,并应在手指上用小拨针将其展平,取小块滤纸,将展平的黏膜平贴在滤纸上,立即放入固定液中固定。
③内镜下黏膜切除术(EMR)/内镜下黏膜下剥离术(ESD)标本:应由内镜医师展平标本,黏膜面向上,使用不生锈的细钢针固定于软木板(或泡沫板)上,避免过度牵拉导致标本变形,亦不应使标本皱褶,标记口侧及肛侧方向,立即完全浸入固定液中。
④根治切除术标本:沿肿瘤对侧打开食管壁。黏膜面向上,使用大头针固定于软木板(或泡沫板)上,板上应垫纱布,钉好后黏膜面向下,尽快(离体30分钟内)完全浸入固定液中。
5.取材及大体描述规范
(1)查对
取材时,应核对基本信息,如姓名、送检科室、床位号、住院号、标本类型等。
(2)活检标本
①大体检查及记录:描述送检组织的大小及数目。
②取材:送检黏膜全部取材,应将黏膜包于滤纸中以免丢失,取材时应滴加伊红,利于包埋和切片时技术员辨认。大小相差悬殊的要分开放入不同脱水盒,防止小块活检组织漏切或过切。包埋时需注意一定要将展平的黏膜立埋(即黏膜垂直于包埋盒底面包埋)。一个蜡块中组织片数不宜超过3片、平行方向立埋(由于食管癌前病变及早期癌多较平坦,而对食管癌前病变程度及早期癌的判断要看异型细胞累及鳞状上皮层次的比例、是否有黏膜固有层浸润,对组织层次清晰度要求较高。只有做好上述展平和立埋这两步骤,才能保证切片上活检组织的层次分明,这对食管早期癌及癌前病变的准确诊断至关重要)。蜡块边缘不含组织的白边尽量用小刀去除,建议每张玻片含6~8个连续组织片,便于连续观察。
(3)内镜下黏膜切除术(EMR)/内镜下黏膜下剥离术(ESD)标本
①大体检查及记录:测量并记录标本大小(最大径×最小径×厚度),食管胃交界部标本要分别测量食管和胃的长度和宽度。记录黏膜表面的颜色,是否有肉眼可见的明显病变,病变的轮廓是否规则,有无明显隆起或凹陷,有无糜烂或溃疡等,记录病变的大小(最大径×最小径×厚度)、大体分型(附录A)以及病变距各切缘的距离(至少记录病变与黏膜侧切缘最近距离)。多块切除的标本宜由手术医师根据内镜下病变的轮廓/碘不染色轮廓(食管鳞状上皮病变)在标本固定前进行重建。复杂标本建议临床病理沟通或由手术医师提供标本延展及重建的示意图。
②取材:内镜下黏膜切除术(EMR)/内镜下黏膜下剥离术(ESD)标本应全部取材。宜涂碘(从固定液中取出并至少冲水半小时以上再做碘染色)识别病变(碘不染色区)和最近侧切缘。垂直于最近侧切缘取材。黏膜侧切缘与基底切缘可用墨汁或碳素墨水标记(有条件的可于口侧和肛侧涂不同颜色以便于辨别),以便在镜下观察时能够对切缘做出定位,并评价肿瘤切缘情况。食管胃交界部标本宜沿口侧-肛侧的方向取材,以更好的显示肿瘤与食管胃交界的关系。每间隔2~3mm平行切开,全部取材。如果标本太大,可以进行改刀,将1条分为多条,分别标记a、b等。按同一方向立埋(包埋第一块和最后一块的刀切面,如果第一块和最后一块镜下有病变,再翻转180°包埋,以确保最终切片观察黏膜四周切缘情况),并记录组织块对应的包埋顺序/部位。记录组织块对应的部位(建议附照片或示意图并做好标记)。建议将多块切除的标本分别编号和取材,不需考虑侧切缘的情况,其他同单块切除标本。
(4)根治切除术标本规范
①大体检查及记录:取材时记录切除食管长度,可见或未见食管胃交界部,如果有则记录胃的长度。肿瘤部位(结合手术及内镜检查):颈段食管、胸上段食管、胸中段食管、胸下段食管、食管胃交界部。记录肿瘤距口侧切缘和肛侧切缘及环周切缘的距离。肿瘤大体分型(包括外观描写)(附录A)、大小、切面颜色、质地;浸润深度;累及/未累及食管胃交界部(肿瘤与食管胃交界部的关系:肿瘤完全位于食管,未累及食管胃交界部;肿瘤中心位于远端食管,累及食管胃交界部;肿瘤中心位于食管胃交界部;肿瘤中心位于近端胃,累及食管胃交界部)。累及食管胃交界部者,记录肿瘤中心距食管胃交界部的距离(单位:cm)(用于Siewert分型)。
食管癌建议报告与食管胃交界部的关系;食管胃交界部腺癌建议报告Siewert分型(附录E)。
②取材:必要时涂碘(从固定液中取出并至少冲水半小时以上再做碘染色)识别病变(碘不染色区)。食管取材可自肿瘤中心从口侧切缘至肛侧切缘取一条组织分块包埋(包括肿瘤、肿瘤旁黏膜及两端切缘),并记录组织块对应的方位(宜附照片或示意图并做好标记)。推荐纵向取两端切缘与肿瘤的关系,对肿瘤距两端切缘较远者,也可横向取两端切缘。单独送检的闭合器切缘应剔除闭合器后全部取材观察。对肿瘤侵犯最深处及可疑环周切缘受累处应重点取材。推荐使用墨汁或碳素墨水标记环周切缘。
对早期食管癌或新辅助治疗后病变不明显的根治术标本,建议将可疑病变区和瘤床全部取材。
对周围黏膜糜烂、粗糙或碘不染色等改变的区域或周围食管/胃壁内结节及食管胃交界部组织应分别取材。送检的分组淋巴结应全部包埋取材。若附纵隔胸膜、肺和膈肌等其他邻近器官应观察取材。
推荐取材组织大小不大于2.0cm×1.5cm×0.3cm。
标准的二野或三野清扫且未经新辅助治疗的根治术标本应检出12枚以上淋巴结。
6.病理报告内容及规范
食管癌的病理报告应包括与患者治疗和预后相关的所有内容,如标本类型、肿瘤部位、大体分型、大小及数目、组织学类型、亚型及分级、浸润深度、脉管和神经侵犯、壁内转移、周围黏膜情况、淋巴结情况、环周及两端切缘情况等。推荐报告最后注明pTNM分期。
(1)大体描写:包括标本类型、肿瘤部位、大体分型、大小(肿瘤大小应量出三维的尺寸)及数目。
(2)主体肿瘤:组织学类型、亚型及分级(见附录B)、浸润深度(包括黏膜固有层、黏膜肌层、黏膜下层、浅肌层、深肌层、纤维膜及周围组织或器官)。对于黏膜下层浸润癌,如为内镜下切除标本,应测量黏膜下层浸润深度,建议区分SM1(黏膜下层侵犯深度<200μm)和SM2(黏膜下层侵犯深度>200μm);如为外科根治术标本,建议区分SM1(黏膜下层上1/3)、SM2(黏膜下层中1/3)和SM3(黏膜下层下1/3),切缘(内镜下切除标本包括侧切缘和基底切缘,根治切除标本包括口侧、肛侧切缘及环周切缘)(切缘的情况要说明,包括:浸润癌或上皮内瘤变/异型增生或巴雷特食管或巴雷特食管伴上皮内瘤变/异型增生,建议注明距切缘的距离,根治切除标本建议采用0、0~0.1cm及≥0.1cm注明距环周切缘的距离),淋巴管/血管浸润(尤其是对于内镜下切除标本,如果怀疑有淋巴管/血管浸润,建议做免疫组化CD31、D2-40确定是否有淋巴管/血管浸润,EVG染色判断有无静脉侵犯),神经侵犯,壁内转移。
(3)癌旁:上皮内瘤变/异型增生及程度、巴雷特食管,有无食管炎、胃炎及类型。
(4)淋巴结转移情况:转移淋巴结数/淋巴结总数。宜报告转移癌侵及淋巴结被膜外的数目。
(5)治疗反应(新辅助治疗的病例)。
(6)应报告合并的其他病变。
(7)食管胃交界腺癌应做HER2免疫组化检测及错配修复蛋白(MLH1、PMS2、MSH2、MSH6)免疫组化检测和(或)MSI检测。
(8)备注报告内容包括重要的相关病史(如相关肿瘤史和新辅助治疗史)。
(9)pTNM分期(附录C)。
四、食管癌的治疗规范
(一)治疗原则
临床上建议采取个体化综合治疗的原则,即根据患者的机体状况,肿瘤的病理类型、侵犯范围(病期)和发展趋向,有计划地、合理地应用现有的治疗手段,以期最大幅度地根治、控制肿瘤和提高治愈率,改善患者的生活质量。对拟行放疗、化疗的患者,应做KPS或ECOG评分(附录H)。
(二)手术治疗
外科手术治疗是食管癌的主要根治性手段之一,在早期阶段外科手术治疗可以达到根治的目的,在中晚期阶段,通过以手术为主的综合治疗可以使其中一部分患者达到根治,其他患者生命得以延长。目前我国手术入路存在左胸和右胸2种入路,在2000年以前我国食管癌外科治疗的主要入路以左胸入路为主,由于左胸主动脉弓遮挡和弓上三角狭小导致上纵隔淋巴结清扫不完全,因此,食管癌左胸入路治疗后下颈和上纵隔淋巴结复发率高达30%~40%,严重影响长期生存。导致我国以左胸入路外科治疗食管癌术后5年生存率近30年来一直徘徊在30%~40%。随着近年我国食管癌规范化巡讲的开展和食管癌胸腹腔镜微创手术的推广应用,右胸入路逐渐增多,但我国北方地区仍有较多医院继续开展左胸入路治疗食管癌。目前左右胸比例约各占50%。右胸入路由于没有主动脉弓的遮挡,有利于胸部淋巴结的完全清扫,腹部游离胃时为平躺体位,因此,也有利于腹部淋巴结的清扫。目前我国小部分医院已常规开展颈胸腹三野淋巴结清扫。大部分医院颈部淋巴结清扫为选择性。相比较左胸入路,经右胸入路行完全胸腹二野或颈胸腹三野淋巴结清扫能降低术后颈部和胸部淋巴结转移复发率,可提高5年生存率约10%,使术后总体5年生存率提高至50%左右。以手术为主的综合治疗主要为术前新辅助和术后辅助治疗,术前新辅助主要为化疗、放疗及放化疗,依据文献报道,术前放化疗优于术前化疗或放疗,因此,对于术前手术切除有困难或有2个以上淋巴结转移胸段食管癌患者(T3~T4aN0~2M0),目前我国大部分医院采用术前放化疗,小部分医院采用化疗或放疗为主。术前新辅助治疗后如果有降期,通常在6~8周后给予手术治疗。不降期者给予继续放化疗或手术治疗。术后辅助治疗主要为化疗或放疗,或放疗+化疗。主要对未能完全手术切除的患者或有高危因素的食管癌患者,包括姑息切除,淋巴结阳性,有脉管瘤栓,低分化等患者,术后可适当给予术后化疗/放疗。
1.手术治疗原则
(1)完善术前所有相关检查,并做好术前患者状况和病变期别评估(cTNM)。术前必须完成胃镜,腔内超声(推荐),病理或细胞学检查,颈、胸、腹部高清加强薄层CT,颈部超声,上消化道造影,肺功能,心电图,PET-CT(选择性),营养风险筛查和营养状况评估(推荐),血常规,尿常规,肝肾功能全项,肝炎、梅毒及艾滋病抗原抗体,出凝血功能等,以便于制订全面、合理和个体化的治疗方案。术前要依据高清薄层加强颈胸腹部CT或PET-CT和EUS评估T和N分期,结合脑MRI/CT及全身骨核素扫描或PET-CT评估M分期。
(2)术前风险评估
①心血管功能评估:心功能Ⅰ~Ⅱ级,日常活动无异常的患者,可耐受食管癌手术,否则需进一步检查及治疗。患者若有心肌梗死、脑梗死病史,一般在治疗后3~6个月手术比较安全,抗凝药如阿司匹林和波立维等应至少在术前一周停服。术前发现心胸比>0.55,左室射血分数<0.4,需治疗纠正后再评估。对于轻中度高血压的患者,经药物治疗控制可,手术风险较小,降压药物可口服至术晨。对于既往有器质性心脏病患者、心肌梗死患者建议行超声心动图检查,有严重心动过速、房室传导阻滞、窦房结综合征等严重心律失常的患者,建议行24小时动态心电图检查和相应药物治疗后再手术。
②肺功能评估:肺功能正常或轻中度异常(VC%>60%、FEV1>1.2L、FEV1%>40%、DLco>40%),可耐受食管癌手术,但中度异常者,术后较难承受肺部并发症的发生。必要时可行运动心肺功能检查或爬楼试验做进一步检测,食管癌开胸手术一般要求前者VO2max>15ml/(kg·min),后者要求患者连续爬楼3层以上。
③肝肾功能评估:肝功能评估参照Child-Pugh分级评分表,积分5~6分,手术风险小;8~9分,手术风险中等;>10分时,手术风险大。肾功能评估主要参考术前尿常规、血尿素氮、血肌酐水平,轻度肾功能受损者可耐受食管手术,中重度受损者建议专科医师会诊。食管癌手术一般对肝肾功能无直接损伤,但是围手术期用药、失血、低血压可影响肝肾脏器,当此类因素存在时应注意术后监测。
④营养状况评估:中晚期食管癌患者常合并吞咽困难,部分患者有营养不良、消瘦、脱水表现,术前应注意患者的近期体重变化及白蛋白水平,体重下降>5kg常提示预后不良;白蛋白<30g/L,提示术后吻合口瘘风险增加。若无需紧急手术,则应通过静脉高营养和鼻饲胃肠营养改善患者营养状况后再行手术治疗。以减少术后相关并发症。
(3)由胸外科外科医师决定手术切除的可能性和制订及实施手术方案:根据患者的病情、合并症、肿瘤的部位和期别以及术者的技术能力决定手术入路选择和手术方式。尽量做到肿瘤和区域淋巴结的完全性切除。
(4)手术入路选择
左胸入路:依据文献报道,对于胸中下段食管癌,右胸入路淋巴结清扫和预后要好于左胸入路。因此推荐选择右胸入路行食管癌的根治性手术治疗,即右胸-上腹二切口食管癌根治术(IVOR-LEWIS术式)。但国内文献报道回顾性分析结果显示,上纵隔无淋巴结转移的患者无论经左胸入路或右胸入路,术后生存及复发无显著性差异,因此,上纵隔无淋巴结转移的早中期胸中下段食管癌目前仍可以选择左胸一切口或两切口入路,即左胸一切口食管癌根治术(Sweet术式)。
右胸入路:对于伴有上纵隔淋巴结转移的胸段食管癌患者,应选择右胸入路两切口或三切口手术。行完全胸腹二野淋巴结清扫或颈胸腹三野淋巴结清扫,即左颈-右胸-上腹正中三切口食管癌根治术(McKeown术式)。
经膈肌裂孔入路:经颈部及膈肌裂孔食管切除术(transhiatal esophagectomy,THE)主要适用于食管肿瘤无明显外侵和纵隔无明显转移肿大淋巴结的偏早期患者。尤其是高龄或心肺功能不全等不适宜开胸手术的患者。既往应用术式为食管拔脱术,该手术虽创伤小,心肺功能损失少,有利于术后恢复,但胸腔内操作无法在直视下进行,有气管损伤、后纵隔出血等风险;且该径路不能清扫胸腔内淋巴结,目前在国内已不作为食管癌根治的基本术式,随着胸腹腔镜食管癌根治术的开展,目前已有少数医师尝试应用胸、腹腔镜辅助行不开胸的食管癌根治术,基本代替了既往的食管拔脱术,并可以清扫纵隔淋巴结,但手术过程复杂,初期费时费力,但患者术后恢复快。其适应证目前为高龄或心肺功能不全等不适宜开胸手术的早期食管癌患者,但仍需进一步探索和拓展。
(5)手术方式选择:常规开胸或胸腹腔镜辅助食管癌切除加淋巴结清扫是目前常规的手术方法。随着胸腹腔镜手术的逐渐流行,胸腹腔镜手术与常规开胸手术相比可以减少手术并发症,尤其是呼吸道并发症。回顾性研究显示预后略好于经右胸开放性食管癌根治术,因此,对于适合胸腔镜手术切除患者(T1~3N0~1M0),目前,推荐经右胸胸腹腔镜食管癌根治术。对于经放化疗降期的患者,优先推荐经右胸胸腹腔镜食管癌根治术,以减少术后心肺相关并发症。但不同级别医院应根据当地医疗设备条件和技术能力及医师的经验选择合适手术方式。
(6)淋巴结清扫
参考ISDE、JSED食管癌淋巴结的分组和命名法,新的食管区域淋巴结分组及命名见图2。
颈部淋巴结:左侧颈部喉返神经旁,右侧颈部喉返神经旁,左侧颈深下组,右侧颈深下组,左侧锁骨上,右侧锁骨上。
胸部淋巴结:根据2017年中国抗癌协会食管癌专业委员会制定的食管癌胸部淋巴结分组中国标准如下。
C201组:右侧喉返神经旁淋巴结(右侧迷走神经折返起始部至右侧锁骨下动脉末端之间右侧喉返神经周围淋巴结及脂肪组织)。
C202组:左侧喉返神经旁淋巴结(气管上1/3 左侧缘,主动脉弓上缘的左侧喉返神经周围淋巴结及脂肪组织)。
C203组:胸上段食管旁淋巴结(从肺尖至奇静脉弓下缘之间气管前后淋巴结)。
C204组:气管旁淋巴结(右侧迷走神经旁至食管旁,气管右侧面淋巴结)。
C205组:隆突下淋巴结(位于气管与左、右主气管分叉下的淋巴结)。
C206组:胸中段食管旁淋巴结(气管分叉至下肺静脉下缘间食管周围淋巴结)。
C207组:胸下段食管旁淋巴结(下肺静脉下缘至食管胃结合部间食管旁淋巴结)。
C208组:下肺韧带淋巴结(紧贴右下肺静脉下缘,下肺韧带内的淋巴结)。
C209组:膈肌旁淋巴结(右侧心膈角淋巴结)。
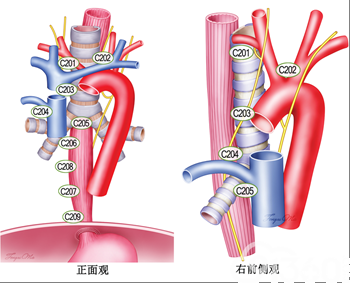
图2 食管癌胸部淋巴结分组中国标准示意图
注:“C”表示中国标准,“2”表示胸部淋巴结;C201组:右侧喉返神经旁淋巴结;C202组:左侧喉返神经旁淋巴结;C203 组:胸上段食管旁淋巴结;C204组:气管旁淋巴结;C205组:隆突下淋巴结;C206组:胸中段食管旁淋巴结;C207组:胸下段食管旁淋巴结;C208组:下肺韧带淋巴结;C209组:膈肌旁淋巴结
腹部淋巴结:贲门旁,胃左动脉旁及胃小弯旁,腹腔动脉干旁,脾动脉干旁,肝总动脉干旁。
依据文献报道,颈胸腹三野淋巴结清扫预后要好于二野淋巴结清扫,但三野清扫后术式并发症增加,尤其是喉返神经麻痹和吻合口瘘及吸入性肺炎等,因此,食管癌完全性切除手术应常规进行完全胸腹二野淋巴结清扫,并标明淋巴结清扫位置并送送病理学检查,为达到根治和进行准确的分期,推荐胸腹二野最少清扫15个淋巴结以上。胸、腹二野淋巴结清扫区域应包括以下食管淋巴结引流区,胸部:双侧喉返神经旁(双侧气管食管沟),胸上段食管旁,胸中段食管旁,胸下段食管旁,隆凸下及左主支气管旁;下肺韧带,膈肌裂孔旁。腹部:贲门旁,胃小弯旁,胃左动脉旁,腹腔动脉干旁,肝总动脉旁及脾动脉干旁。
为避免增加术后并发症和延缓患者康复,目前颈部淋巴结清扫推荐为选择性,胸中下段食管癌患者应依据术前颈部CT和超声等检查结果或术中双侧喉返神经旁淋巴结冰冻检查结果决定是否需要行颈部淋巴结清扫。若术前怀疑有颈部淋巴结转移或术中冰冻阳性推荐行颈部淋巴结清扫。上段食管癌推荐行颈部淋巴结清扫。颈部淋巴结清扫包括颈内侧的左右下颈内侧喉返神经旁和颈深淋巴结及左右颈外侧锁骨上淋巴结。具体清扫范围见图3。
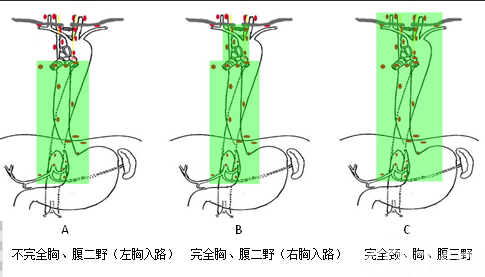
图3 不同术式淋巴结清扫范围
(7)替代器官:胃是最常替代食管的器官,通常制作成管状胃来替代食管和重建消化道。其次可依据患者情况以选择结肠和空肠。
(8)替代器官途径:通常选择食管床,也可选择胸骨后或皮下隧道。为术后放疗提供空间。
文献报道食管癌手术数量(volume)是影响食管癌术后的并发症和病死率的重要因素,推荐接受胸外科专科医师培训和在大的食管癌诊治中心培训的医师进行食管癌切除手术。
2.手术适应证
(1)UICC/AJCC分期(第8版)中的T1aN0M0期主要治疗以内镜下黏膜切除和黏膜剥离术为主,详见早期食管癌治疗。T1b~3N0~1M0期患者适合首选手术治疗。T3~4aN1~2M0期别患者可选择先行术前辅助放化疗或化疗或放疗,术前辅助治疗结束后再评估是否可以手术治疗。任何T4b或N3或M1期患者一般推荐行根治性放化疗而非手术治疗(图4)。
(2)食管癌放疗后复发,无远处转移,术前评估可切除,一般情况能耐受手术者。
3.手术禁忌证
①一般状况和营养状况很差,呈恶液质样;②病变严重外侵(T4b),UICC/AJCC分期(第8版)中T4b病变,侵犯心脏、大血管、气管和邻近器官如肝、胰腺、脾等;多野和多个淋巴结转移(N3),全身其他器官转移(M1);③心肺肝脑肾重要脏器有严重功能不全者,如合并低肺功能,心力衰竭、半年以内的心肌梗死、严重肝硬化、严重肾功能不全等。
4.围手术期的药物管理
需行手术治疗的患者,若合并下列情况之一: 6个月内体重丢失10%~15%,或BMI<18.5kg/m2,或PG-SGA达到C级,或无肝功能不全患者的血清白蛋白<30g/L,营养治疗可以改善患者的临床结局(降低感染率,缩短住院时间)。这些患者应在术前给予营养治疗10~14天,即使手术因此而推迟也是值得的。该条意见中营养治疗系指肠内营养。
5.手术治疗后随访
对于术后食管癌患者,第1~2年内推荐每3个月随访1次,第3~5年每6个月随访1次,此后每年随访1次;随访内容包括病史询问和体检,根据临床情况决定行血常规、血液生化(肝肾功能、蛋白、肿瘤标志物等)、内镜和上消化道造影及CT等影像学检查。如怀疑有复发转移依据病情推荐行PET-CT、MRI及骨扫描等检查,并及时转放疗及化疗。
(三)放射治疗
放射治疗是食管癌综合治疗的重要组成部分。我国70%的食管癌患者就诊时已属中晚期,失去根治性手术切除的机会;而我国食管癌病理95%以上均为鳞状细胞癌,对放射线相对敏感。此时,就需要术前放疗联合手术或根治性放化疗的综合治疗模式来改善患者生存。可手术食管癌,经术前放疗后,5年生存率可由33%提高至47%。不可手术食管癌,也在应用先进的调强放疗技术和同步放化疗后,5年生存率从单纯放疗时代的5%提高到现在的15%~20%。因此,目前对于中、晚期的可手术、不可手术或拒绝手术的食管癌,术前同步放化疗联合手术或根治性同步放化疗是重要的治疗原则。
1.食管癌放疗适应证
当患者不能耐受同步放化疗时可行单纯放疗。
(1)术前新辅助放疗/同步放化疗:能耐受手术的T3~4N+ M0
备注:不可手术食管癌术前放疗后如转化为可手术,建议手术切除。如仍不可手术,则继续行根治性放疗。
(2)术后辅助放疗/同步放化疗
①R1(包括环周切缘+)或R2切除。
②R0切除,鳞癌,病理分期N+,或T4aN0,淋巴结被膜受侵;腺癌,病理分期N+,或T3~4aN0,或T2N0中具有高危因素(低分化,脉管瘤栓,神经侵犯,<50岁)的下段或食管胃交界癌建议术后放疗或同步放化疗。目前并无循证医学证据明确术后放化疗的治疗顺序。一般建议R1或R2切除后,先进行术后放疗或同步放化疗,再进行化疗。R0切除术后,鳞癌建议先进行术后放疗或同步放化疗,再进行化疗;腺癌建议先化疗后再进行放疗或同步放化疗。
(3)根治性放疗/同步放化疗
①T4bN0~3。
②颈段食管癌或颈胸交界癌距环咽肌<5cm。
③经术前放疗后评估仍然不可手术切除。
④存在手术禁忌证。
⑤手术风险大,如高龄、严重心肺疾患等。
⑥患者拒绝手术。
(4)姑息性放疗
①术后局部区域复发(术前未行放疗)。
②较为广泛的多站淋巴结转移。
③骨转移、脑转移等远地转移病变,缓解临床症状。
④晚期病变化疗后转移灶缩小或稳定,可考虑原发灶放疗。
⑤晚期病变解决食管梗阻,改善营养状况。
⑥缓解转移淋巴结压迫造成的临床症状。
2.放疗前相关检查评估
建议放疗前2周内完成。
①胃镜、腔内超声(颈段食管癌需行下咽喉镜检查)。
②病理或细胞学检查。
③颈胸、腹部CT,颈部超声。
④上消化道造影。
⑤肺功能。
⑥心电图。
⑦PET-CT(选择性)。
⑧食管MRI(选择性)。
⑨营养风险筛查和营养评定。
⑩实验室检查:包括血常规,尿常规,便常规,肝肾全项等。
3.放疗方案制订规范
(1)放射治疗技术
建议采用三维适形放疗或调强放疗技术。已有多个放射物理方面的研究表明,相较于早年的常规二维放疗技术,三维适形或调强放疗在靶区剂量分布和正常组织器官保护等方面均表现优异,特别是对于心脏和肺的保护,可降低放疗相关不良反应。
(2)CT模拟定位
采取仰卧位,双臂伸直置于体侧或者双肘交替后置于额前。颈段及上段患者建议头颈肩罩固定,中下段及食管胃交界癌体膜固定。食管下段或食管胃交界癌,由于食管肿瘤受到呼吸和心脏等器官运动影响较大,可采用四维模拟CT(4D-CT)定位,观察肿瘤实际运动偏移程度,提高放疗精度。行静脉造影增强扫描,层厚0.5cm。对对比剂过敏者可不行增强扫描。
如果原发灶为早期,不能明确从影像检查确定病变长度,则需要在胃镜下放置银夹标记后再定位。因银夹固定较差易脱落,胃镜标记后需要尽快模拟定位。
食管下段及食管胃交界癌,或者需要照射胃左、腹腔淋巴结的患者,为了减少胃部充盈大小造成的照射体积差异,CT模拟定位前空腹3~4小时,CT扫描前及每次放疗前15分钟,患者需服用200~300ml半流食(如稠粥、酸奶等,每次定量)。上中段患者无需此步骤。
术后残胃位于纵隔的患者,不要充盈胃,以胃内无内容物时定位为佳,放疗时亦如此。
(3)靶区定义
A.术前新辅助放疗/同步放化疗或根治性放疗/同步放化疗
①GTV和GTVnd
结合各项检查可见的食管原发肿瘤为GTV,确诊转移或不能除外转移的淋巴结为GTVnd。放置银夹标记后,GTV以银夹标记的上下界为准。
②CTV
颈段/上段:GTV上下放3~5cm,或GTVnd上下放0.5~1cm,以最高(低)为界。一般需包括1(下颈、双侧锁骨上)、2、4、7淋巴结引流区。
中段:GTV上下放3cm,或GTVnd上下放0.5~1cm,以最高(低)为界。一般需包括1(下颈、双侧锁骨上)、2、4、7、部分8淋巴结引流区。
下段/SiewertⅠ/SiewertⅡ型:GTV上下放3~5cm,或GTVnd上下放0.5~1cm,以最高(低)为界。一般需包括7、部分8、贲门、胃左、腹腔干淋巴引流区。
注:GTV上、下外放3cm还是5cm,如果3cm以外没有肿大淋巴结,则建议外放3cm;如在3~5cm范围内有转移淋巴结或可疑转移淋巴结,可外放5cm。若5cm以外还有淋巴结,可考虑累及野照射。
③PTV
在CTV的基础上外放0.5cm形成,头颈肩网罩固定的颈段或上段食管癌可外放0.3cm。
④PGTV(采用序贯或同步加量时)
GTV+GTVnd外放0.5cm。
B. 术后辅助放疗/同步放化疗
术后残胃位于纵隔内(术后放疗照射野)的患者,因残胃对放疗耐受性差,除肿瘤有明显残留(R1/2切除)外,不建议积极的预防放疗。当残胃位于左侧或右侧胸腔内,且符合术后放疗适应证时,可行纵隔淋巴结引流区的预防性放疗。
需包括吻合口情况:原发于颈段或上段食管癌,或切缘距肿瘤≤3cm。
①GTV和GTVnd
R1或R2切除后,残留的原发肿瘤、切缘阳性的吻合口、残留的淋巴结或可疑淋巴结为GTV或GTVnd。
②CTV
颈段/上段:包括GTV+GTVnd(如有),吻合口、1(下颈、双侧锁骨上)、2、4、7淋巴结引流区。颈段可酌情不包括7区。
中段:包括GTV+GTVnd(如有),1(下颈、双侧锁骨上)、2、4、7、部分8淋巴结引流区。T4b需包括瘤床。
下段食管癌/ SiewertⅠ/SiewertⅡ型:包括GTV+GTVnd(如有),1(下颈、双侧锁骨上)、2、4、7、8、贲门、胃左、腹腔干淋巴结引流区。T4b需包括瘤床。
③PTV
在CTV的基础上外放0.5cm形成,头颈肩网罩固定的颈段或上段食管癌可外放0.3cm。
④PGTV(有肿瘤或淋巴结残存需序贯或同步加量时)
GTV+GTVnd外放0.5cm。
4.处方剂量
(1)术前新辅助放疗/同步放化疗
95% PTV 41.4~50Gy/1.8~2.0Gy,每日1次,每周5次。有条件的单位也可采用同步加量技术。
(2)术后辅助放疗/同步放化疗
①R0术后:95% PTV 50~56Gy/1.8~2.0Gy,每日1次,每周5次。
②R1/2术后:95% PTV 50Gy/1.8~2.0Gy,序贯95% PGTV 10~14Gy/1.8~2.0Gy,每日1次,每周5次。有条件的单位也可采用同步加量技术。
(3)根治性放疗/同步放化疗
①95% PTV 60~64Gy/1.8~2.0Gy,每日1次,每周5次。
②95% PTV 50Gy/1.8~2.0Gy,序贯95% PGTV 10~14Gy/1.8~2.0Gy,每日1次,每周5次。有条件的单位也可采用同步加量技术。
5.正常组织限量
对于术后或术前放疗的患者,建议先按足量处方剂量(如95% PTV 60Gy)进行正常组织评估,再按实际处方剂量执行,同时确定正常组织的实际受量。
(1)双肺:平均剂量14~16Gy,V5≤60%,V20=30%,V30≤20%。同步放化疗者V20≤28%。
(2)心脏:V30≤40%,V40≤30%。
(3)脊髓PRV:Dmax≤45Gy。
(4)胃:V40≤40%,Dmax 55~60Gy。
(5)小肠:V40≤40%,Dmax≤55Gy。
(6)双肾:V20≤30%。
(7)肝:V30≤30%。
6.同步化疗方案
(1)紫杉醇+铂类
紫杉醇 45~60mg/m2,d1。
卡铂AUC 2,d1(或联合奈达铂20~25 mg/m2,d1;或联合顺铂20~25 mg/m2,d1),7天1个周期,共5~6个周期。
(2)顺铂+5-FU或卡培他滨或替吉奥
由于卡培他滨或替吉奥疗效与5-FU相似或更优,不良反应较轻,且口服方便,可代替5-FU。
顺铂 30mg/m2,d1。
卡培他滨 800mg/m2,bid,d1~5(或替吉奥 40~60mg/m2,bid,d1~5),7天1个周期,共5~6个周期。
(3)紫杉醇+5-FU或卡培他滨或替吉奥
紫杉醇 45~60mg/m2,d1。
卡培他滨625~825mg/m2,bid,d1~5(或替吉奥 40~60mg/m2,bid,d1~5),7天1个周期,共5~6个周期。
(4)奥沙利铂+5-FU或卡培他滨或替吉奥
奥沙利铂85mg/m2,d1、15、29。
卡培他滨 625mg/m2,bid,d1~5(或替吉奥 40~-60mg/m2,bid,d1~5),7天1个周期,共5~6个周期。
疗效评估详见附录F。
7.放疗相关并发症防治
(1)营养不良
食管癌的营养不良发生率居所有恶性肿瘤第一位,达60%~85%。主要原因为进食梗阻和基础代谢率增加。而放化疗期间因患者会产生不同程度的放疗反应,如放射性食管炎、食欲不振、反酸等,造成患者营养不良进一步加重。营养支持治疗可以明显改善患者的营养不良状态,有利于提高放化疗的完成率,进而提高肿瘤控制率;还能帮助患者尽快度过不良反应恢复期,缩短肿瘤治疗间歇期。
①营养评估与评定
经过营养筛查与评估后,进行营养评定,综合了解营养不良类型,选择个体化营养支持方案。营养不良的治疗模式主要包括营养教育、肠内营养和肠外营养。临床建议优先使用肠内营养。根据食管癌放疗肠内营养专家共识,进行肠内营养支持的主要适应证有:1个月体重下降5%以上,BMI<18.5kg/m2,患者主观整体评分(PG-SGA)≥4分,摄食量少于正常需要量的60%且持续3~5天以上。
②肠内营养支持
患者进行放疗前,如符合肠内营养支持情况之一或预计放疗期间可能有较大营养风险的患者,建议放疗前即开始接受营养治疗(鼻饲或胃造瘘,胃造瘘不适用于可手术患者),并持续到放化疗后1~2周,个别恢复较慢的患者可能需要到放化疗后1~2个月。对因营养状态较差而预计可能不能耐受放疗的患者,放疗前营养支持治疗建议至少1~2周,待营养状态改善后再行治疗。一般推荐能量供给量为25~30kcal/(kg·d)。
(2)食管穿孔
食管穿孔是食管癌最常见的严重并发症之一,可能发生在放疗前、放疗中或放疗后。肖泽芬报道食管癌一旦出现穿孔,62%在3个月内死亡,82%在半年内死亡。主要的穿孔原因,首先是肿瘤自身生长外侵,突破纤维膜后造成。其次与肿瘤对放疗敏感有关,肿瘤消退过快,合并感染,影响正常组织修复能力,造成退缩性穿孔,此时的穿孔分为癌性穿孔和无癌性穿孔。其中无癌性穿孔占比约为20%~30%。预后明显好于癌性穿孔。
①临床表现
穿孔前的临床表现多有发热、胸背部疼痛或不适、实验室炎性指标升高等。一旦穿孔,胸背痛消失,并可能伴有饮水呛咳。
②处理
放疗前食管造影显示有毛刺、龛影等穿孔征象时,建议抗感染治疗,同时加强营养,每次进食后饮清水冲刷食管,避免食物残留,还可口服庆大霉素。放疗期间,每周进行食管造影,有利于早期发现穿孔。食管穿孔后停止放化疗,同时禁食水、静脉抗炎、抑酸、置鼻饲管或胃造瘘,补充蛋白等。根据食管穿孔的部位酌情置入食管支架。
穿孔并非放疗的绝对禁忌证,非癌性穿孔、食管纵隔瘘孔较小的患者,在后期静脉抗炎有效,营养改善的情况下,穿孔可能愈合。愈合后可继续放疗。
(3)放射性食管炎
放疗期间(一般20Gy左右开始)多数患者会出现放射性食管炎,主要表现为吞咽疼痛、进食梗阻感加重(放疗性食管炎评估见附录G)。如果不影响每日进食量可观察,进软食、半流食等,多饮水;中重度疼痛影响进食,可给与静脉补液、抗炎、激素对症处理。溃疡不明显者可给与镇痛药物或贴剂。
(4)气道反应
气管受到放射线照射时可能产生气道反应,多表现为刺激性干咳,夜间加重。但咳嗽的原因较多,上呼吸道感染、食管反流等均可能造成咳嗽。一般给与雾化吸入治疗效果较好,可一日数次,每次15~20分钟。雾化液可加入氨溴索、异丙托溴铵、糜蛋白酶、少量激素等。
(5)食管梗阻
放疗期间因食管局部水肿,可能出现梗阻加重的情况,表现为唾液增多,进食困难。已置入鼻饲管或胃造瘘患者不用特殊处理。无管饲的患者,可静脉营养支持,口服流质营养餐,或临时置入鼻饲管,以保证每日能量摄入。抗生素和激素有助于缓解水肿。一般放疗至40Gy左右梗阻可缓解。
放疗后出现的梗阻,首先明确是否为肿瘤复发,胃镜检查排除肿瘤复发后,则考虑食管壁的放疗纤维化造成的局部管腔狭窄。为了解决进食问题,可行内镜下食管扩张。
8.放疗后随访
(1)术前放疗后随访
术前放疗后建议休息1个月左右,复查CT,消化道造影,超声,胃镜,实验室各项指标等术前检查。手术建议在放疗结束后6~8周进行。
(2)术后放疗后随访
术后放疗结束后,2年内3个月复查1次,2~5年半年复查1次,5年以后每年复查1次。CT、消化道造影、超声、胃镜、实验室各项检查为常规项目。PET-CT、骨扫描、脑磁共振等为选择性检查。
(3)根治性放疗后随访
根治性放疗后建议休息1~2个月,复查CT、消化道造影、超声、实验室各项检查。胃镜、PET-CT、骨扫描、脑磁共振等可在其他影像学检查发现有问题或者患者出现相应部位症状时选择进行。
(四)药物治疗
早期食管癌的临床症状不明显,难于发现;大多数食管癌患者在确诊时已为局部晚期或存在远处转移。因此,以控制播散为目的的化疗在食管癌的治疗中占有重要的地位。近年来,随着分子靶向治疗、免疫治疗新药的不断发现,药物治疗在食管癌综合治疗中的作用前景广阔。
目前,药物治疗在食管癌中主要应用领域包括针对局部晚期患者的新辅助化疗和辅助化疗,以及针对晚期患者的化疗、分子靶向治疗和免疫治疗。
临床研究有可能在现有标准治疗基础上或失败后,给部分患者带来获益。鉴于食管癌的药物治疗在很多情形下缺乏标准方案,因此鼓励患者在自愿前提下参加与适宜的临床研究。食管是重要的消化器官,原发病灶的存在直接影响患者的营养状况,同时可能存在出血、消化道梗阻、穿孔等各种并发症,因此在整个抗肿瘤治疗过程中,需要特别关注患者营养状况的维持、并发症的积极预防和及时处理,尽量维持患者的生活质量。
1.食管癌化疗的适应证
(1)新辅助化疗
新辅助化疗有利于肿瘤降期、消灭全身微小转移灶,并观察肿瘤对该方案化疗的反应程度,指导术后治疗。对于食管鳞癌,由于目前新辅助化疗证据不足,建议行术前放化疗效果更佳。食管腺癌围手术期化疗的证据充足。对于可手术切除的食管下段及胃食管结合部腺癌患者,推荐行新辅助化疗,能够提高5年生存率,而不增加术后并发症和治疗相关死亡率。
(2)术后辅助化疗
食管鳞癌术后是否常规进行辅助化疗仍存在争议,尚未得到大型随机对照研究的支持。基于前瞻性Ⅱ期及回顾性临床研究的结果,对术后病理证实区域淋巴结转移(N+)的患者,可选择行2~3个周期术后辅助化疗。
食管腺癌术后辅助化疗的证据来自于围手术期化疗的相关研究,对于术前行新辅助化疗并完成根治性手术的患者,术后可沿用原方案行辅助化疗。
辅助化疗一般在术后4周以后开始。术后恢复良好、考虑行术后辅助化疗的患者可在术后4周完善化疗前检查并开始辅助化疗;如果患者术后恢复欠佳,可适当延迟辅助化疗,但不宜超过术后2个月。
(3)姑息性化疗
对转移性食管癌患者,如能耐受,推荐行化疗。转移性食管癌经全身治疗后出现疾病进展,可更换方案化疗。根治性治疗后出现局部复发或远处转移的患者,如能耐受,可行化疗。
2.化疗前相关检查评估
(1)评估肿瘤情况
通过病理和细胞学明确病理类型,通过病史、体格检查、影像学检查明确疾病的范围、发展趋向,以确定治疗目标。化疗前应视具体情况行胸腹部CT或颈胸部CT检查,留作基线片,方便化疗后对比疗效或长期随访。
(2)评估患者身体条件
患者应当一般状况良好,ECOG PS评分0~1分。详见附录H。
化疗开始前1周内行血常规、肝肾功能、心电图等检查。心、肝、肾和造血功能无明显异常。血常规中性粒细胞绝对值≥1.5×109/L、血小板≥80×109/L、HGB≥80g/L可考虑化疗。
(3)评估合并疾病情况
患者应无活动性消化道出血、胃肠梗阻、穿孔、栓塞、休克等严重并发症。若合并非肿瘤性发热,体温应<38℃。如患者合并心、肺或其他慢性内科疾病,可根据病情进行相关检查,如:心肌酶谱、24小时动态心电图、超声心动图、BNP、肺功能等。
3.常用化疗方案
(1)顺铂+5-FU
顺铂 75-100 mg/m? i.v. 输注4h d1
5-FU 750-1000 mg/m? i.v. 持续输注 d1-4
每3-4周重复
(2)紫杉醇+顺铂
紫杉醇 135-175 mg/m? i.v. 输注3h d1
顺铂 75 mg/m? i.v. d1
每3周重复
(3)紫杉醇+顺铂
紫杉醇 90-150 mg/m? i.v. 输注3h d1
顺铂 50 mg/m? i.v. d1
每2周重复
(4)表柔比星+顺铂+5-FU(ECF)
表柔比星 50 mg/m? i.v. 推注 d1
顺铂 60 mg/m? i.v. 推注 d1
5-FU 200 mg/m? i.v. 持续输注 d1-21
每3周重复,5-FU持续给药
(5)表柔比星+奥沙利铂+卡培他滨(EOX)
表柔比星 50 mg/m? i.v. 推注 d1
奥沙利铂 130 mg/m? i.v. 输注2h d1
卡培他滨 625 mg/m? bid.p.o. 每日 d1-21
每3周重复,卡培他滨持续口服
(6)奥沙利铂+亚叶酸钙+5-FU(FLO)
奥沙利铂 85 mg/m? i.v. 输注2h d1
亚叶酸钙 200 mg/m? i.v. 输注2h d1,之后用5-FU
5-FU 2600 mg/m? i.v. 输注24h d1
每2周重复
(7)多西他赛+顺铂+5-FU(改良的DCF方案)
多西他赛 60 mg/m? i.v. 输注1h d1
顺铂 60 mg/m? i.v. 输注1-3h d1
5-FU 750 mg/m? i.v. 持续输注 d1-4
每3周重复
(8)伊立替康+5-FU/亚叶酸钙
伊立替康 80 mg/m? i.v. 输注30min d1
亚叶酸钙 500 mg/m? i.v. 输注2h d1
5-FU 2000 mg/m? i.v. 输注22h d1
每周重复,连用6周后休2周
(9)伊立替康+5-FU/亚叶酸钙
伊立替康 180 mg/m? i.v. 输注30min d1
亚叶酸钙 125 mg/m? i.v. 输注15min d1
5-FU 400 mg/m? i.v. 推注22h d1
5-FU 1200 mg/m? i.v. 每日输注24h d1-2,
每2周重复
4.化疗后疗效评估
详见附录F。
5.化疗相关不良反应的防治
化疗期间应根据化疗方案的不良反应特点,定期进行实验室检查,必要时应给予相应的对症支持治疗。化疗后骨髓抑制、胃肠道反应、肝肾功能损害是相对常见的不良反应。
(1)骨髓抑制
建议患者于化疗后每周复查1~2次血常规。根据具体化疗方案及患者血象变化的特点,复查时间间隔可酌情增减。若出现3、4度白细胞或中性粒细胞降低应停药,对症给予粒细胞集落刺激因子(G-CSF)治疗,并视具体情况延迟或减量下一周期化疗。当血小板<50×109/L时应给予白介素11(IL-11)或重组人血小板生成素(TPO)等药物治疗,酌情使用止血药物。根据患者的血象结果和化疗方案的特点,也可预防性使用上述升白细胞及升血小板药物。
(2)胃肠道反应
化疗相关恶心呕吐:可发生于化疗后数小时或数天。可单独或联合应用5-HT3受体拮抗剂类、糖皮质激素及神经激肽-1受体拮抗剂等药物。甲氧氯普胺与苯海拉明连用,可提高止吐作用且可控制锥体外系不良反应。应注意对症纠正严重呕吐造成水电解质紊乱。
食欲下降:尤其是术后患者,手术改变造成消化系统异常,故化疗时更要注意营养支持。可以口服营养制剂和增强食欲的药物,如甲地孕酮等。或者放置胃或空肠营养管并通过营养管进行营养支持,必要时应静脉营养支持。
腹泻:应注意避免进食寒凉和粗纤维丰富的食物,及时服用止泻药。腹泻超过每日5次或出现血性腹泻应停止化疗,并注意足量补液及纠正水电解质紊乱。
(3)肝、肾功能损害
化疗前应了解患者有无肝炎病史。建议每化疗周期复查1次肝肾功能。一旦出现肝功能损害,应当全面评估肝功能,并予以保肝药物治疗。肾功能不全者禁用有肾毒性的药物,在使用肾毒性药物,如顺铂时,应注意足量水化,且需要注意药物间的相互作用。
(4)神经系统毒性
应用奥沙利铂等药物前,须告知患者避免接触寒冷物品,并给予营养神经药物。严重神经毒性应停药。
(5)过敏反应
使用糖皮质激素、H2受体拮抗剂、苯海拉明预处理可降低过敏反应发生的几率。使用易引起过敏的化疗药时,应在给药后2小时内密切观察患者的反应,一旦发生过敏,应立即停药,并予以肾上腺素、糖皮质激素、吸氧、升压药等抢救。
6.化疗后随访
(1)对于可手术切除、接受新辅助化疗的患者,应及时评估疗效。推荐每周期化疗前进行病史询问、体格检查;2~3周期后复查影像学。如病史、体格检查或影像学检查结果提示疾病进展,应终止化疗,并再次评估肿瘤的可切除性;对于可根治性切除的患者,应及时行手术治疗。
(2)对于根治性术后接受辅助化疗的患者,因无明确观察指标,推荐在完成既定的化疗后行影像学检查。如病情稳定,且无自觉症状,在治疗结束后的2年内,可每3~6个月进行随访,内容包括病史询问、体格检查、复查影像学,并根据临床需要复查血常规、血生化、消化内镜等。自第3年起,可每6~12个月进行随访,内容同上。自第6年起,可每年随访1次,内容同上。
(3)对于转移性食管癌接受姑息性化疗的患者,因中位缓解期短,推荐在完成既定的化疗后行影像学检查。如病情稳定,且无自觉症状,可每2个月进行随访,内容包括病史询问、体格检查、复查影像学,并根据临床需要复查血常规、血生化、消化内镜等。
7.分子靶向治疗和免疫治疗进展
根据现有的临床研究结果,分子靶向治疗和免疫治疗均应用于转移性食管癌的二线及以后的治疗,目前还未列入常规推荐。
(1)分子靶向治疗
EGFR-TKI类药物在转移性食管癌的二线治疗中的作用已有III期随机对照研究的结果。其无进展生存(PFS)较安慰剂略有延长,但两组的差别极小;而总生存(OS)则无显著差异。进一步的研究提示,EGFR基因扩增患者可能是EGFR-TKI类药物治疗的潜在获益人群。
EGFR单克隆抗体类药物联合化疗对比单纯化疗在转移性食管鳞癌和食管胃结合部腺癌中,均未观察到中位无进展生存(mPFS)和中位总生存(mOS)方面的显著获益,其在晚期食管癌中的应用还有待进一步探索。
(2)免疫检查点抑制剂治疗
近年来,国外有多项临床研究初步观察到免疫检查点抑制剂在转移性食管癌二线治疗中取得了令人鼓舞的疗效。在日本进行的KEYNOTE-028 研究纳入了23 例PD-L1 阳性的患者接受Pembrolizumab单药治疗,客观缓解率(ORR)达30%,其中PR 7 例,无CR 病例,SD 2例,PD 13 例。一项来自日本的单臂Ⅱ期研究报道了Nivolumab用于经氟尿嘧啶类/铂类/紫杉类药物治疗失败或不可耐受的晚期食管鳞癌患者的疗效和安全性,64 例可评估疗效的患者中,ORR为17%,其中1 例获得CR,中位PFS 和OS 分别为1.5个月和2.3个月。更多的免疫检查点抑制剂治疗晚期食管癌的相关研究尚在国内外开展中,有望在未来成为转移性食管癌二线治疗的有效选择。
8.对症支持治疗与姑息治疗
(1)营养支持
由于食管梗阻或肿瘤消耗,食管癌患者常合并营养不良。营养不良进而导致患者对抗肿瘤治疗的耐受性下降,影响疗效或增加并发症。因此,对于食管癌合并营养不良患者,临床中应积极给予营养支持治疗。
尚可进食患者,可给予口服配方营养素进行营养支持。食管梗阻患者,可内镜下放置食管支架,或留置空肠营养管行鼻饲。无法放置食管支架和留置空肠营养管鼻饲者,可酌情行胃造瘘术。
对于不能行上述肠内营养支持者,可行静脉(肠外)营养支持治疗。
(2)姑息治疗
姑息治疗理念应贯穿于包括所有食管癌分期患者。对食管癌患者的躯体、心理、社会和精神问题提供针对性治疗和(或)支持,以提高患者的生活质量。
食管癌的姑息治疗的内容主要包括:止痛、睡眠指导、心理沟通及终末期患者及家属的指导和教育等。
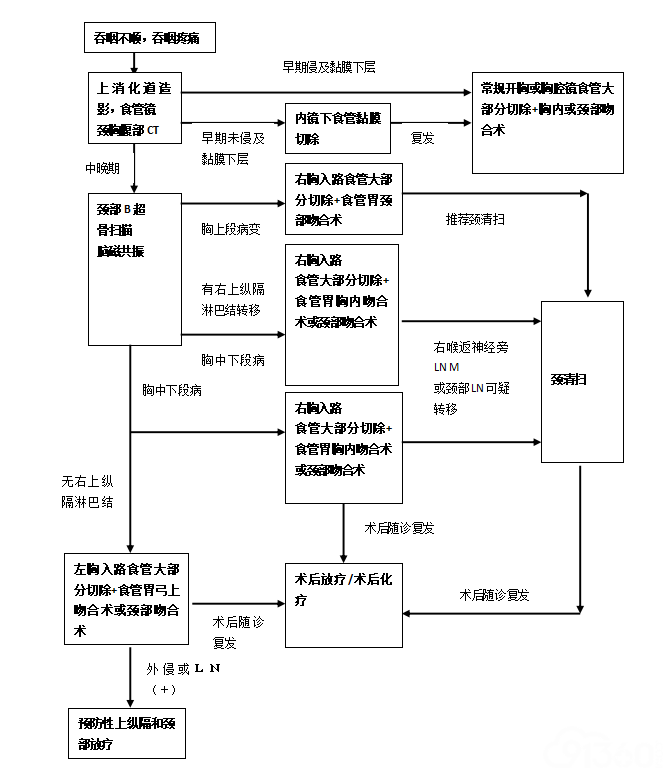
图4食管癌规范化诊疗流程图
(五)早期食管癌及癌前病变筛查和内镜治疗原则
早诊早治是提高食管癌诊治效果和患者生活质量及减轻国家与个人医疗负担的重要手段,因此,对于高危人群的定期筛查有助于发现癌前病变或早期食管癌以达到早诊早治的目的,阻止患者发展成为中晚期食管癌患者。
1.食管癌高危人群定义
食管癌的发病率随年龄增长而升高,40岁以下人群发病率较低,40岁以上年龄组占食管癌患者的99%因此,我国食管癌筛查常设定40岁为起始年龄,对于70岁以上人群是否需要继续进行食管癌筛查尚需要进一步研究。
根据我国国情和食管癌危险因素及流行病学,符合第1条和2~6条中任1条者应列为食管癌高危人群,建议作为筛查对象。
(1)年龄超过40岁。
(2)来自食管癌高发区。
(3)有上消化道症状。
(4)有食管癌家族史。
(5)患有食管癌前疾病或癌前病变者。
(6)有食管癌的其他高危因素(吸烟、重度饮酒、头颈部或呼吸道鳞癌等)。
2.筛查方法
(1)检查前准备
A.检查前患者应禁食≥6小时,禁水>2小时,有梗阻或者不全梗阻症状的患者应延长禁食、禁水时间。
B.检查前应取得知情同意,并向患者做好解释工作,消除患者的恐惧感,嘱其平静呼吸、不要吞咽唾液,避免不必要的恶心反应。
C.检查前10~20 分钟可给予患者黏液去除剂(如链酶蛋白酶)及去泡剂(如西甲硅油)口服,以清除上消化道内黏液与气泡,改善视野,提高微小病变的检出率。
D.检查前5 分钟给予1%盐酸达克罗宁胶浆或l%利多卡因胶浆5~10ml含服30秒,或咽部喷雾麻醉。有条件的单位可在麻醉师配合下使用静脉镇静或麻醉,可提高受检者内镜检查的接受度。
(2)内镜检查技术
A.普通白光内镜:食管黏膜病灶有以下几种状态:①红区,即边界清楚的红色灶区,底部平坦;②糜烂灶,多为边界清楚、稍凹陷的红色糜烂状病灶;③斑块,多为类白色、边界清楚、稍隆起的斑块状病灶;④结节,直径在1cm以内,隆起的表面黏膜粗糙或糜烂状的结节病灶;⑤黏膜粗糙,指局部黏膜粗糙不规则、无明确边界的状态;⑥局部黏膜上皮增厚的病灶,常遮盖其下的血管纹理,显示黏膜血管网紊乱、缺失或截断等特点。内镜医师应提高对上述形态特征的认识,在检查时注意观察黏膜的细微变化,对可疑病灶多点活检是提高早癌检出率的关键。然而,多数早期食管癌在普通内镜下表现不典型,可能会被漏诊,病灶范围亦不清晰,因而检查中结合色素或电子染色的方法进行观察有助于提高病变检出率。
B.色素内镜:将各种染料散布或喷洒在食管黏膜表面后,使病灶与正常黏膜在颜色上形成鲜明对比,更清晰的显示病灶范围,并指导指示性活检,以提高早期食管癌诊出率。色素内镜常用染料有碘液、甲苯胺蓝等,可单一染色,也可联合使用。
(a)碘染色:正常鳞状上皮细胞内富含糖原,遇碘可变成深棕色,而早癌及异型增生组织内糖原含量减少甚至消失,呈现不同程度的淡染或不染区。不染区的黄色程度从淡黄到深黄,取决于病灶的异型程度。根据病变着色深浅、范围大小及边缘形态,结合指示性活检,可提高高危人群早期鳞癌及异型增生的检出率。注意对碘过敏、甲亢患者不能使用该法。
(b)甲苯胺蓝染色:甲苯胺蓝为碱性染料,可与组织细胞的酸性物质相结合使之呈蓝色。因癌细胞增殖活跃,富含核酸物质,易被甲苯胺蓝染色,而正常细胞核内遗传物质相对较少,遇甲苯胺蓝着色不明显。与碘染色相比,甲苯胺蓝染色对操作技术要求更高,耗时长,假阳性率较高,因此在国内并不常用。
(c)联合染色:单一染色对早期食管癌及癌前病变的检出效率受到染色原理、染色剂浓度等因素影响,而联合染色法可使各染色方法取长补短。研究报道碘液-甲苯胺蓝染色法和碘液-亚甲蓝染色法对早期食管麟癌及癌前病变检出的准确率高于单独碘染色,且对病变浸润程度评估也有一定价值。
C.电子染色内镜:通过特殊的光学处理实现对食管黏膜的电子染色,比白光内镜更能清楚显示黏膜表面结构、微血管的形态及病变范围,又可弥补色素内镜的染色剂不良反应及染色耗时长等不足。电子染色内镜和普通白光内镜之间可实现反复切换对比观察,操作更为简便。
窄带成像技术(narrow band imaging,NBI)已广泛应用于临床,其对早期食管癌的诊断价值已得到公认。研究发现NBI在食管鳞癌筛查方面较普通白光内镜有明显优势,另有研究报道其对食管鳞癌诊断的准确度和特异度优于碘染色,尚需更多研究进一步证实。利用NBI结合放大内镜观察食管上皮乳头内毛细血管袢(intrapapillary capillary loops,IPCL)和黏膜微细结构有助于更好地区分病变与正常黏膜及评估病变浸润深度,已成为早期食管癌内镜精查的重要手段。
智能电子分光技术(flexible spectral imaging color enhancement ,FICE)将白光分解成不同波段,可进行多达50种光谱组合,从而获得不同黏膜病变的最佳图像,可清晰显示IPCL,可作为碘染色的重要补充。智能电子染色内镜技术(I-Scan)增强了不同性质黏膜间颜色的对比,在表面增强、对比度、色调处理方面有了很大提升。
D.放大内镜(magnifying endoscopy):放大内镜是在普通内镜的前端配置了一个可调焦距的放大系统,可将食管黏膜放大几十甚至上百倍,有利于观察组织表面显微结构和黏膜微血管网形态特征的细微变化,尤其在与电子染色内镜相结合时,其对黏膜特征显示更为清楚,不仅可鉴别黏膜病变的良恶性,进一步提高早期食管癌检出的准确度,还可清晰显示病变的边界和范围,指导治疗方式的选择。
E.激光共聚焦显微内镜(confocal laser endomicroscopy,CLE):CLE可将组织放大至1000倍,从微观角度显示细胞及亚细胞结构,在无需活检的情况下即可从组织学层面区分病变与非病变区域,实现“光学活检”的效果。CLE可实时提供早期食管癌的组织学成像且精确度较高,省去了病理活检步骤,大大缩短诊断时间。利用对CLE三维重建图像对食管鳞状上皮表面成熟度进行评分,可有效区分鳞状上皮内瘤变和非肿瘤上皮,敏感度为81%,特异度超过90%。
F.自发荧光内镜(autofluorescence imaging,AFI):自发荧光内镜可将正常组织与病变组织自发荧光光谱的不同转换为成像颜色的差异,从而对其加以区分。但自发荧光内镜检查对设备要求比较高,检查费用昂贵,且发现食管鳞状上皮异型增生的敏感度和阳性预测值较低,目前临床应用较少。
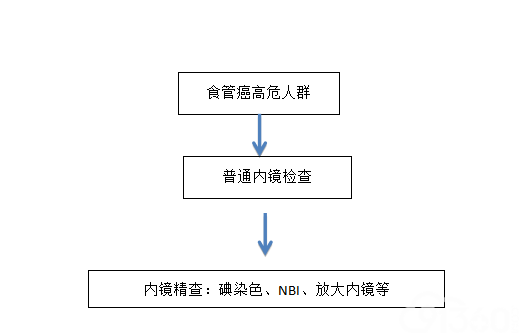
早期食管癌的内镜精查应以普通白光内镜检查为基础,全面细致地观察食管的各个部分,根据各医院的设备状况和内镜医师经验,综合使用染色内镜、放大内镜、共聚焦显微内镜等特殊技术可进一步突显早期食管癌的内镜下表现,并有助于了解病变范围、浸润深度及病理类型,指导治疗方案的选择。早期食管癌内镜精查流程详见图5。
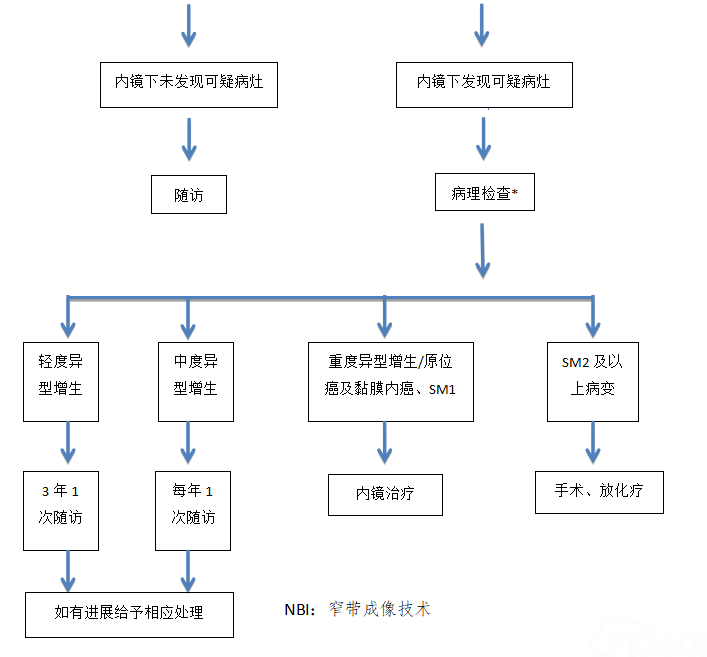
*病理检查主要为指示性活检,但对反映病变全貌有一定局限性,经仔细评估必要时可进行内镜下诊断性切除
图5食管癌筛查流程图
(3)早期食管癌及癌前病变的内镜下分型及病变层次
A.早期食管癌及癌前病变的内镜下分型:依照2002年巴黎分型标准和2005年巴黎分型标准更新版,表浅型食管癌及癌前病变(Type 0)分为隆起型病变(0-Ⅰ)、平坦型病变(0-Ⅱ)和凹陷型病变(0-Ⅲ)。0-Ⅰ型又分为有蒂型(0-Ⅰp)和无蒂型(0-Ⅰs)。0-Ⅱ型根据病灶轻微隆起、平坦、轻微凹陷分为0-Ⅱa、0-Ⅱb和0-Ⅱc三个亚型。0-Ⅰ型与0-Ⅱa型病变的界限为隆起高度达到1.0mm(与张开活检钳单个钳片的厚度1.2mm比较),0-Ⅲ型与0-Ⅱc型界限为凹陷深度达0.5 mm(与活检钳单个钳厚度的一半0.6mm比较)。同时具有轻微隆起和轻微凹陷的病灶根据隆起/凹陷比例分为0-Ⅱc+Ⅱa和0-Ⅱa+Ⅱc型;凹陷和轻微凹陷结合的病灶则根据凹陷/轻微凹陷比例分为0-Ⅲ+Ⅱc和0-Ⅱc+Ⅲ型。具体可参考图6。
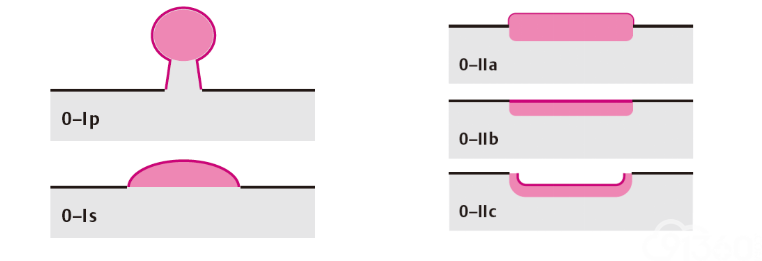
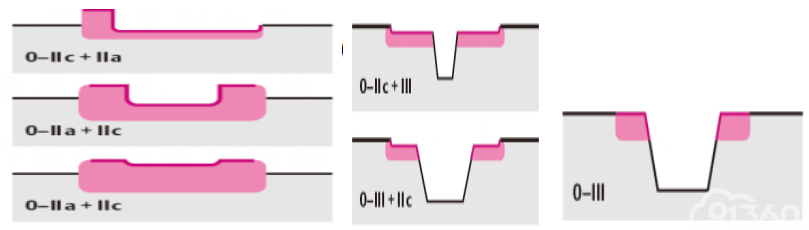
图6早期食管癌内镜下分型(巴黎分型,2005年)
B.病变层次分类:病变仅局限于上皮内(epithelium,EP),未突破基底膜者,为M1(原位癌/重度不典型增生;Tis);早期食管癌分为黏膜内癌和黏膜下癌:黏膜内癌分为M2和M3;M2指病变突破基底膜,浸润黏膜固有层(lamina propria mucosa,LPM);M3指病变浸润黏膜肌层(muscularis mucosa,MM)。黏膜下癌根据其浸润深度可分为SM1、SM2、SM3,SM1指病变浸润黏膜下层上1/3;SM2指病变浸润黏膜下层中1/3;SM3指病变浸润黏膜下层下1/3 。对于内镜下切除的食管鳞癌标本,以200μm作为区分黏膜下浅层和深层浸润的临界值,二者淋巴结转移风险有显著区别。
C.病变内镜下形态与病变层次的关系:通常,黏膜内癌表现为0-Ⅱb型、0-Ⅱa型及0-Ⅱc型,病灶表面光滑或呈规则的小颗粒状;而黏膜下癌通常为0-Ⅰ型及0-Ⅲ型,病灶表面呈不规则粗颗粒状或凹凸不平小结节状。应用上述标准,可初步预测病变浸润深度。我国学者将早期食管癌病理形态分为隐伏型(充血型)、糜烂型、斑块型和乳头型,隐伏型多为原位癌;糜烂性大部分为原位癌,部分为早期浸润癌,癌细胞分化较差;斑块型最多见,大部分为早期浸润癌,癌细胞分化较好;乳头型主要为早期浸润癌,癌细胞分化一般较好。
(4)活组织病理检查
内镜下发现可疑病变应行活检,活检的块数根据病变的范围和大小确定。提倡应用色素内镜、新型内镜技术进行指示性活检。黏膜活检取材要求标本应足够大,深度尽可能达到黏膜肌层。
3.早期食管癌内镜下治疗术前评估
(1)病灶范围、浸润深度及淋巴结转移评估
目前,对于无淋巴结转移的早期食管癌主张行内镜下微创治疗,而已有淋巴结转移或尚未发现淋巴结转移但风险较高的SM2、SM3食管癌,以及有远处转移的病变仍首选外科手术治疗,因此术前准确判断肿瘤浸润深度、范围及有无淋巴结转移是选择合理的治疗方式和评估预后的先决条件。判断肿瘤范围主要借助色素内镜和电子染色内镜,对浸润深度的评估则主要依靠超声内镜、鳞状上皮IPCL分型、病变内镜下形态等信息,但目前缺乏统一的标准,操作者经验水平易对诊断结果产生影响,准确的评估仍依靠术后标本的病理诊断。
超声内镜(Endoscopic ultrasound,EUS):EUS下早期食管癌的典型表现为局限于黏膜层且不超过黏膜下层的低回声病灶。EUS可清楚显示食管壁层次结构的改变、食管癌的浸润深度及病变与邻近脏器的关系,T分期的准确度可达74%~86%,但EUS对病变浸润深度诊断的准确度易受病变大小及部位的影响。EUS诊断局部淋巴结转移的敏感度为80%,明显高于CT(50%)及PET(57%),但特异度(70%)略低于后二者(83%和85%)。EUS对食管癌腹腔淋巴结转移的诊断敏感度和特异度分别为85%和96%,均高于CT(42%和93%)。 EUS联合FNA可进一步提高对可疑淋巴结转移的诊断效能。由于超声波穿透力有限,EUS难以用于远处转移的评估,应结合CT、MRI或PET-CT等影像学检查。
考虑到成本效益,本共识推荐可应用EUS等内镜技术联合增强CT获得淋巴结转移及远处转移的信息,进一步完善食管癌的术前分期。
(2)病理分型标准及临床处理原则
参照1998年维也纳消化道上皮肿瘤病理分型标准及其修订案(2002年),根据内镜和病理诊断,选择不同的临床处理方式(详见表1)。
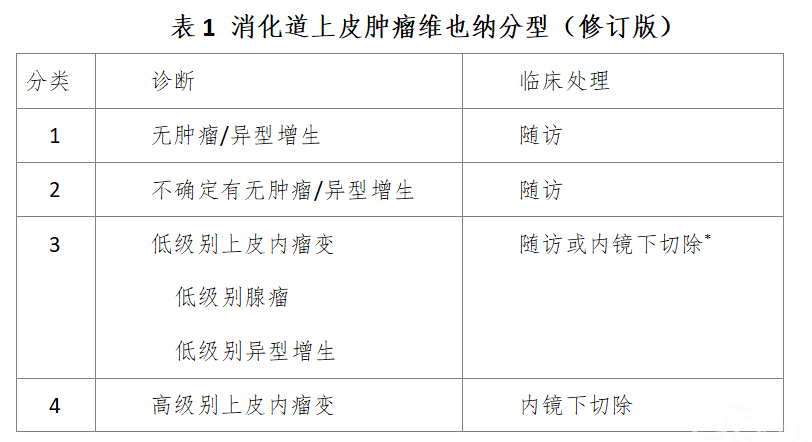
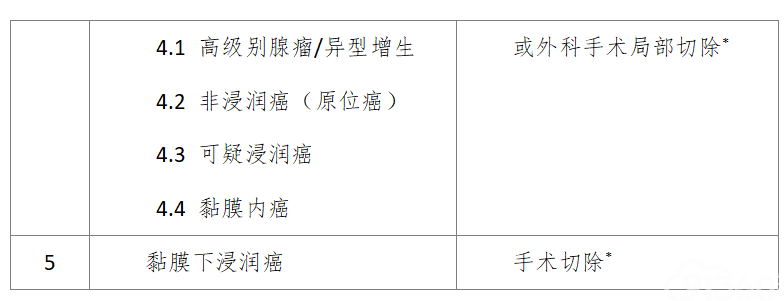
注:*处理方式的选择应综合考虑病变大小、浸润深度(通过内镜、放射影像或EUS等评估)以及患者年龄、伴随疾病等因素
4.早期食管癌内镜下治疗
(1)治疗原则
与传统外科手术相比,早期食管癌及癌前病变的内镜下切除具有创伤小、并发症少、恢复快、费用低等优点,且二者疗效相当,5年生存率可达95%以上。原则上,无淋巴结转移或淋巴结转移风险极低、残留和复发风险低的病变均适合进行内镜下切除,可作为符合条件的早期食管癌首选的治疗方式。
A.食管鳞癌适应证
(a)绝对适应证:
①病变局限在上皮层(M1)或黏膜固有层(M2)的T1a期食管鳞癌,未发现淋巴结转移的临床证据。
②癌前病变。
(b)相对适应证:
①病变浸润黏膜肌层(M3)或黏膜下浅层(T1b-SM1,黏膜下浸润深度<200?m),未发现淋巴结转移的临床证据。
②范围大于3/4 环周、切除后狭窄风险大的病变、同时有手术禁忌证者可视为内镜下切除的相对适应证,但应向患者充分告知术后狭窄等风险。
B.食管腺癌适应证
目前较为公认的内镜切除适应证为:
①直径小于或等于2cm、可完全切除和组织病理学评估证明良好或中度分化、深度不超过浅层黏膜下层,未发现淋巴结转移的临床证据。
②癌前病变。
所有经内镜切除的标本经规范病理处理后,必需根据最终病理结果,决定是否需要追加其他治疗。
C.禁忌证:
1.绝对禁忌证:
①明确发生淋巴结转移的病变。
②若术前判断病变浸润至黏膜下深层,有相当比例患者内镜下切除无法根治,原则上应行外科手术治疗。
③一般情况差、无法耐受内镜手术者。
2.相对禁忌证:
①非抬举征阳性。
②伴发凝血功能障碍及服用抗凝剂的患者,在凝血功能纠正前不宜手术。
③术前判断病变浸润至黏膜下深层,患者拒绝或不适合外科手术者。
(2)内镜下切除术
早期食管癌常用的内镜切除技术主要包括内镜下黏膜切除术(endoscopic mucosal resection,EMR)、内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)等。1989年,Saitoh等首次将EMR技术用于表浅食管鳞癌的切除。日本学者Hosokawa等设计并开始使用头端绝缘电刀(insulation-tipped knife,IT刀)治疗消化道早癌标志着内镜治疗进入了ESD时代,ESD技术的出现使较大消化道黏膜病灶的完整切除成为可能,消化道早癌和癌前病变的内镜切除适应证再次得到扩展。目前,食管ESD技术已趋于成熟。
A. EMR
(a)定义:EMR指内镜下将黏膜病灶整块或分块切除,用于胃肠道表浅肿瘤诊断和治疗的方法。
(b)方法:随着内镜器械的创新和内镜技术的进步,EMR技术不断发展。在传统的黏膜下注射-抬举-切除法的基础上逐渐演变出透明帽法(EMR with a cap,EMRC)、套扎法(EMR with ligation,EMRL)、分片黏膜切除术(endoscopy piecemeal mucosal resection,EPMR)等技术。各种EMR技术的基本原理相同,多是先通过黏膜下注射将黏膜下层与固有肌层分离,然后利用不同的方法切除局部隆起的黏膜病灶。
EMRC是利用内镜前端安置的透明帽对病变进行吸引,再行圈套切除,对操作技术要求不高,并发症少,但可切除的病变大小受透明帽的限制,具体操作步骤见图5。EMRL是先对病变进行套扎,阻断血流并形成亚蒂后切除,视野清晰,出血较少。EPMR用于传统EMR不能一次完整切除的较大病灶,将病灶分几部分切除,适用于>2cm的巨大平坦病变,但分片切除的组织标本体外拼接困难,难以评估根治效果,易导致病变局部残留或复发。
(c)疗效:国外文献报道,EMR可根除 57.9%~78.3%的T1a期食管癌和癌前病变,整块切除率可达46%~78.6%,5年生存率可达95%。国内报道,EMR治疗早期食管癌及其癌前病变,整块切除率为44.1% ~84.5%,完全切除率为44.8%~100%。
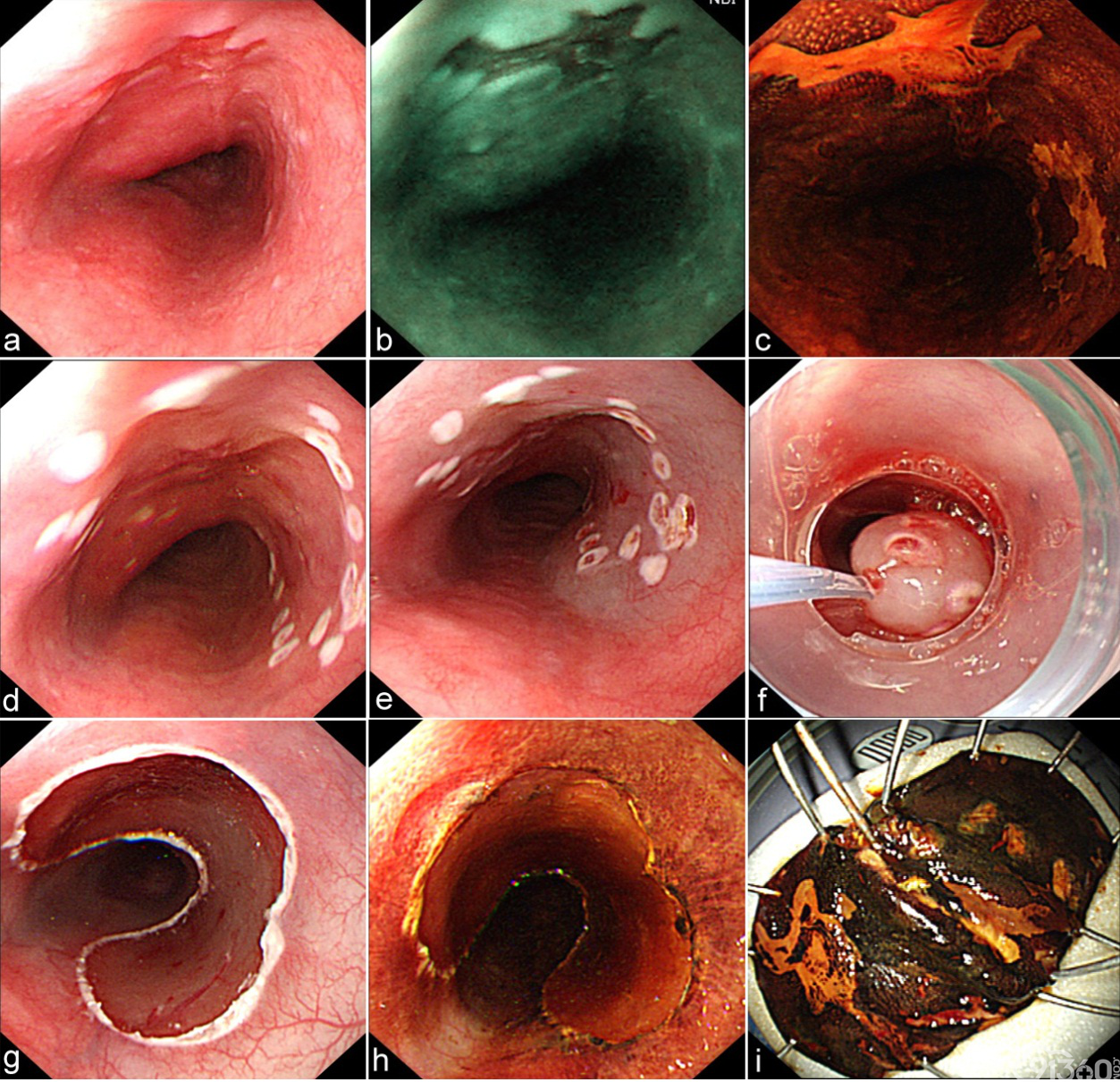
图5EMRC操作步骤
a 内镜下显示食管黏膜粗糙、糜烂,活检病理为重度异型增生;b NBI模式下病变呈深棕色;c 碘染色阳性;d 标记后;e 黏膜下注射后; f 透明帽法行内镜下黏膜切除;g 切除后创面;h 切除后重新碘染色,人工溃疡周围未见阳性病灶;i 切除的标本
B. 多环套扎黏膜切除术(multi-band mucosectomy,MBM)
MBM是在食管曲张静脉套扎器的基础上改良而来的多块黏膜切除技术,主要包括标记、圈套切除、处理创面等步骤。具体操作见图6。
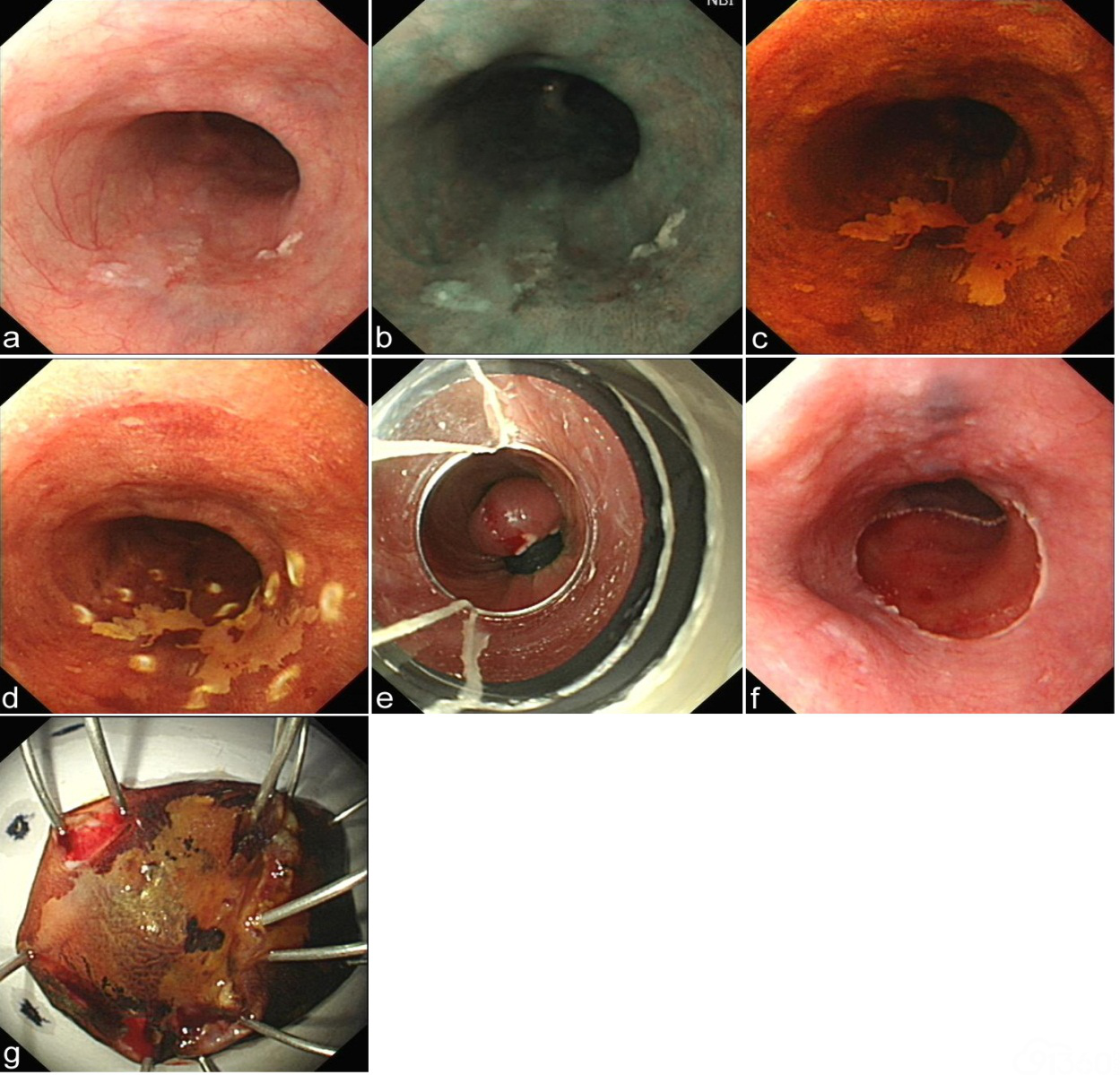

图6MBM操作步骤
a.白光内镜示食管黏膜糜烂,b.病变NBI图像 c.病变碘染色阳性;d.病变周边标记后;e.套扎切除;f.切除后创面;g.切除标本重建后
与EMR相比,MBM不需要行黏膜下注射,可显著缩短操作时间。同时,在保证相同治疗效果的前提下MBM较EMR具有操作简单、成本低、治疗时间短、安全高效的优点,便于在基层推广,应注意规范化操作,避免病变残留。
C.ESD
(a)定义:ESD是对不同部位、大小、浸润深度的病变,在进行黏膜下注射后使用特殊电刀逐渐分离黏膜层与固有肌层之间的组织,将病变黏膜及黏膜下层完整剥离的方法。
(b)操作步骤:操作大致分为5步:①病灶周围标记;②黏膜下注射,使病灶充分抬举;③部分或环周切开黏膜;④黏膜下剥离,使黏膜与固有肌层完全分离开,一次完整切除病灶;⑤创面处理:包括创面血管处理与病灶边缘检查。具体操作见图7。国内学者对经典ESD技术进行改进,发明了隧道式黏膜剥离技术(标记-注射-远端开口-近端切开-建立隧道-两边切开),是治疗大面积食管病变的理想方法,有效简化了操作步骤,缩短了内镜手术时间,使内镜手术更加安全快捷。
(c)疗效:ESD治疗早期食管癌在美国应用较少,欧洲近几年逐步开始使用。日本开展较多,ESD治疗食管鳞癌可达到93%~100%的整块切除率,完全切除率达88%以上。而国内ESD整块切除率为80%~100%,完全切除率为74%~100%,平均操作时间为40~95分钟。
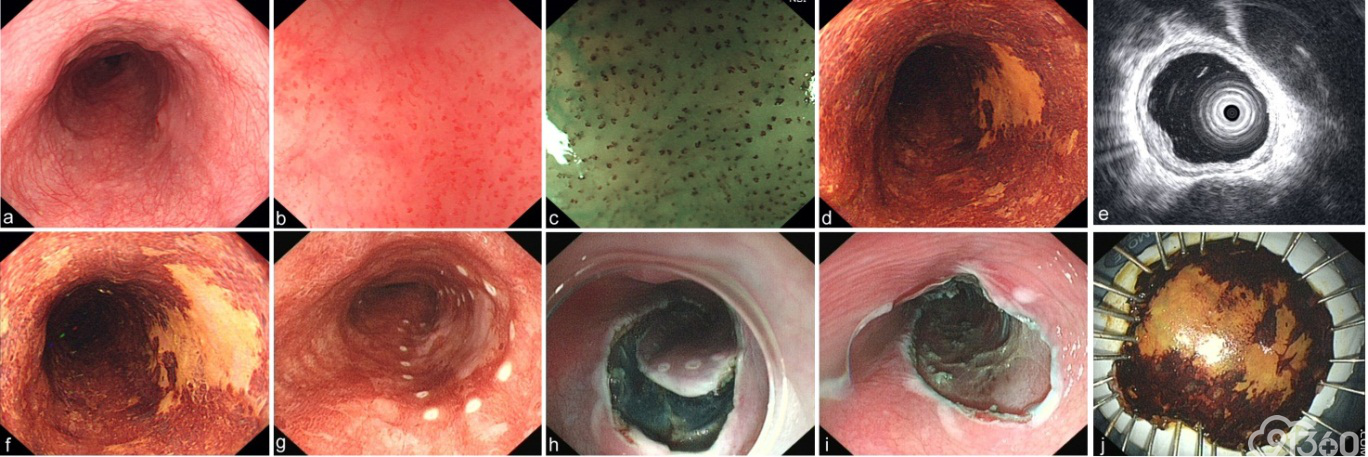
图7ESD操作步骤
a 白光内镜示病变处食管黏膜粗糙,树枝状血管网消失;b 白光放大内镜观察病变处IPCL分型;c NBI观察病变处IPCL分型,为Ⅳ型(井上晴洋分型);d 碘染色阳性;e 超声内镜显示病变主要位于黏膜层;f 仔细观察病变边界;g 标记后;h 黏膜下注射后切开黏膜;i 完整剥离病变并仔细检查创面;j 切除后标本
(3)适应证和禁忌证
内镜下切除治疗主要用于淋巴结转移风险低且可能完整切除的食管癌病变。目前国内尚无统一规范的内镜下切除适应证,由于欧美食管癌发病率及鳞癌比例较低,加之内镜下切除技术的应用现状与我国差别较大,因此,国内早期食管癌内镜下切除治疗多以参考日本指南为主。
日本食道学会(JES)食管癌诊治指南(2012年版):早期食管癌内镜下切除的绝对适应证:病变局限在上皮层或黏膜固有层的T1a期食管癌,淋巴结转移风险极低,内镜下切除可获得根治。内镜下切除的相对适应证:病变浸润黏膜肌层(M3)或黏膜下浅层(T1b-SM1,黏膜下浸润深度<200μm)。黏膜下浸润深度超过200μm的病变发生淋巴结转移的比例高,内镜下治疗难以根治。
内镜治疗适应证多基于国外数据,目前有研究显示部分超出现有内镜治疗适应证的患者预后仍然较好,所以需要国内多中心研究进一步确定内镜下治疗的适应证。
目前,国内较为公认的早期食管癌和癌前病变内镜下切除的绝对适应证:病变层次局限在上皮层或黏膜固有层的食管癌(M1、M2);食管黏膜重度异型增生。内镜下切除的相对适应证:病变浸润黏膜肌层或黏膜下浅层(M3、SM1),未发现淋巴结转移的临床证据。范围大于3/4环周、切除后狭窄风险大的病变可视为内镜下切除的相对适应证,但应向患者充分告知术后狭窄等风险。内镜下切除的禁忌证:明确发生淋巴结转移的病变;若术前判断病变浸润至黏膜下深层及以上,原则上应行外科手术治疗;若患者拒绝或不适合外科手术,可考虑内镜下切除治疗。内镜下切除的相对禁忌证:非抬举征阳性;伴发凝血功能障碍及服用抗凝剂的患者,在凝血功能纠正前不宜手术;有食管静脉曲张者;一般情况差、无法耐受内镜手术者。
(4)操作相关并发症及处理
虽然内镜下切除属于微创治疗,但受设备器械、内镜技术方法、操作者经验、患者全身情况等因素的影响,仍存在一定的并发症发生率,主要包括出血、穿孔、术后食管狭窄、感染等。
A.出血:术中出血指术中需要止血治疗(如电凝或止血夹止血)的局部创面出血;术后迟发性出血指操作术后30天内出现呕血、黑便等征象,血红蛋白下降20g/L以上。
出血发生率及危险因素:国外文献报道,食管EMR相关出血率可达2%,ESD术中出血常见,术后迟发出血率不足1%。国内文献报道,EMR术中出血发生率为1.52%~11.7%,迟发性出血率为0~7.04%。ESD术中出血率为22.9%~59.6%,迟发性出血率为0~4.88%。EMR出血与切除病变的大小有一定的关系,病灶 >2.0 cm者出血机率增加,混合电流切除者易发生术中出血,凝固电流切除者易发生延迟性出血。食管ESD出血可能与病变部位、大小及类型、剥离层次、病变的黏连程度、血管分布、操作者的熟练程度等相关。
出血治疗原则及处理方法:术中出血多见,应根据情况选择最佳的止血方法。对于少量渗血,内镜喷洒肾上腺素生理盐水即可有效,而大量的渗血则可酌情选用内镜黏膜下注射肾上腺素生理盐水,或采用热活检钳钳夹止血以及APC止血,也可用止血夹夹闭出血部位进行止血。术后出血相对少见,若患者血流动力学稳定,经保守治疗一般可恢复;而支持治疗后仍存在血流动力学不稳定,则需急诊内镜下电凝、止血夹确切有效止血,极少需要外科手术。术中出血多因操作中损坏黏膜下血管所导致,因此,操作中采取必要的预防措施是极为重要的,包括黏膜下注射液中加入肾上腺素生理盐水以收缩血管,术中应用热活检钳对可疑血管进行钳夹电凝处理等。病变切除后仔细处理创面,对可见血管进行预凝,有助于预防术后出血。术后应用止血药和抗酸剂也可达到预防出血的效果。
B.穿孔:食管EMR穿孔较少,但ESD相关穿孔并不少见。术中穿孔可及时发现。术后患者出现前胸和颈部皮下气肿,胸部平片或CT发现纵隔气体或查体见穿孔征象等,应考虑术后穿孔。
穿孔发生率及危险因素:国外文献报道,EMR穿孔率不超过2%,ESD穿孔率2~10%。国内文献报道,EMR穿孔率小于6.3%,ESD穿孔率0~11.5%。ESD穿孔与操作者经验、病变部位及大小、病变处有无溃疡形成等相关。操作过程中使用CO2气体及预防性夹闭肌层破损处可降低穿孔发生率,而创面处肌层暴露则会增加穿孔风险。消化道内积聚大量气体,容易使小的肌层裂伤形成穿孔,因此,操作过程中应及时抽吸消化道内的气体。严格掌握内镜切除适应证、充分的黏膜下注射及选用合适的器械也有利于预防穿孔发生。
穿孔治疗原则及处理方法:术中及时发现穿孔,后续操作应减少注气注水,切除结束后行内镜下夹闭,术后予禁食、胃肠减压、静脉使用广谱抗生素及支持治疗等保守治疗多可恢复,有利于降低外科手术率。内镜夹闭失败或穿孔较大内镜无法夹闭时,可能需要外科手术,以防病情进展。穿孔并发气胸时,应及时进行负压引流。隐形穿孔保守治疗多可痊愈。
C.食管狭窄:指内镜切除术后需要内镜下治疗的食管管腔狭窄,常伴有不同程度的吞咽困难,多在术后1个月出现。
狭窄发生率及危险因素:病变大小、浸润深度及创面的环周比例和纵向长度对食管内镜切除术后狭窄率影响较大,其中,切除范围大于3/4周及浸润深度超过M2是发生术后狭窄的独立危险因素。大于3/4环周的病变内镜切除术后狭窄发生率可达88%~100%。
狭窄治疗原则及处理方法:内镜下食管扩张术是最常规的治疗方法,多数狭窄经数次内镜下扩张可缓解,存在高危因素的病例术后行预防性食管扩张可降低狭窄发生率。支架置入可作为难治性病例的选择,但存在疼痛、肉芽组织长入支架、食管溃疡形成及部分支架不能取出等问题,近来有研究报道预防性覆膜支架置入可安全有效降低近环周食管ESD患者术后狭窄发生率。生物可降解支架因支架降解支撑力下降及移位等问题导致长期疗效不理想。口服或黏膜下注射糖皮质激素是预防狭窄的重要措施,通过口服或黏膜下注射激素可以降低狭窄的程度和减少扩张的次数。口服及局部注射糖皮质激素可有效预防术后狭窄发生,降低扩张需求,但最佳方案尚未达成共识。目前多采用如下方案:糖皮质激素局部注射方法如下,在ESD术后创面残留的黏膜下层注射曲安奈德(稀释至5mg/ml),注射通常在溃疡边缘开始、由远及近、线性注射,每个位点注射0.5~1ml,共注射20~40个位点,总量控制在100mg。也有文献报道,通过术后多次注射糖皮质激素预防狭窄,即在ESD术后残留的黏膜下层注射倍他米松,共注射8~10个位点,总量控制在4~8mg,每周1~2次直至创面完全上皮化。局部注射糖皮质激素切勿碰到肌层,否则存在发生迟发性穿孔的可能。口服糖皮质激素预防狭窄可分为长期(高剂量)和短期(低剂量)两种。长期(高剂量)口服泼尼松龙,术后第3天开始,计量依次递减,30mg/d×2周,25mg/d×2周,20mg/d×1周,15mg/d×1周,10mg/d×1周,5mg/d×1周,共计8周1120mg。短期(低剂量)口服泼尼松龙,术后第2天开始,计量依次递减,30mg/ d×1周,20mg/ d×1周,10mg/ d×1周,共计3周420mg。细胞补片等再生医学技术尚处研究阶段。
(5)内镜下非切除治疗
射频消融术(radiofrequency ablation,RFA)利用电磁波生物物理中的热效应发挥治疗作用,使肿瘤组织脱水、干燥和凝固坏死,从而达到治疗目的,在多发、病变较长或累及食管全周的早期食管癌及其癌前病变的治疗中具有明显的优势,且其治疗的深度控制在1000μm左右,降低了穿孔和术后狭窄的发生率。初步研究结果显示,RFA可用于Ⅱb型病变,且治疗前活检证实为食管鳞状上皮细胞中度异型增生和(或)重度异型增生及局限于M2层的中-高分化鳞癌。符合条件早期食管鳞癌及其癌前病变的RFA术后12个月完全缓解率可达97% 。但RFA对早期平坦食管鳞癌疗效的大样本量研究尚缺乏,长期疗效尚需进一步验证。环周型消融系统多应用于多发、延伸较长或环周病变的治疗,治疗过程包括记录消融位置、测量食管内径、置入消融导管进行消融等步骤,依据病变及第一次消融情况,可在清除已消融病变黏膜后行第二次消融(具体步骤见图8、图9),局灶型消融系统则多应用于局灶性病变及术后残余灶的处理,无需经过测量步骤。
内镜下非切除治疗方法还包括光动力疗法(photodynamic therapy,PDT)、氩离子凝固术(argon plasma coagulation,APC)、激光疗法、热探头治疗和冷冻疗法等。这些技术既可单独使用,也可与内镜切除术联合应用。PDT是利用特定激光激发选择性聚集于肿瘤组织的光敏剂产生单态氧,通过物理、化学和免疫等复杂机制导致肿瘤坏死的疗法,可用于处理大面积早期多灶病变,应注意光敏反应、术后穿孔狭窄等不良事件。APC是一种非接触性热凝固方法,可有效处理食管癌前病变,但应用于早期食管癌则需严格掌握适应证。非切除治疗方法致肿瘤毁损,但不能获得组织标本进行精确的病理学评估,也无法明确肿瘤是否完整切除,治疗后需密切随访,长期疗效还有待进一步研究证实。
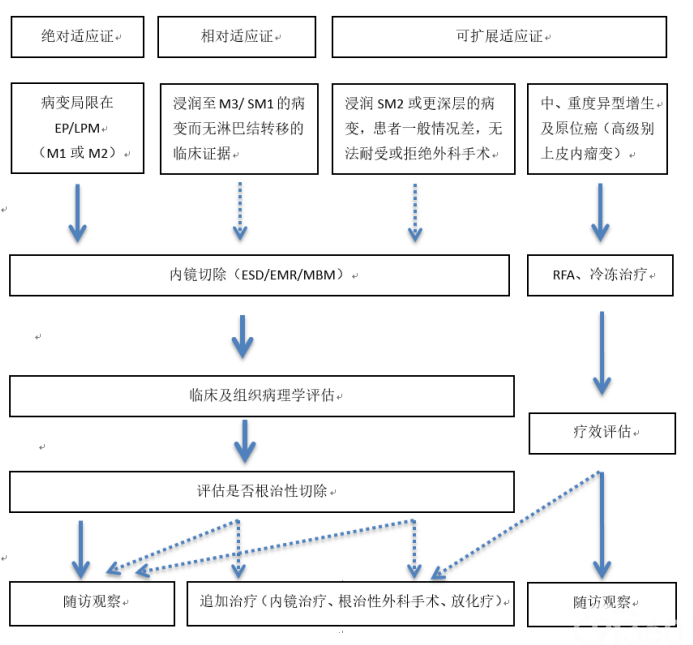
图8 早期食管癌内镜治疗流程
EMR:内镜下黏膜切除术;MBM:多环套扎黏膜切除术;ESD:内镜黏膜下剥离术;RFA:射频消融术
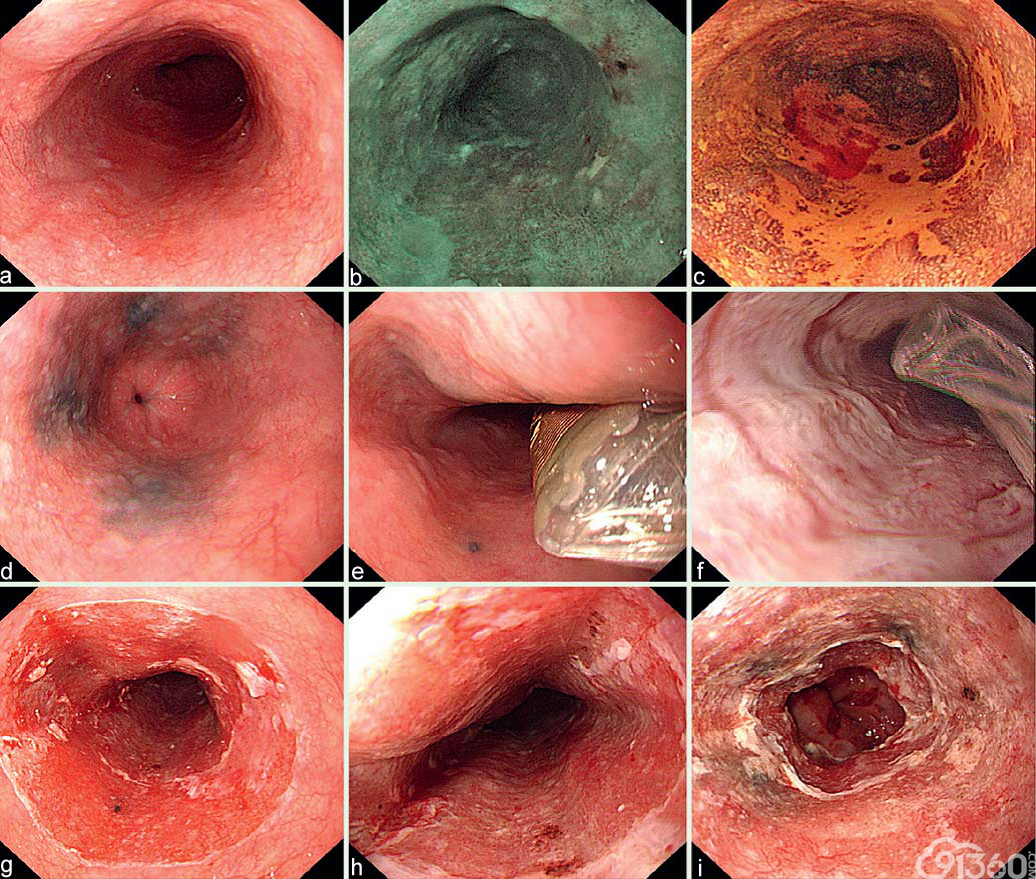
图9 RFA操作步骤
a 食管鳞状上皮重度异型增生,长约4cm、近乎全周;b 窄带成像图像;c 碘染色阳性;d,e 治疗范围近端和远端的标记;e RFA球囊置于近端标记处(6点位);f 第一次消融后黏膜的外观;g 清除消融后病变黏膜后的外观;h,i 第二次消融后近端(h)和远端(i)的黏膜外观
5.高危人群和内镜治疗后随访
轻度异型增生的患者随访要求3年/次,中度异型增生随访要求1年/次。内镜切除后随访要求3个月、6个月和12个月各复查1次内镜,若无复发,此后每年复查1次内镜。随访时应结合染色和(或)放大内镜检查,发现阳性或可疑病灶行选择性活检及病理诊断。另外,肿瘤标志物和相关影像学检查亦不可忽视。同时应警惕异时多原发食管鳞癌和第二原发癌(如头颈部鳞癌、胃癌等)。
复发的预防和处理:病变切除后应仔细检查创面,必要时使用染色或NBI进行观察,发现病变残留时应及时行再次内镜下处理,有利于降低复发率。局部残留和复发的病变多可通过内镜下治疗清除,内镜下治疗失败者可追加手术或放化疗。
(六)食管癌分期综合治疗模式
目前食管癌的治疗仍是以手术为主的综合治疗。对食管癌的治疗应在分期后由外科、放射治疗科、化疗科和内镜科等多学科联合讨论会诊后提出个体化综合治疗方案。以下采用的是UICC/AJCC分期(第8版)。
1.Ⅰ期(T1N0M0):Ⅰa期病变如果病变适合内镜治疗,首选内镜下黏膜切除或黏膜剥离术。如果病变过长>3cm 或过宽>3/4周径或侵及黏膜下层或有可疑淋巴结转移,建议行外科手术治疗。Ib期首选外科手术治疗。如心肺功能差或不愿手术者,可行内镜下ESD加术后放疗。完全性切除的Ⅰ期食管癌,术后一般不行辅助放疗或化疗。
2. ⅠB期、Ⅱ期和部分ⅢA期(T1b~3N0M0、T1~2N1M0)。首选外科手术治疗。如心肺功能差或不愿手术者,可行根治性放化疗。完全性切除的T2~3N0M0食管鳞癌,术后不行辅助放疗或化疗;对于完全性切除的术后病理报告为T4N0或T1~4N1~3M0食管鳞癌,但由于目前证据还不充分,术后可选择辅助放疗/化疗,亦可以选择观察。对于完全性切除的T2N0M0食管腺癌,术后不行辅助放疗或化疗;对于完全性切除的T3N0M0和T1-2N1M0食管腺癌,可以选择含氟嘧啶方案的术后放化疗。对于R1、R2的患者,选择含氟嘧啶方案的术后放化疗。
3.Ⅲ期(T3N1M0、T4N0~1M0):对于T1~3N1~2M0和部分T4aN0-1M0(侵及心包、膈肌和胸膜)可手术切除患者,推荐术前辅助放化疗或辅助放疗或辅助化疗后评估是否可手术治疗。
与单纯手术相比较,术前化疗的价值尚未确定,术前放疗可提高切除率,但并不能改善总体生存率。对于术前检查发现肿瘤外侵明显,外科手术不易彻底切除的食管癌,通过术前放疗可以增加切除率。术前放化疗可改善食管鳞癌患者总体生存率,因此,对于T3以上或有淋巴结转移的可切除患者术前可行辅助放化疗/化疗。对于无淋巴结转移的完全性切除的食管鳞癌患者,不推荐常规术后化疗。对于完全性切除的食管腺癌,可以选择含氟嘧啶方案的术后辅助放化疗。对于R1、R2的患者,选择含氟嘧啶方案的术后放化疗。
对于不能手术的Ⅲ期患者,目前的标准治疗是同步放化疗。
4.Ⅳ期(任何T,任何 N,M1,N3 或T4b):主要以化疗/放化疗/放疗为主。对于一般状况较好者(ECOG评分≤2或Karnofsky评分≥60分),可加用加化疗:①对于HER2高表达的腺癌一线化疗建议联合曲妥珠单抗。②腺癌二线和后续治疗雷莫卢单抗可单独应用或联合化疗。③二线和后续治疗如果MSI-H或dMMR可应用Pembrolizumab。④三线和后续治疗PD-L1阳性(PD-L1>1)的腺癌可应用Pembrolizumab。
一般状况不能耐受上述治疗者,以姑息和支持治疗为主要手段,治疗目的为延长生命,提高生活质量。
姑息治疗主要包括内镜治疗(包括食管扩张、食管支架等治疗)和止痛对症治疗及营养支持等。
(七)中医中药治疗
中医药治疗有助于改善手术后并发症,减轻放、化疗的不良反应,可以作为食管癌治疗的重要辅助手段。对于高龄、体质差、病情严重而无法耐受西医治疗的患者,中医药治疗可以作为辅助的治疗手段。
对于早期发现的食管癌前病变(如:食管溃疡与食管炎,食管黏膜白斑,食管上皮不典型增生,食管瘢痕狭窄等)可选择中医药治疗调理,且需要加以饮食结构、生活方式的调整,有可能延缓肿瘤的发生。
五、治疗指引图
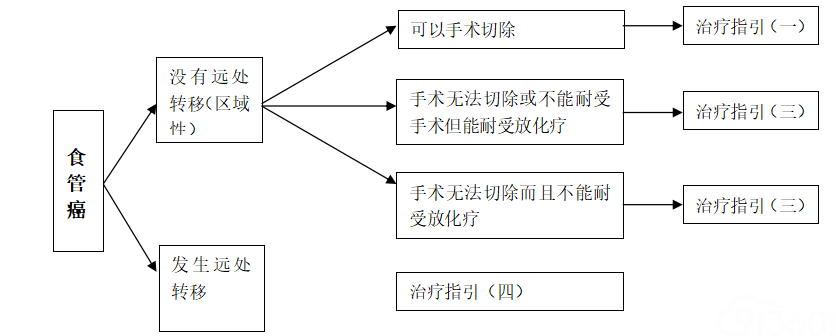
1、治疗指引(一)
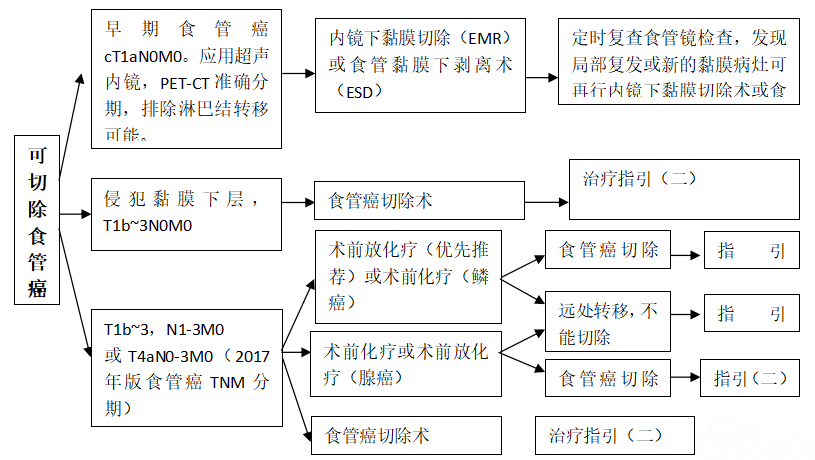
2、治疗指引(二)
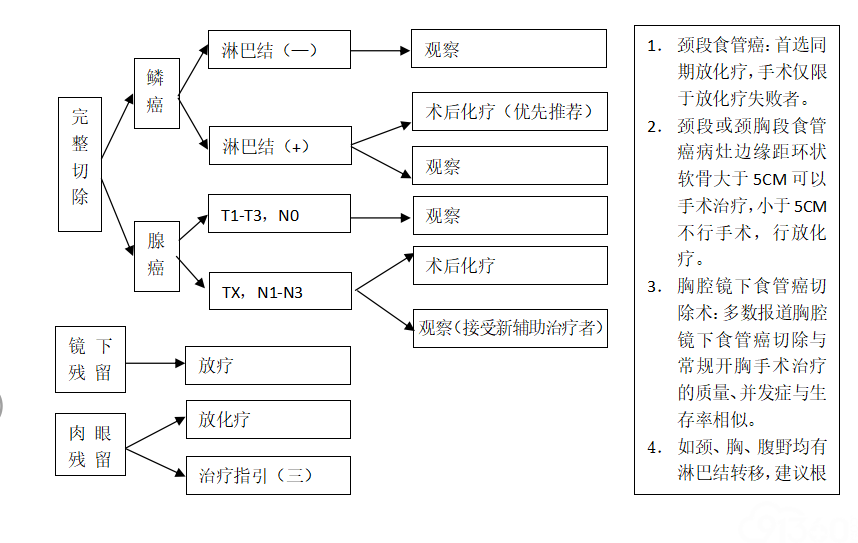
3、治疗指引(三)
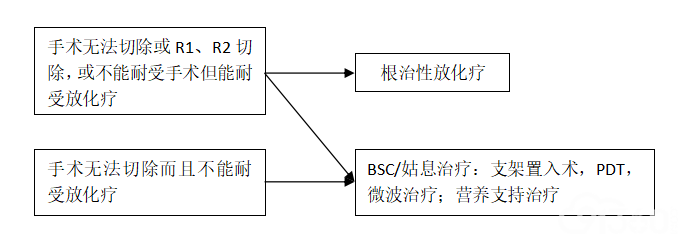
4、治疗指引(四)
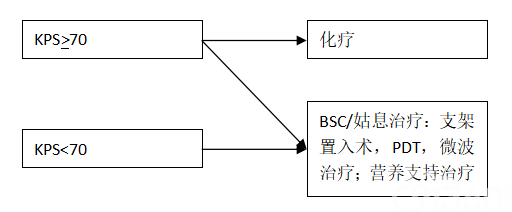
六、参考文献
诊断部分参考文献:
1.Esophageal cancer: Risk factors, screening and endoscopic treatment in Western and Eastern countries. World J Gastroenterol.2015 Jul 14;21(26) :7933-43.
2.Impact of (18)F-FDG PET/CT on the therapeutic management in the initial staging of the esophageal cancer. Rev Esp Med Nucl.2009 May-Jun;28(3):101-5.
3.Prognostic significance of tumor length in patients receiving esophagectomy for esophageal cancer. J Surg Oncol.2017 Dec;116(8):1114-1122.
4.Survival based radiographic-grouping for esophageal squamous cell carcinoma may impact clinical T stage. Oncotarget.?2018 Jan 9;9(10):9512-9530.
5.Value of oral effervescent powder administration for multidetector CT evaluation of esophageal cancer. Eur J Radiol.?2015 Feb;84(2):215-20.
6.Diagnosis of esophageal cancer and metastatic lymph node using CT and MRI. Nihon Rinsho.2011 Aug;69 Suppl 6:174-81
7.Role of clinically determined depth of tumor invasion in the treatment of esophageal carcinoma. J Thorac Cardiovasc Surg.2003 May;125(5):1091-102
8.NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines) , Esopageal and Esophagogastric Junction Cancer, Version 1.2018 — March 16, 2018.
9.Zhu W, Sun X, Xing L, et al. Oesophageal squamous cell carcinoma: relationship between fluorine - 18 fludeoxyglucose positron emission tomography CT maximum standardised uptake value, metabolic tumour volume, and tumour, node and 10.metastasis classification[J]. Bri J Radiol, 2014, 85(1016):383 -387.
11.Levine EA, Farmer MR, Clark P, et al.Predictive value of 18- fluorodeoxy- glucose- positron emission tomography(18F- FDG- PET) in the identification of responders to chemoradiation therapy for the treatment of locally advanced esophageal 12.cancer.Ann Surg,2006(243): 472-8.
13.Goel R,Subramaniam RM,Wachsmann JW, et al.PET/Computed Tomography Scanning and Precision Medicine:Esophageal Cancer.PET Clin. 2017 Oct;12(4):373-391.
病理部分参考文献
1.中国消化内镜活组织检查与病理学检查规范专家共识(草案). 中华消化杂志, 2014, 34(9): 577-581.
2.消化道黏膜病变内镜黏膜下剥离术治疗专家共识. 中华胃肠外科杂志, 2012, 15(10): 1083-1086.
3.中国早期食管癌筛查及内镜诊治专家共识意见(2014年, 北京). 胃肠病学, 2015, 20(4): 220-240.
4.中国早期食管鳞状细胞癌及癌前病变筛查与诊治共识(2015年, 北京). 中国医刊, 2016, 51(1): 17-31.
5.The Paris endoscopic classification of superficial neoplastic lesions: esophagus, stomach, and colon: November 30 to December 1, 2002. Gastrointestinal Endoscopy. 2003; 58(6 Suppl): S3-43.
6.Dawsey SM, Lewin KJ, Wang GQ, et al. Squamous esophageal histology and subsequent risk of squamous cell carcinoma of the esophagus: A prospective follow-up study from Linxian, China. Cancer, 1994, 74(6): 1686-1692.
7.Wang GQ, Abnet CC, Shen Q, et al. Histological precursors of oesophageal squamous cell carcinoma: Results from a 13 year prospective follow up study in a high risk population. Gut, 2005, 54(2): 187-192.
8.Xue L, Ren L, Zou S, et al. Parameters predicting lymph node metastasis in patients with superficial esophageal squamous cell carcinoma. Modern Pathology, 2012, 25(10): 1364-77.
外科部分及综合治疗参考文献
1.毛友生,赫捷,程贵余.我国食管癌外科治疗的现状与未来对策.中华肿瘤杂志,2010,32(6):401-404.
2.肖泽芬,杨宗贻,王绿化等.食管癌术后淋巴结转移对生存率的影响和放射治疗的意义. 中华肿瘤杂志2004,26(2):112-115.
3.彭林,陈利华,李强等.Ivor Lewis食管次全切除术和二野淋巴结清扫术及其对预后的影响.中国癌症杂志2003,13:574-576.
4.吴昌荣,薛恒川,朱宗海等.现代二野淋巴结清扫食管癌切除术的疗效分析.中华肿瘤
杂志2009,31:630-633.
5.安丰山,黄金球,陈少湖.217例胸段食管癌淋巴结转移及其对预后影响的分析.癌症
2003,22:974-977.
6.余志廉.食管癌颈胸腹淋巴结清扫研究.中国肿瘤2001,10:148-149.
7.Jun Ma, Cheng Zhan, Lin Wang, etal.The Sweet Approach Is Still Worthwhile in Modern Esophagectomy. Ann ThoracSurg 2014;97:1728–33.
8.Altorki N, Kent M, Ferrara C, Port J.Three-field lymph node dissection for squamous cell and adenocarcinoma of the esophagus.Ann Surg. 2002 Aug,236(2): 177-183.
9. Shimada H, Okazumi S, Matsubara H,etal.Impact of the number and extent of positive lymph nodes in 200 patients with thoracic esophageal squamous cell carcinoma after three-field lymph node dissection.World J Surg.2006Aug,30(8): 1441-1449.
10. Shiozaki H, Yano M, TsujinakaT,et al. Lymph node metastasis along the recurrent nerve chain is an indication for cervical lymph node dissection in thoracic esophageal cancer.Dis Esophagus. 2001;14(3-4): 191-6.
11..Luketich JD, Alvelo-Rivera M, Buenaventura PO, et al. Minimally invasive esophagectomy: outcomes in 222 patients. Ann Surg,2003,238(4):486-494.
12..Nafteux P,Moons J,Coosemans W,et al. Minimally invasive oesophagectomy: a valuable alternative to open oesophagectomy for the treatment of early oesophageal and gastro-oesophageal junction carcinoma. Eur J Cardiothorac Surg,?2011 ,40(6):1455-1463.
13.Sihag S,WrightCD,WainJC,etal.Comparison of perioperative outcomes following open verus minimally invasive Iv or Lewis oesophagectomy at a single, high-volume centre.Eur J Cardiothorac Surg,2012,42(3):430-437.
14.郭明,胡蒙,孙晓燕等.全胸腔镜联合非气腹腹腔镜辅助食管癌根治术与常规手术的对比研究.中国微创外科杂志2012,12(1):53-56.
15.Tsujimoto H, Takahata R, Nomura S, et al. Video-assisted thoracoscopic surgery for esophageal cancer attenuates postoperative systemic responses and pulmonary complications. Surgery2012,151(5): 667-673.
16.Biere SS, van Berge Henegouwen MI, Maas KW, et al. Minimally invasive versus open oesophagectomy for patients with oesophageal cancer: a multicentre, open-label, randomised controlled trial. Lancet2012 ,379(9829):1887-1892.
17.van der Sluis PC,Ruurda JP,van der Horst S,et al. Robot-assisted minimally invasive?thoraco-laparoscopic esophagectomy versus open transthoracicesophagectomy for resectable esophageal cancer, a randomized controlled trial (ROBOT trial). Trials?2012,13:230.
18.Zhang J,Wang R,?Liu S,et al. Refinement of minimally invasive esophagectomy techniques after 15 years of experience. J Gastrointest Surg2012,16(9): 1768-1774.
19.汪灏,谭黎杰,李京沛等.胸腔镜食管癌根治术的安全性评价.中华胃肠外科杂志2012, 15(9):926–929.
20.Zhang DW, Cheng GY, Huang GJ, et al. Operable squamous esophageal cancer: current results from the East[J]. World J Surg 1994; 18: 347-354.
21.Ando N, Iizuka T, Kakegawa T, et al. A randomized trial of surgery with and without chemotherapy for localized squamous carcinoma of the thoracic esophagus: the Japan Clinical Oncology Group Study[J]. J ThoracCardiovascSurg 1997; 114: 205-209.
22..Ando N, Iizuka T, Ide H, et al. Surgery plus chemotherapy compared with surgery alone for localized squamous cell carcinoma of the thoracic esophagus: a Japan Clinical Oncology Group Study--JCOG9204[J]. J ClinOncol 2003; 21: 4592-4596.
23.Ando N, Kato H, Igaki H, et al. A randomized trial comparing postoperative adjuvant chemotherapy with cisplatin and 5-fluorouracil versus preoperative chemotherapy for localized advanced squamous cell carcinoma of the thoracic esophagus (JCOG9907)[J]. Ann SurgOncol 2012; 19: 68-74.
24.Lee J, Lee KE, Im YH, et al. Adjuvant chemotherapy with 5-fluorouracil and cisplatin in lymph node-positive thoracic esophageal squamous cell carcinoma[J]. Ann ThoracSurg 2005; 80: 1170-1175.
25.Huang J, Zhou Y, Zhang H, et al.: A phase II study of biweekly paclitaxel and cisplatin chemotherapy for recurrent or metastatic esophageal squamous cell carcinoma: ERCC1 expression predicts response to chemotherapy. Med Oncol 2013;30:343.
26.Lyu X, Huang J, Mao Y, et al. Adjuvant chemotherapy after esophagectomy: Is there a role in the treatment of the lymph node positive thoracic esophageal squamous cell carcinoma?[J]. J SurgOncol 2014.110(7):864-8.
27.Teniere P, Hay JM, Fingerhut A, Fagniez PL. Postoperative radiation therapy does not increase survival after curative resection for squamous cell carcinoma of the middle and lower esophagus as shown by a multicenter controlled trial. French University Association for Surgical Research[J]. SurgGynecolObstet 1991; 173: 123-130.
28.Xiao ZF, Yang ZY, Liang J, et al. Value of radiotherapy after radical surgery for esophageal carcinoma: a report of 495 patients[J]. Ann ThoracSurg 2003; 75: 331-336.
29.Xiao ZF, Yang ZY, Miao YJ, et al. Influence of number of metastatic lymph nodes on survival of curative resected thoracic esophageal cancer patients and value of radiotherapy: report of 549 cases[J]. Int J RadiatOncolBiolPhys 2005; 62: 82-90.
30.Tachibana M, Yoshimura H, Kinugasa S, et al. Postoperative chemotherapy vs chemoradiotherapy for thoracic esophageal cancer: a prospective randomized clinical trial[J]. Eur J SurgOncol 2003; 29: 580-587.
31.Lv J, Cao XF, Zhu B, et al. Long-term efficacy of perioperative chemoradiotherapy on esophageal squamous cell carcinoma[J]. World J Gastroenterol 2010; 16: 1649-1654.
32.Chen J PJ, Liu J et al. Postoperative radiation therapy with or without concurrent chemotherapy for node-positive thoracic esophageal squamous cell carcinoma. Int J RadiatOncolBiol Phys. 2013;86(4):671-677.
33.陈万青, 郑荣寿, 张思维, et al. 2013年中国恶性肿瘤发病和死亡分析[J]. 中国肿瘤, 2017, 26(01): 1-7.
放疗部分参考文献
1.van Hagen P, Hulshof MC, van Lanschot JJ, et al. Preoperative chemoradiotherapy for esophageal or junctional cancer. N Engl J Med 2012, 366:2074 – 2084 .
2.Tepper J, Krasna MJ, Niedzwiecki D, et al. Phase III trial of trimodality therapy with cisplatin, fluorouracil, radiotherapy, and surgery compared with surgery alone for esophageal cancer: CALGB 9781. J Clin Oncol. 2008. 26(7): 1086-92.
3.Khushalani NI, Leichman CG, Proulx G, et al. Oxaliplatin in combination with protracted-infusion fluorouracil and radiation: report of a clinical trial for patients with esophageal cancer. J Clin Oncol. 2002. 20(12): 2844-50.
4.Ajani JA, Mansfield PF, Crane CH, et al. Paclitaxel-based chemoradiotherapy in localized gastric carcinoma: degree of pathologic response and not clinical parameters dictated patient outcome. J Clin Oncol. 2005. 23(6): 1237-44.
5.Ajani JA, Winter K, Okawara GS, et al. Phase II trial of preoperative chemoradiation in patients with localized gastric adenocarcinoma (RTOG 9904): quality of combined modality therapy and pathologic response. J Clin Oncol. 2006. 24(24): 3953-8.
6.Bedenne L, Michel P, Bouché O, et al. Chemoradiation followed by surgery compared with chemoradiation alone in squamous cancer of the esophagus: FFCD 9102. J Clin Oncol. 2007. 25(10): 1160-8.
7.van Hagen P, Hulshof MC, van Lanschot JJ, et al. Preoperative chemoradiotherapy for esophageal or junctional cancer. N Engl J Med. 2012. 366(22): 2074-84.
8.[8]Zhang ZX, Gu XZ, Yin WB, Huang GJ, Zhang DW, Zhang RG. Randomized clinical trial on the combination of preoperative irradiation and surgery in the treatment of adenocarcinoma of gastric cardia (AGC)--report on 370 patients. Int J Radiat Oncol Biol Phys. 1998. 42(5): 929-34.
9.Stahl M, Walz MK, Stuschke M, et al. Phase III comparison of preoperative chemotherapy compared with chemoradiotherapy in patients with locally advanced adenocarcinoma of the esophagogastric junction. J Clin Oncol. 2009. 27(6): 851-6.
10.Klevebro F, Alexandersson vDG, Wang N, et al. A randomized clinical trial of neoadjuvant chemotherapy versus neoadjuvant chemoradiotherapy for cancer of the oesophagus or gastro-oesophageal junction. Ann Oncol. 2016. 27(4): 660-7.
11.Gebski V, Burmeister B, Smithers BM, Foo K, Zalcberg J, Simes J. Survival benefits from neoadjuvant chemoradiotherapy or chemotherapy in oesophageal carcinoma: a meta-analysis. Lancet Oncol. 2007. 8(3): 226-34.
12.Sjoquist KM, Burmeister BH, Smithers BM, et al. Survival after neoadjuvant chemotherapy or chemoradiotherapy for resectable oesophageal carcinoma: an updated meta-analysis. Lancet Oncol. 2011. 12(7): 681-92.
13.Herskovic A, Martz K, al-Sarraf M, et al. Combined chemotherapy and radiotherapy compared with radiotherapy alone in patients with cancer of the esophagus. N Engl J Med. 1992. 326(24): 1593-8.
14.Xiao ZF, Yang ZY, Liang J, et al. Value of radiotherapy after radical surgery for esophageal carcinoma: a report of 495 patients. Ann Thorac Surg. 2003. 75(2): 331-6.
15.Yang J, Zhang W, Xiao Z, et al. The Impact of Postoperative Conformal Radiotherapy after Radical Surgery on Survival and Recurrence in Pathologic T3N0M0 Esophageal Carcinoma: A Propensity Score-Matched Analysis. J Thorac Oncol. 2017. 12(7): 1143-1151.
化疗部分参考文献:
1.Medical Research Council Oesophageal Cancer Working Group. Surgical resection with or without preoperative chemotherapy in oesophageal cancer: a randomised controlled trial.[J]. Lancet, 2002, 359(9319):1727-1733.
2.Ando N, Kato H, Igaki H, et al. A randomized trial comparing postoperative adjuvant chemotherapy with cisplatin and 5-fluorouracil versus preoperative chemotherapy for localized advanced squamous cell carcinoma of the thoracic esophagus (JCOG9907).[J]. Annals of Surgical Oncology, 2012, 19(1):68.
3.Cunningham D, Allum W H, Stenning S P, et al. Perioperative chemotherapy versus surgery alone for resectable gastroesophageal cancer.[J]. N Engl J Med, 2006, 355(1):11.
4.Ychou M, Boige V, Pignon J P, et al. Perioperative chemotherapy compared with surgery alone for resectable gastroesophageal adenocarcinoma: an FNCLCC and FFCD multicenter phase III trial.[J]. Journal of Clinical Oncology Official Journal of the American Society of Clinical Oncology, 2011, 29(13):1715-21.
5.Varadhachary, Gauri R. ASCO 2017: Gastrointestinal Cancer Updates[J]. Oncology Times, 2017, 39(15):1.
6.Ando N, Iizuka T, Ide H, et al. Surgery Plus Chemotherapy Compared With Surgery Alone for Localized Squamous Cell Carcinoma of the Thoracic Esophagus: A Japan Clinical Oncology Group Study-JCOG9204[J]. Journal of Clinical Oncology, 2003, 21(24):4592-4596.
7.Lee J, Lee K E, Im Y H, et al. Adjuvant Chemotherapy with 5-Fluorouracil and Cisplatin in Lymph Node-Positive Thoracic Esophageal Squamous Cell Carcinoma[J]. Annals of Thoracic Surgery, 2005, 80(4):1170-1175.
8.Zhang J, Zhang Y W, Chen Z W, et al. Adjuvant chemotherapy of cisplatin, 5-fluorouracil and leucovorin for complete resectable esophageal cancer: a case-matched cohort study in east China[J]. Diseases of the Esophagus, 2008, 21(3):207-213.
9.Lyu X, Huang J, Mao Y, et al. Adjuvant chemotherapy after esophagectomy: Is there a role in the treatment of the lymph node positive thoracic esophageal squamous cell carcinoma?[J]. Journal of Surgical Oncology, 2015, 110(7):864-868.
10.Cunningham D, Rao S, Starling N, et al. Randomised multicentre phase III study comparing capecitabine with fluorouracil and oxaliplatin with cisplatin in patients with advanced oesophagogastric (OG) cancer: The REAL 2 trial.[J]. Journal of Clinical Oncology, 2006, 24(18_suppl):182S-182S.
11.Dutton S J, Ferry D R, Blazeby J M, et al. Gefitinib for oesophageal cancer progressing after chemotherapy (COG): a phase 3, multicentre, double-blind, placebo-controlled randomised trial.[J]. Lancet Oncology, 2014, 15(8):894-904.
12.Petty R D, Dahlesmith A, Daj S, et al. Gefitinib and EGFR Gene Copy Number Aberrations in Esophageal Cancer.[J]. Journal of Clinical Oncology, 2017, 35(20):2279-2287.
13.Huang J, Fan Q, Lu P, et al. Icotinib in Patients with Pretreated Advanced Esophageal Squamous Cell Carcinoma with EGFR Overexpression or EGFR Gene Amplification: A Single-Arm, Multicenter Phase 2 Study.[J]. Journal of Thoracic Oncology Official Publication of the International Association for the Study of Lung Cancer, 2016, 11(6):910-917.
14.Crosby T, Hurt C N, Falk S, et al. Chemoradiotherapy with or without cetuximab in patients with oesophageal cancer (SCOPE1): a multicentre, phase 2/3 randomised trial.[J]. Lancet Oncology, 2013, 14(7):627-637.
15.Suntharalingam M, Winter K, Ilson D, et al. Effect of the Addition of Cetuximab to Paclitaxel, Cisplatin, and Radiation Therapy for Patients With Esophageal Cancer: The NRG Oncology RTOG 0436 Phase 3 Randomized Clinical Trial.[J]. Jama Oncology, 2017, 3(11).
16.Lorenzen S, Schuster T, Porschen R, et al. Cetuximab plus cisplatin–5-fluorouracil versus cisplatin–5-fluorouracil alone in first-line metastatic squamous cell carcinoma of the esophagus: a randomized phase II study of the Arbeitsgemeinschaft Internistische Onkologie[J]. Annals of oncology, 2009, 20(10): 1667-1673.
17.Lordick F, Kang Y K, Chung H C, et al. Capecitabine and cisplatin with or without cetuximab for patients with previously untreated advanced gastric cancer (EXPAND): a randomised, open-label phase 3 trial[J]. Lancet Oncology, 2013, 14(6):490-499.
18.Okines A F C, Ashley S E, Cunningham D, et al. Epirubicin, oxaliplatin, and capecitabine with or without panitumumab for advanced esophagogastric cancer: dose-finding study for the prospective multicenter, randomized, phase II/III REAL-3 trial[J]. Journal of Clinical Oncology, 2010, 28(25): 3945-3950.
19.Doi T, Piha-Paul S A, Jalal S I, et al. Updated results for the advanced esophageal carcinoma cohort of the phase Ib KEYNOTE-028 study of pembrolizumab (MK-3475)[J]. J Clin Oncol, 2016, 34(suppl 4S; abstr 7).
20.Kudo T, Hamamoto Y, Kato K, et al. Nivolumab treatment for oesophageal squamous-cell carcinoma: an open-label, multicentre, phase 2 trial[J]. Lancet Oncology, 2017, 18(5):631.
21.Huang J, Mo H, Wu D, et al. Phase I study of the anti-PD-1 antibody SHR-1210 in patients with advanced solid tumors[J]. J Clin Oncol 2017, 35(suppl_15):e15572.
内镜及筛查参考文献
1.王国清, 魏文强, 乔友林. 食管癌筛查和早诊早治的实践与经验[J]. 中国肿瘤. 2010; 19(1): 4-8.
2.王国清, 刘韵源, 郝长青, 等. 食管黏膜碘染色图像和浅表食管癌及癌前病变组织学的关系[J]. 中华肿瘤杂志. 2004; 26: 342-344.
3.Carvalho R, Areia M, Brito D, et al. Diagnostic accuracy of lugol chromoendoscopy in the oesophagus in patients with head and neck cancer[J]. Rev Esp Enferm Dig. 2013; 105(2): 79-83.
4.Dawsey S M, Fleischer D E, Wang G Q, et al. Mucosal iodine staining improves endoscopic visualization of squamous dysplasia and squamous cell carcinoma of the esophagus in Linxian, China[J]. Cancer. 1998; 83(2): 220-31.
5.Peng G, Long Q, Wu Y, et al. Evaluation of double vital staining with lugol's iodine and methylene blue in diagnosing superficial esophageal lesions[J]. Scand J Gastroenterol. 2011; 46(4): 406-13.
6.Uedo N, Fujishiro M, Goda K, et al. Role of narrow band imaging for diagnosis of early-stage esophagogastric cancer: current consensus of experienced endoscopists in Asia-Pacific region[J]. Dig Endosc. 2011; 23 Suppl 1: 58-71.
7.Muto M, Minashi K, Yano T, et al. Early detection of superficial squamous cell carcinoma in the head and neck region and esophagus by narrow band imaging: a multicenter randomized controlled trial[J]. J Clin Oncol. 2010; 28(9): 1566-72.
8.Nagami Y, Tominaga K, Machida H, et al. Usefulness of non-magnifying narrow-band imaging in screening of early esophageal squamous cell carcinoma: a prospective comparative study using propensity score matching[J]. Am J Gastroenterol. 2014; 109(6): 845-54.
9.李艳霞, 余世界, 沈磊, 等. 内镜智能分光比色技术对早期食管癌及癌前病变的诊断价值[J]. 中华消化内镜杂志. 2012; 29: 689-692.
10.Kodashima S, Fujishiro M. Novel image-enhanced endoscopy with i-scan technology[J]. World J Gastroenterol. 2010; 16(9): 1043-9.
11.Liu H, Li Y Q, Yu T, et al. Confocal laser endomicroscopy for superficial esophageal squamous cell carcinoma[J]. Endoscopy. 2009; 41(2): 99-106.
12.Li M, Zuo X L, Yu T, et al. Surface maturation scoring for oesophageal squamous intraepithelial neoplasia: a novel diagnostic approach inspired by first endomicroscopic 3-dimensional reconstruction[J]. Gut. 2013; 62(11): 1547-55.
13.李淑德, 许国铭, 李兆申. 荧光内镜在上消化道疾病诊断中的应用[J]. 国外医学:消化系疾病分册. 2003; 23: 282-284.
14.Ishihara R, Inoue T, Hanaoka N, et al. Autofluorescence imaging endoscopy for screening of esophageal squamous mucosal high-grade neoplasia: a phase II study[J]. J Gastroenterol Hepatol. 2012; 27(1): 86-90.
15.Ciocirlan M, Lapalus M G, Hervieu V, et al. Endoscopic mucosal resection for squamous premalignant and early malignant lesions of the esophagus[J]. Endoscopy. 2007; 39(1): 24-9.
16.Saitoh Y, Koyama S, Sai S, et al. [A case of superficial squamous cell carcinoma of the esophagus showing multicentric development][J]. Gan No Rinsho. 1989; 35(9): 1050-60.
17.Takekoshi T, Baba Y, Ota H, et al. Endoscopic resection of early gastric carcinoma: results of a retrospective analysis of 308 cases[J]. Endoscopy. 1994; 26(4): 352-8.
18.夏芸, 邹晓平, 吕瑛, 等. 内镜下分片黏膜切除术治疗早期食管癌及癌前病变[J]. 中国微创外科杂志. 2012; 12: 197-201.
19.Katada C, Muto M, Tanabe S, et al. Surveillance after endoscopic mucosal resection or endoscopic submucosal dissection for esophageal squamous cell carcinoma[J]. Dig Endosc. 2013; 25 Suppl 1: 39-43.
20.Zhang Y M, Bergman J J, Weusten B, et al. Radiofrequency ablation for early esophageal squamous cell neoplasia[J]. Endoscopy. 2010; 42(4): 327-33.
21.Bergman J J, Zhang Y M, He S, et al. Outcomes from a prospective trial of endoscopic radiofrequency ablation of early squamous cell neoplasia of the esophagus[J]. Gastrointest Endosc. 2011; 74(6): 1181-90.
22.Van Vilsteren F G, Alvarez Herrero L, Pouw R E, et al. Radiofrequency ablation for the endoscopic eradication of esophageal squamous high grade intraepithelial neoplasia and mucosal squamous cell carcinoma[J]. Endoscopy. 2011; 43(4): 282-90.
23.Tanaka T, Matono S, Nagano T, et al. Photodynamic therapy for large superficial squamous cell carcinoma of the esophagus[J]. Gastrointest Endosc. 2011; 73(1): 1-6.
24.王国清, 郝长青, 魏文强, 等.氩离子热凝固术治疗癌前病变和早期食管癌的远期效果[J]. 中华肿瘤杂志. 2013; 35: 456-458.
附录A:
食管癌的大体分型
早期/表浅食管癌推荐巴黎分型(同早期/表浅食管癌日本大体分型,即0型):
隆起型(0-Ⅰ):又可分为有蒂隆起型(0-Ⅰp)和无蒂隆起型(0-Ⅰs);
表浅型(0-Ⅱ):又可分为表浅隆起型(0-Ⅱa)、表浅平坦型(0-Ⅱb)和表浅凹陷型(0-Ⅱc)。同时具有表浅隆起和表浅凹陷的病灶根据表浅隆起/表浅凹陷的比例分为表浅凹陷+表浅隆起型(0-Ⅱc+Ⅱa型)和表浅隆起+表浅凹陷型(0-Ⅱa+Ⅱc型)。
凹陷(溃疡)型(0-Ⅲ):凹陷和表浅凹陷结合的病灶根据凹陷/表浅凹陷的比例分为表浅凹陷+凹陷型(0-Ⅱc+Ⅲ型)和凹陷+表浅凹陷型(0-Ⅲ+Ⅱc型)。
进展期食管癌推荐国内分型:
髓质型:以食管壁增厚为特点,边缘坡状隆起。
蕈伞型:肿瘤边缘隆起,唇状/蘑菇样外翻,表面可伴有浅溃疡。
溃疡型:少见,此类型也可见于早期癌。中央有明显溃疡,通常伴有边缘隆起(与Borrmann分型的2或3型对应)。
缩窄型:以管腔明显狭窄为特点,患者的吞咽困难症状明显。
腔内型:少见,此类型也可见于早期癌。病变像蘑菇样或大息肉样,有细蒂。
附录B:
附录B:



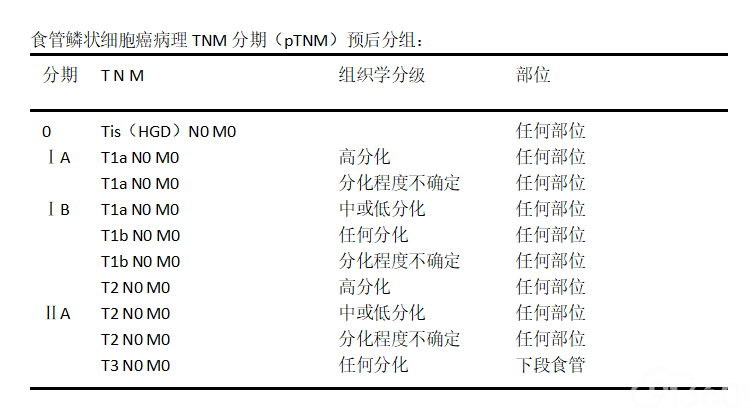
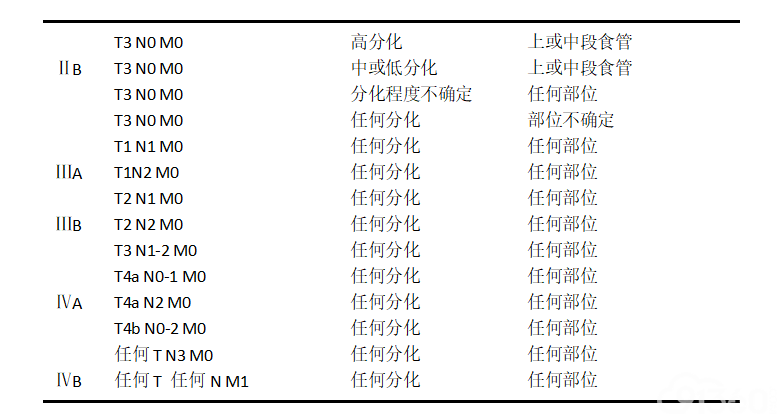
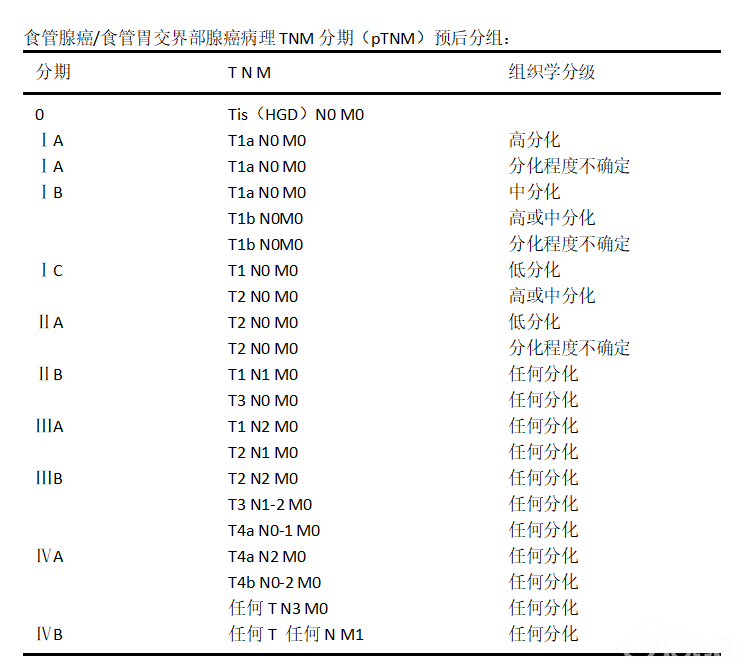
注释:
1.HGD,高级别上皮内瘤变/异型增生。
2.要达到准确分期,区域淋巴结的数目应该≥12个。
3.肿瘤部位按照肿瘤中心的位置分段(分上、中、下段,上段=颈段+胸上段,中段=胸中段;下段=胸下段+腹段)。
4.若肿瘤累及食管胃交界部,肿瘤中心在食管胃交界部食管侧者或在胃侧2cm之内者(Siewert分型Ⅰ型和Ⅱ型),按食管癌分期;肿瘤中心在近端胃2cm之外(Siewert分型Ⅲ型)按胃癌分期。肿瘤中心虽在近端胃2cm之内但未累及食管胃交界部者,按胃癌分期。
5.基底细胞样鳞状细胞癌、梭形细胞鳞状细胞癌、小细胞癌、大细胞神经内分泌癌及未分化癌按低分化鳞状细胞癌分期。混合有鳞状细胞癌成分的混合型癌(如腺鳞癌)或组织学类型不明确的按鳞状细胞癌分期。
6.食管的神经内分泌瘤(NET)十分罕见,其分期参照胃肠道神经内分泌瘤的TNM分期。
7.本分期不适用于非上皮性肿瘤,如淋巴瘤、肉瘤、胃肠道间质瘤和黑色素瘤等。


附录D:
新辅助治疗后病理学评估:
CAP(College of American Pathologists)/NCCN(The National Comprehensive Cancer Network)指南的新辅助治疗后病理学评估标准:
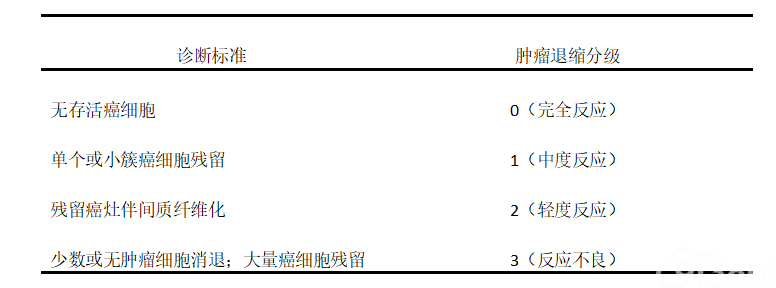
注释:1)肿瘤退缩分级只能在原发肿瘤评估,不适用于评估转移病灶;2)疗效评估根据存活肿瘤细胞决定,经过新辅助治疗后出现的无肿瘤细胞的角化物或黏液湖不能认为是肿瘤残留;淋巴结内出现无肿瘤细胞的角化物或黏液湖不能认为是肿瘤转移。
附录E:
Siewert分型:是Siewert等学者基于食管胃交界部的解剖学特点提出的分型,也称Munich分型。他们认为,远端食管腺癌和贲门腺癌应属同一种疾病,即食管胃交界部腺癌。食管胃交界部腺癌是指肿瘤中心位于解剖学上食管胃交界部(解剖学上的食管胃交界部是指管状食管变为囊状胃的部位,即食管末端和胃的起始,相当于希氏角或腹膜返折水平或食管括约肌下缘,与组织学上的鳞柱交界不一定一致)上、下各5cm这段范围内的腺癌。可分为三型:
Ⅰ型:相当于远端食管腺癌,肿瘤中心位于食管胃交界部上1cm-5cm处。
Ⅱ型:相当于贲门腺癌,肿瘤中心位于食管胃交界部上1cm-下2cm处。
Ⅲ型:相当于贲门下腺癌,肿瘤中心位于食管胃交界部下2cm-5cm处。
附录F:
放射治疗及化学治疗疗效判定标准
1.WHO实体瘤疗效评价标准(1981):
完全缓解(CR),肿瘤完全消失超过1个月。
部分缓解(PR),肿瘤最大直径及最大垂直直径的乘积缩小达50%,其他病变无增大,持续超过1个月。
病变稳定(SD),病变两径乘积缩小不超过50%,增大不超过25%,持续超过1个月。
病变进展(PD),病变两径乘积增大超过25%。
2.RECIST疗效评价标准(2000):
2.1靶病灶的评价
完全缓解(CR),所有靶病灶消失。
部分缓解(PR),靶病灶最长径之和与基线状态比较,至少减少30%。
病变进展(PD),靶病灶最长径之和与治疗开始之后所记录到的最小的靶病灶最长径之和比较,增加20%,或者出现一个或多个新病灶。
病变稳定(SD),介于部分缓解和疾病进展之间。
2.2非靶病灶的评价
完全缓解(CR),所有非靶病灶消失和肿瘤标志物恢复正常。
未完全缓解/稳定(IR/SD),存在一个或多个非靶病灶和/或肿瘤标志物持续高于正常值。
病变进展(PD),出现一个或多个新病灶和/或已有的非靶病灶明确进展。
3.最佳总疗效的评价
最佳总疗效的评价是指从治疗开始到疾病进展或复发之间所测量到的最小值。通常,病人最好疗效的分类由病灶测量和确认组成。
附录G:
急性放射性肺损伤和急性食管炎分级标准
1.急性放射性肺损伤RTOG分级标准:
0级:无变化。
1级:轻度干咳或劳累时呼吸困难。
2级:持续咳嗽需麻醉性止咳药/稍活动即呼吸困难,但休息时无呼吸困难。
3级:重度咳嗽,对麻醉性止咳药无效,或休息时呼吸困难/临床或影像有急性放射性肺炎的证据/间断吸氧或可能需类固醇治疗。
4级:严重呼吸功能不全/持续吸氧或辅助通气治疗。
5级:致命性。
2.急性食管炎诊断RTOG标准
0级:无变化。
1级:轻度吞咽困难,需要表面麻醉或止痛剂或软食。
2级:中度吞咽困难,需要麻醉剂或流食。
3级:重度吞咽困难,或脱水,或体重减轻15%需要管饲饮食。
4级:完全梗阻、溃疡或穿孔。
5级:致命性。


附录I:
术语和定义(适用本规范)
(一)、食管癌 esophageal cancer
从下咽食管起始部到食管胃结合部之间食管上皮来源的癌。包括食管鳞癌与食管腺癌两种主要类型及其他少见类型恶性肿瘤。
1.食管鳞状细胞癌 esophageal squamous cell carcinoma
起源于食管上皮并具有鳞状细胞分化的恶性上皮细胞肿瘤。
2.食管腺癌 adenocarcinoma of the esophagus
主要起源于食管下1/3的Barrett粘膜的腺样分化的恶性上皮细胞肿瘤,偶尔起源于上段食管的异位胃粘膜,或食管固有腺体。
(二)Barrett食管 Barrett esophagus
指食管下段的复层鳞状上皮被单层柱状上皮所代替。
(三)食管的癌前疾病和癌前病变
癌前疾病包括慢性食管炎、Barrett食管炎、食管白斑症、食管憩室、食管失弛缓症、食管管型、返流性食管炎和食管良性狭窄。
癌前病变是指以食管黏膜鳞状上皮内不同层次的异型鳞状细胞为特征的癌前病变,根据病变累及层次,分为低级别上皮内瘤变/异型增生(局限于鳞状上皮下1/2),高级别上皮内瘤变/异型增生(累及食管鳞状上皮超过下1/2,既往称原位癌)。
附录J:
缩略语(适用本规范)
UICC:国际抗癌联盟(International Union Against Cancer)
AJCC:美国癌症联合会(American Joint Committee on Cancer)
EMR:内镜下粘膜切除术(endoscopic mucosal resection)
ESD:内镜下粘膜剥离术(endoscopic submucosal dissection)
MBM:多环套扎黏膜切除术(multi-band mucosectomy)
VATS:胸腔镜辅助胸部手术(Video-assisted Thoracic
Surgery)
EUS:超声内镜(Endoscopic ultrasound)
CLE:激光共聚焦显微内镜(confocal laser endomicroscopy)
AFI:自发荧光内镜(autofluorescence imaging)
NBI:窄带成像技术(narrow band imaging)
GERD:胃食管反流病 (gastroesophageal reflux disease)
责任编辑: 大黄






 苏公网安备 32011402011742
苏公网安备 32011402011742