
前言:非小细胞肺癌中MET基因异常包括MET ex14跳读突变、MET基因扩增和MET蛋白过表达。不同MET基因异常具有不同的临床意义和检测方法。最近发布的《非小细胞肺癌 MET临床检测中国专家共识》对MET基因的改变进行了详细介绍。本文重点介绍MET基因扩增在非小细胞肺癌中的临床意义,以及其检测方法。
MET基因扩增的临床意义及检测方法
非小细胞肺癌(NSCLC)是全球癌症相关死亡的最常见原因。大多数晚期NSCLC患者通常通过化疗可适度改善生存期。
近十年来,已发现许多NSCLC亚型,主要是腺癌,其特征为单一致癌事件驱动肿瘤生长。表皮生长因子受体(EGFR)基因突变、BRAF V600E突变以及间变性淋巴瘤激酶(ALK)和ROS1基因重排代表了腺癌的不同分子亚型,其对特异性靶向治疗敏感。大约25%的肺腺癌患者有靶向的驱动突变。然而,在亚洲人中,仅EGFR致癌突变就占腺癌患者的40-50%。但随着越来越多的分子亚型被发现,一些罕见基因的比例在未来会有所增高。其中包括c-Met、NTRK易位和RET易位的基因改变。2022年中华医学会病理学分会、国家病理质控中心、中华医学会肿瘤学分会肺癌学组、中国抗癌协会肺癌专业委员会、中国胸部肿瘤研究协作组联合发布的《非小细胞肺癌 MET临床检测中国专家共识》(下称《共识》)旨在推动MET基因规范化的临床检测,使得更多的病人从中获益。
MET 异常包括MET 14跳突、 MET基因扩增、MET基因点突变(主要是激酶区突变)、 MET基因融合及MET蛋白过表达等(图1),均可能导致MET信号通路的异常激活。MET基因扩增是指该基因拷贝数(gene copy number, GCN)增加, 包括局部扩增(focal amplification) 和多体(polysomy)2种形式。局部扩增是指MET基因(或合并周围区域)的拷贝数增加, 而位于染色体其他区域的基因的拷贝数没有明显变化;多体是指整条染色体(或染色体较大区段)的拷贝数增加。2种形式都可能导致METmRNA水平上调, 进一步增加MET蛋白表达, 从而增加激活状态的MET通路信号。MET基因扩增可作为原发性肿瘤驱动基因变异之一, 多种实体肿瘤中都有发现,NSCLC中原发MET基因扩增发生比例为 1%~5%。MET基因扩增与较高的组织学分级、较晚的临床分期以及不良预后相关。MET基因扩增更常继发于其他驱动基因阳性NSCLC患者靶向治疗后, 是 EGFR-TKI耐药的重要机制之一。继发MET基因扩增在EGFR信号通路被EGFR-TKI抑制时, 作为旁路信号途径绕过EGFR激活下游通路导致耐药。不同代 EGFR-TKI耐药后出现MET基因扩增比例不尽相同,根据文献数据,第一、二代 EGFR-TKI耐药后MET基因扩增的比例为5%~22%,第三代EGFR-TKI奥希替尼一线耐药后MET基因扩增比例为7%~15%,二线耐药后为5%~50% 。除EGFR-TKI外,MET基因扩增也是ALK-TKI耐药机制之一,第二、三代ALK-TKI耐药后MET基因扩增的比例约为13%。临床研究数据表明,EGFR-TKI 联合MET抑制剂可能是继发MET基因扩增导致的 EGFR-TKI耐药患者的潜在治疗策略。另有报道显示,ALK-TKI耐药后发生 MET基因扩增的患者应用MET抑制剂治疗也取得了一定的疗效,值得进一步探索和研究[1]。MET拷贝数增益包括多体或扩增。当携带MET的7号染色体存在多个拷贝时,就会发生多体性。扩增后,MET在7号染色体的一个特定臂(位于7q31)中发生区域或局灶性拷贝数增加,而在其他区域无变化。与多体相比,扩增更容易诱导癌基因。
因此,共识中指出,MET基因扩增是NSCLC的原发驱动基因变异, 也是EGFR-TKI和ALK-TKI耐药的重要机制之一,可作为晚期患者耐药后联合靶向治疗的潜在分子标志物,临床应重视MET基因扩增检测[1]。
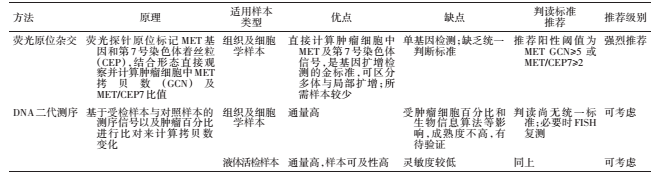
表1.非小细胞肺癌MET基因扩增常见检测方法

参考文献:
1.中华医学会病理学分会,中国病理质控中心,中华医学会肿瘤学分会肺癌学组《非小细胞肺癌MET临床检测中国专家共识》,中华病理学杂志,2022,51(11):1094-1103
1.中华医学会病理学分会,中国病理质控中心,中华医学会肿瘤学分会肺癌学组《非小细胞肺癌MET临床检测中国专家共识》,中华病理学杂志,2022,51(11):1094-1103




 苏公网安备 32011402011742
苏公网安备 32011402011742